يمكن أن يؤدي الضمادة الجراحية الفعالة للغاية المصممة لمرضى سرطان الجلد إلى تسريع عملية الشفاء بعد الجراحة. طورها باحثون في المملكة المتحدة والصين ، تستغل الضمادة أيضًا التأثيرات الحرارية الضوئية لمنع ظهور الأورام مرة أخرى.
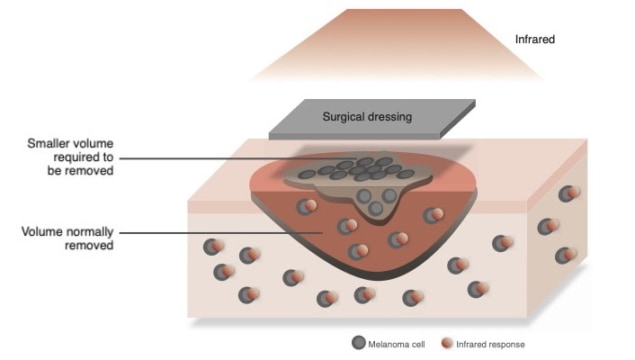
برز العلاج بالحرارة الضوئية (PTT) كطريقة واعدة لعلاج سرطان الجلد. إنه ينطوي على حقن الأورام بمواد نانوية موصلة تحول الضوء إلى حرارة ، ثم إلقاء الضوء عليها بأطوال موجية محددة لقتل الخلايا السرطانية. بالنسبة للأورام الكبيرة ، يجب إجراء هذا العلاج جنبًا إلى جنب مع الجراحة ، وترك الجروح التي يجب معالجتها بضمادات جراحية لمنع العدوى.
في الآونة الأخيرة ، تم اقتراح طرق علاج أكثر تقدمًا يتم فيها دمج PTT مباشرة في الضمادات الجراحية. الأمل هو أن هذه المواد يمكن أن تعزز التئام الجلد ، مع منع الأورام من الظهور مرة أخرى بعد العلاج. تعتمد التصميمات النظرية لهذه الضمادات على المادة الحرارية الضوئية المختزلة بأكسيد الجرافين (rGO). يمكن تصنيع هذه المادة عن طريق ربط المجموعات المحتوية على الأكسجين بصفائح الجرافين أحادية الطبقة ، ثم إخضاعها لعملية تقلل من محتواها من الأكسجين.
حاليًا ، تواجه هذه التقنية عائقًا رئيسيًا: rGO سامة للخلايا الحية ، مما يعني أنه لا يمكن استخدامها مباشرة في الضمادات الجراحية. قبل عملية الاختزال ، يمكن جعل أكسيد الجرافين أكثر توافقًا حيويًا من خلال دمجه مع الجزيئات الحيوية مثل الببتيدات والبروتينات. ومع ذلك ، من أجل تعزيز استجابتها الحرارية الضوئية ، يجب أن تتحمل المادة بعد ذلك عملية اختزال قاسية: يتم إجراؤها في مفاعل مغلق عند درجات حرارة تتجاوز 180 درجة مئوية ، في بيئة من الإيثانول النقي. أثناء تقليل أكسيد الجرافين للمادة ، يؤدي ذلك أيضًا إلى تدمير الهياكل الجزيئية الحيوية الأكثر حساسية المرتبطة بها.
الفريق بقيادة يوانهاو وو في جامعة نوتنغهام ، طور الآن تقنية جديدة تسمح لعملية الاختزال بالحدوث في درجات حرارة منخفضة. وهو يتضمن تجميعًا من رقائق أكسيد الجرافين ، مغلف ببوليمر حيوي بروتيني يسمى "مُعاد التركيب الشبيه بالإيلاستين" (ELR) ، والمعروف بقدرته على تعزيز إصلاح الجلد والتئام الجروح. من خلال التحكم في التفاعلات الجزيئية بين هذه الهياكل ، أنتج الفريق قلبًا متعدد الطبقات من أكسيد الجرافين ، محاطًا بقشرة ELR.
بعد ذلك ، عرّض الباحثون هذه التركيبة لمطهر يحتوي على 70٪ من الإيثانول. عادة ، يخترق هذا السائل مباشرة من خلال البكتيريا وقشور البروتين الخاصة بالفيروسات. في هذه الحالة ، مرت مباشرة من خلال غلاف ELR للتفاعل مع أكسيد الجرافين النقي بالداخل. سمح ذلك للفريق بإطلاق عملية الاختزال عند درجات حرارة أقل بكثير تبلغ 85 درجة مئوية ، مع ترك بنية ELR سليمة.
إجمالاً ، يجمع الهيكل النهائي بين كفاءة PTT العالية لـ rGO والقدرة على تعزيز تجديد الأنسجة. كمكافأة إضافية ، تم تعقيم المادة من خلال معالجتها بالإيثانول.

العلاج بالحرارة الضوئية ثلاثي الشقوق يقضي على الأورام في الفئران
تحقق الباحثون من صحة نهجهم باستخدام في الجسم الحي التجارب على الفئران ، مما يدل على أن الضمادات يمكن أن تمنع تكرار الورم وتعزز التئام الجروح بعد استئصال الورم. احتاجت المادة إلى 15 ثانية فقط من التعرض للضوء القريب من الأشعة تحت الحمراء كل 48 ساعة لتكون فعالة.
يأمل فريق وو أن تؤدي الضمادات الفريدة إلى علاجات عملية بعد الجراحة يمكن لمرضى سرطان الجلد تقديمها في المنزل: تسريع التئام جروحهم الجراحية ، ومنع الأورام من الظهور مجددًا مع تجدد بشرتهم.
تم وصف الدراسة في المواد الوظيفية المتقدمة.