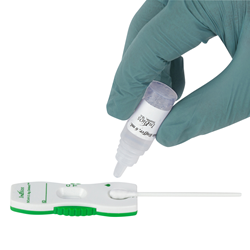
SCoV-2 Ag Detect Rapid Test
SEATTLE (PRWEB) August 22, 2021
InBios International Inc., en førende udvikler af diagnostiske tests for nye infektionssygdomme, meddelte i dag, at laboratorieundersøgelser tyder på, SCoV-2 Ag Detect Rapid Test vil opdage Delta-varianten (afstamning B.1.617.2), som er ansvarlig for en hurtig stigning i infektioner og dødsfald i USA og rundt om i verden. Indledende undersøgelser tyder på, at InBios' point-of-care antigentest vil detektere Delta-varianten ved hastigheder svarende til USA-WA1-2020-isolatet, der blev brugt til at udvikle analysen.
"At have en hurtig test, der hurtigt og præcist kan detektere Delta-varianten, er af største vigtighed, da denne variant viser sig at være meget overførbar og spredes hurtigt," sagde Dr. Syamal Raychaudhuri, Chief Scientific Officer hos InBios. "Vi er glade for, at undersøgelser tyder på, at vores hurtige test kan være et fantastisk diagnostisk værktøj til at lokalisere Delta-varianten, som har vist sig at være den største udfordring lige nu i kampen mod COVID-19."
Ifølge Centers for Disease Control and Prevention er Delta-varianten mere smitsom og fører til øget overførbarhed sammenlignet med andre varianter, selv hos vaccinerede individer. Delta-varianten, der først blev identificeret i Indien, anslås nu at udgøre 86 % af alle sekventerede COVID-19-tilfælde i USA For første gang siden februar har USA i gennemsnit mere end 100,000 nye COVID-19-tilfælde om dagen.
InBios SCoV-2 Ag Detect Rapid Test modtog Emergency Use Authorization (EUA) fra US Food and Drug Administration (FDA) i maj 2021. Finansiering til at opnå EUA til SCoV-2 Ag Detect Rapid Test kommer delvist fra en kontrakt på $12.7 millioner med US Army Medical Materiel Development Activity med finansiering leveret af Defense Health Agency (DHA) gennem CARES Act og Department of Health and Human Services (HHS) Biomedical Advanced Research and Development Authority (BARDA) tildelt i 2020. Testen er enkel og hurtig – den patentanmeldte Designet har en direkte nasal vatpind til kassetteformat. Det kræver ingen instrumentering eller transportmedietrin og kan udføres på stedet med resultater leveret på cirka 20 minutter.
Dette produkt er ikke blevet FDA-godkendt eller godkendt, men er blevet godkendt af FDA under en EUA til brug af autoriserede laboratorier. Dette produkt er kun godkendt til påvisning af proteiner fra SARS-CoV-2, ikke for andre vira eller patogener. Nødbrug af dette produkt er kun autoriseret i løbet af erklæringen om, at der eksisterer omstændigheder, der berettiger godkendelse af nødbrug af in vitro-diagnostik til påvisning og/eller diagnose af COVID-19 i henhold til § 564(b)(1) i Federal Food, Drug and Cosmetic Act, 21 USC § 360bbb-3(b)(1), medmindre erklæringen bringes til ophør eller godkendelse tilbagekaldes hurtigere.
For mere information om InBios COVID-19 test, besøg: http://www.inbios.com/covid-19/.
Besøg venligst for at få flere oplysninger om COVID-19 http://www.cdc.gov or http://www.who.int.
Om InBios: InBios International Inc. har specialiseret sig i design, udvikling og fremstilling af diagnostiske assays til nye infektionssygdomme og biotrusler. Beliggende i Seattle, Washington, tilbyder InBios produkter af overlegen kvalitet, som er nøjagtige, nemme at bruge og omkostningseffektive. InBios er GMP-kompatibel, FDA-registreret, USDA-licenseret og ISO 13485:2016 certificeret. For mere information, besøg http://www.inbios.com
Del artiklen om sociale medier eller e-mail:
