Med sine nysgerrige øjne, lodne snude og frodige skind sidder musen - med tilnavnet Xiao Zhu eller Lille bambus - smidigt på en bambusstilk og sætter en smuk pose for kameraet. Men denne mus findes ikke i naturen.
Fremstillet i et laboratorium i Beijing flytter Xiao Zhu grænsen for, hvad der er muligt for genteknologi og syntetisk biologi. I stedet for at huse de sædvanlige 20 par kromosomer, har musen og dens søskendekohorter kun 19 par. To bidder af forskellige kromosomer blev kunstigt smeltet sammen i et vovet eksperiment, der spurgte: i stedet for at justere individuelle DNA-bogstaver eller flere gener, kan vi genjustere en eksisterende genomisk spillebog engros, blande massive blokke af genetisk materiale rundt på samme tid?
Det er en måneskud idé. Hvis genomet er en bog, er genredigering som kopiredigering - at ændre en tastefejl her og der eller rette flere grammatiske fejl med omhyggeligt placerede tweaks.
Teknik på kromosomniveau er et helt andet dyr: Det er som at omarrangere flere afsnit eller flytte hele sektioner af en artikel og samtidig håbe på, at ændringerne tilføjer muligheder, der kan videregives til den næste generation.
At omprogrammere livet er ikke let. Xiao Zhus DNA-sammensætning er bygget af genetiske bogstaver, der allerede er optimeret af evigheder af evolutionært pres. Det er ingen overraskelse, at pille ved en etableret genomisk bog ofte resulterer i et liv, der ikke er levedygtigt. Indtil videre er det kun gær, der har overlevet ændringen af deres kromosomer.
ny undersøgelse, udgivet i Videnskab, gjorde teknologien mulig for mus. Holdet smeltede kunstigt sammen bidder fra musekromosomer. Et sammensmeltet par lavet af kromosomer fire og fem var i stand til at understøtte embryoner, der udviklede sig til sunde - om end noget mærkeligt opførte - mus. Bemærkelsesværdigt, selv med dette tektoniske skift til deres normale genetik, kunne musene reproducere og videregive deres manipulerede genetiske særheder til en anden generation af afkom.
"For første gang i verden har vi opnået fuldstændig kromosomomlejring hos pattedyr, hvilket gør et nyt gennembrud inden for syntetisk biologi," sagde studieforfatter Dr. Wei Li ved det kinesiske videnskabsakademi.
På en måde efterligner teknikken evolution i halsbrækkende fart. Baseret på eksisterende data om mutationsrater vil den type genetisk swap, der indføres her, generelt tage millioner af år at opnå naturligt.
Studiet er ikke perfekt. Nogle gener i de konstruerede mus var unormalt indstillet, hvilket ligner et mønster, der normalt ses ved skizofreni og autisme. Og selvom musene voksede til voksenalderen og kunne avle sunde unger, var fødselsraten langt lavere end hos deres ikke-udviklede jævnaldrende.
Alligevel er undersøgelsen en tour de force, sagde Evolutionsbiolog Dr. Harmit Malik ved Fred Hutchinson Cancer Center i Seattle, som ikke var involveret i undersøgelsen. Vi har nu dette "smukke værktøjssæt" til at tackle udestående spørgsmål vedrørende genomiske ændringer i større skala, hvilket potentielt kan kaste lys over kromosomsygdomme.
Vent, hvad er kromosomer igen?
Værket tager udgangspunkt i evolutionens mangeårige genetiske spillebog til at bygge nye arter.
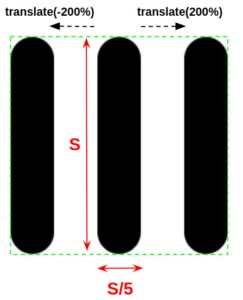
Lad os bakke op. Vores gener er kodet i DNA-dobbelthelix-kæder, som ligner bånd, der flyder inde i cellen. Det er ikke pladsbesparende. Naturens løsning er at vikle hver kæde omkring en proteinspole, som skiver af prosciutto snoet over en mozzarellastang. Yderligere drejninger pakker disse strukturer ind i bittesmå pukke - billedperler på en snor - som derefter pakkes ind i kromosomer. Under mikroskopet ligner de for det meste bogstavet X.
Hver art bærer et bestemt antal kromosomer. Menneskelige celler - bortset fra sæd og æg - rummer alle 46 individuelle kromosomer arrangeret i 23 par, arvet fra hver forælder. Laboratoriemus har derimod kun 20 par. Det komplette sæt af kromosomer kaldes karyotypen, afledt af det græske ord "kerne" eller "frø".
Blanding og matchning af kromosomer har længe været en del af evolutionen. Ifølge nuværende skøn akkumulerer en gnaver generelt omkring 3.5 kromosomomlejringer hver million år; nogle segmenter bliver slettet, andre duplikeres eller blandes. For primater er ændringshastigheden omkring det halve. At skifte rundt i bidder af kromosomer kan virke drastisk for ethvert dyr, men når det er levedygtigt, baner ændringerne vejen for udvikling af helt andre arter. Vores kromosom to, for eksempel, blev smeltet sammen fra to separate kromosomer, men justeringen er ikke til stede i gorillaen, vores nære evolutionære fætter.
Den nye undersøgelse havde til formål at gøre en bedre end evolution: Ved hjælp af genteknologi spurgte den, kan vi kondensere millioner af års evolution ned til blot et par måneder? Det er ikke kun for videnskabelig nysgerrighed: Kromosomsygdomme ligger til grund for nogle af vores hårdeste medicinske gåder, såsom leukæmi hos børn. Forskere har tidligere udløst kromosomomlejring ved hjælp af stråling, men resultaterne var ikke let kontrollerbare, hvilket gjorde det umuligt for dyrene at føde nyt afkom. Her tog syntetiske biologer en mere målrettet tilgang.
Det første skridt er at finde ud af, hvorfor kromosomer er modstandsdygtige over for store ændringer i deres organisation. Som det viser sig, er et stort problem med at bytte - eller fusionere - kromosomstykker en biologisk særhed kaldet prægning.
Vi modtager kromosomer fra begge forældre, hvor hvert sæt indeholder lignende gener. Der er dog kun tændt for ét sæt. Hvordan processen med prægning fungerer, er stadig mystisk, men vi ved, at den begrænser embryonale cellers evne til at udvikle sig til flere typer modne celler og begrænser deres potentiale for genteknologi.
Tilbage i 2018, det samme hold fandt ud af, at sletning af tre gener kan tilsidesætte det prægede biokemiske program i stamceller. Her brugte de disse "ulåste" stamceller til genetisk at lappe to kromosompar sammen.
De satte først deres øjne på kromosom et og to, de to største i et musegenom. Ved hjælp af CRISPR huggede holdet kromosomerne fra hinanden, så de kunne bytte genetiske bidder og omforme dem til stabile genetiske konstruktioner. Celler, der husede kromosomændringen, blev derefter injiceret i oocytter - ægceller. De resulterende embryoner blev transplanteret ind i surrogathunmus for at modnes yderligere.
Byttet var dødbringende. Det kunstige kromosom, med kromosom to efterfulgt af kromosom et eller 2+1, dræbte det udviklende foster kun 12 dage efter undfangelsen. De samme to kromosomer fusioneret i den modsatte retning, 1+2, havde bedre held og gav levende unger med kun 19 kromosompar. Babymusene var unormalt store i forhold til deres størrelse, og virkede i flere tests mere ængstelige end deres normale jævnaldrende.
Et andet kromosomfusionseksperiment klarede sig bedre. Kromosom 4 og 5 er meget mindre i størrelse, og det resulterende embryo – kaldet 4+5 – udviklede sig til sunde museunger. Selvom de også manglede et kromosompar, virkede de overraskende normale: de var ikke så ængstelige, havde gennemsnitlige kropsvægte, og da de blev modne, fødte de unger, der også manglede et par kromosomer.
Med andre ord konstruerede holdet en ny karyotype i en pattedyrart, som kunne videregives gennem generationer.
En helt ny verden af syntetisk biologi?
For Malik handler det om skala. Ved at overvinde prægningsproblemet er "verden deres østers for så vidt angår genteknologi," han sagde til Videnskabsmanden.
Holdets næste mål er at bruge teknologien til at løse vanskelige kromosomsygdomme i stedet for at designe mutante arter. Kunstig evolution er næppe rundt om hjørnet. Men undersøgelsen viser den overraskende tilpasningsevne af pattedyrs genomer.
"Et af målene inden for syntetisk biologi er at generere komplekst flercellet liv med designet DNA-sekvenser," skrev forfatterne. "At være i stand til at manipulere DNA i stor skala, herunder på kromosomniveau, er et vigtigt skridt mod dette mål."
Billedkredit: Chinese Academy of Sciences