Menschliche Proben
FFPE-Gewebe wurden gemäß institutionellen Protokollen gesammelt. Die Kontrollnierenproben wurden in Zusammenarbeit mit der Abteilung für Nephrologie und Klinische Immunologie der RWTH Aachen gesammelt. Nierenbiopsien von Patienten mit MCD und IgAN wurden aus dem Hamburger Glomerulonephritis-Register entnommen (https://www.sfb1192.de/en/register). Ethische Genehmigungen wurden vom Institutional Review Board des Universitätsklinikums der RWTH Aachen eingeholt (EK-016/17); die Ethik-Kommission der Ärztekammer Hamburg; und der örtlichen Ethikkommission der Ärztekammer Hamburg (PV4806). Sie alle stehen im Einklang mit den ethischen Grundsätzen der Deklaration von Helsinki.
Darüber hinaus wurden vom Institut für Neuropathologie des Universitätsklinikums Hamburg-Eppendorf Proben von Patienten mit Glioblastom und AD bereitgestellt. Die Studie wurde von der Ethikkommission der Hamburger Ärztekammer begutachtet (WF72/17). Eine Probe aus menschlicher Plazenta wurde von der Abteilung für Experimentelle Feto-Maternale Medizin, Abteilung für Geburtshilfe und Fetale Medizin, Universitätsklinikum Hamburg-Eppendorf bereitgestellt und von der Ärztekammer Hamburg genehmigt (PV7312).
Mäuseproben
Normales FFPE-Knochenmark der Maus wurde von der Abteilung für Entwicklungsbiologie und dem Oncode-Institut des Erasmus Medical Center Cancer Institute bereitgestellt. Gewebesammlungen wurden von der Tierschutz-/Ethikkommission des EDC gemäß der niederländischen Gesetzgebung (AVD1010020173387) genehmigt.
Kontroll-Maus-Nierengewebe und experimentelles IRI-Gewebe wurden in der Medizinischen Fakultät des Universitätsklinikums Hamburg-Eppendorf gesammelt. Alle Eingriffe erfolgten mit Genehmigung des Universitätsklinikums Hamburg-Eppendorf und des Landesamtes für Tierschutz Hamburg unter der Antrags-Nr. N002/2020. Anästhesie der Maus: 30 min vor der Operation, 0.05 mg kg-1 Buprenorphin wurde subkutan injiziert. Zum Zeitpunkt der Operation wurde die Narkose mit Isofluran (5 % Isofluran in reinem O) induziert und aufrechterhalten2 zur Induktion 2 % Isofluran in O2 für die Wartung). Induktion von IRI: Mäuse wurden anästhesiert und auf ein Heizkissen (39 °C) gelegt. Der Bauch wurde über eine mediane Laparotomie geöffnet und die Nierenarterie der rechten Niere 30 Minuten lang abgeklemmt (Mikro-Serrefine-Klemme, Fine Science Tools; 18055-03). Der Bauch wurde mit 0.9 % NaCl gefüllt und vorübergehend mit Parafilm (Bemis) verschlossen. Nach dieser Zeit wurde die Klemme entfernt, der Bauch mit einer 3.0-Naht verschlossen und die Anästhesie beendet. Die Tiere wurden wieder in ihre jeweiligen Käfige gesetzt und hatten freien Zugang zu weichem Futter und Wasser, gesüßt (acht Tropfen Natreen Classic) mit zugesetztem Metamizol (1.3 mg ml).-1, Ratiopharm). Endpunkt: Nach 24 Stunden wurde die Anästhesie erneut eingeleitet und der Bauch geöffnet. Abdominale Gefäße wurden freigelegt und die Nierenperfusion wurde über die Bauchaorta unter Verwendung von 4 % Paraformaldehyd in 1 × phosphatgepufferter Kochsalzlösung (PBS) bei 200 mmHg für 5 Minuten fixiert. Die Nieren wurden geerntet und bis zur weiteren Analyse in 4 % PFA bei 4 °C gelagert.
Der Dickdarm der Maus wurde aus Kontrollen und einem experimentellen Kolitismodell gewonnen. Alle Eingriffe erfolgten mit Genehmigung des Universitätsklinikums Hamburg-Eppendorf und des Landesamtes für Tierschutz Hamburg unter der Antrags-Nr. TVA17/13. Die Mäuse wurden unter spezifischen pathogenfreien Bedingungen in individuell belüfteten Käfigen mit Standardfutter und Wasser gehalten ad libitum. Es wurden alters- und geschlechtsangepasste B6-Wildtyp-Mäuse im Alter zwischen 8 und 12 Wochen verwendet. Während der Experimente wurden die Mäuse täglich überwacht. Den Mäusen der Interventionsgruppe wurde 1.8 Tage lang 36,000 % DSS-Salz (MP Biomedicals; Molekulargewicht 50,000–7 Da) im Trinkwasser verabreicht, um eine Kolitis auszulösen, während die Kontrollmäuse normales Wasser erhielten41.
Aus einem früheren Experiment wurden Archivgewebe aus einem experimentellen Modell von gestörtem GBM gewonnen. Die Entstehung dieser Mauslinie wurde in der Originalveröffentlichung beschrieben, zusammen mit der ethischen Genehmigung des Regierungspräsidiums Freiburg (G16-122) und der BGV Hansestadt Hamburg (Ü 004/2018).
Entparaffinierung und Antigengewinnung
Paraffinschnitte wurden in einer Dicke von 2–4 µm geschnitten und auf Superfrost Plus-Objektträger montiert. Anschließend wurden alle Proben nacheinander 3x (jeweils 10 Minuten) in Xylol getaucht, gefolgt von einer Ethanolserie (jeweils 5 Minuten) mit 3x 100 %, 2x 70 %, 1x 50 % und schließlich 3x (jeweils 5 Minuten). ) in doppelt entionisiertem Wasser. Die Antigengewinnung wurde mit Agilent DAKO Target Retrieval Solution bei pH 9 (Katalognr. S236884-2) in einem Braun Multiquick FS20 Steamer für 15 min durchgeführt, gefolgt von einer Abkühlung auf Raumtemperatur für 30 min. Anschließend wurden die Schnitte 800721 Minuten lang bei Raumtemperatur in Agilent Waschpufferlösung (Katalog-Nr. K2-15) inkubiert.
Fluoreszierende Immunmarkierung
Die Proben wurden mit primären Antikörpern in Konzentrationen gemäß den Herstellerrichtlinien in Agilent Antikörper-Verdünnungslösung (Katalog-Nr. K800621-2) über Nacht bei 4 °C inkubiert und anschließend dreimal 5 Minuten lang mit Agilent Waschpufferlösung gewaschen. Anschließend wurden die Schnitte mit geeigneten Sekundärantikörpern sowie direkt konjugierten Primärantikörpern in Konzentrationen gemäß den Herstellerrichtlinien mit DAPI (Sigma-Aldrich D9542) in einer Endkonzentration von 1 μg ml inkubiert-1 in Agilent Antikörper-Verdünnungslösung für 1 Stunde bei Raumtemperatur gewaschen und erneut dreimal für 5 Minuten mit Agilent Waschpufferlösung gewaschen. Die Pan-Protein-Färbung wurde unter Verwendung von NHS-Ester (Succinimidylester), konjugiert mit Alexa Fluor 555 (Invitrogen), durchgeführt A20009) gemäß den Richtlinien des Anbieters. Folgende Sekundärantikörper wurden verwendet: Ziegen-Anti-Meerschweinchen Alexa Fluor 488 (Invitrogen). A11073), Ziegen-Anti-Meerschweinchen Alexa Fluor 555 (Invitrogen A21435), Ziegen-Anti-Maus-IgG1 Alexa Fluor 488 (Invitrogen A21121), Ziegen-Anti-Kaninchen-Atto 647N (Sigma-Aldrich MFCD06798562), Ziegen-Anti-Ratten-Alexa Fluor 555 (Invitrogen). A21434) und Streptavidin Alexa Fluor 555-Konjugat (Invitrogen S21381). Nach der Immunfärbung wurden die Proben mit ProLong Gold (Invitrogen) fixiert P36930) für die Bildgebung vor der Erweiterung.
Fluoreszierende In-situ-Hybridisierung
Die fluoreszierende In-situ-Hybridisierung wurde in FFPE-Mausnierenproben unter Verwendung des RNAscope Multiplex Fluorescent Reagent Kit V2 Assay (Katalognr. 323100) gemäß den Richtlinien des Herstellers und wie zuvor beschrieben durchgeführt42. Die RNAscope-Sonde NPHS-1 von Advanced Cell Diagnostics (Katalognr. 43357) wurde zum Nachweis von NPHS-1-mRNA verwendet und der Farbstoff Opal 570 von Akoya Biosciences (Katalognr. OP-001003; Verdünnung 1:1,500) wurde zur Signalentwicklung eingesetzt.
Entfernen des Deckglases
Zuvor immunmarkierte Schnitte, die montiert und abgebildet wurden, wurden kurz für 5 Minuten bei Raumtemperatur in Xylol eingetaucht, wonach das Deckglas vorsichtig mit einer Rasierklinge entfernt wurde. Das Eindeckmedium wurde mit PBS 5 Minuten lang bei Raumtemperatur abgewaschen.
Primärantikörper
Die in dieser Studie verwendeten Primärantikörper und ihre jeweiligen Spezies und Verdünnungen sind wie folgt: AIF1 (Cell Signaling Technology 5318; Kaninchen, 1:200), aSMA/FITC-Konjugat (Abcam F3777; Maus, 1:200), Calreticulin (Abcam ab92516; Kaninchen, 1:200), CD42b (Abcam ab227669; Kaninchen, 1:200), Kollagen IV (Abcam ab6586; Kaninchen, 1:200), Cytokeratin 8 (R&D Systems MAB3165; Maus-IgG1, 1:200), Endomucin (Santa Cruz Biotechnology sc-65495; Ratten-IgG2a, 1:200), GFAP (Thermo Fisher Scientific 14-9892-82; Maus-IgG1, 1:200), MIB1 (Abcam ab124929; Kaninchen, 1:200), Nephrin (Progen GP- N2; Meerschweinchen, 1:100), Synaptopodin (Synaptic Systems 163 004; Meerschweinchen, 1:100), β-Amyloid (Thermo Fisher Scientific 715800; Kaninchen, 1:200), Vimentin (Progen GP53; Meerschweinchen, 1 :200), vWF (Agilent A008229-2; Kaninchen, 1:200), Laminin (Abcam ab11575; Kaninchen, 1:200) und CD144 VE-CAD (Thermo Fisher Scientific 14-1441-82; Ratte, 1:200) .
Gewebeexpansion
Protokolle zur Gewebeexpansion für eine verbesserte optische Auflösung in dünnen Schnitten wurden bereits beschrieben6. Kurz gesagt, immunmarkierte und fluoreszenz-in-situ-hybridisierte Schnitte wurden einer Verankerungsbehandlung mit 0.1 mg ml unterzogen-1 Acryloyl-X, 6-((Acryloyl)amino)hexansäure, Succinimidylester (Invitrogen A20770). Andererseits war für fluoreszenzin-situ-hybridisierte Schnitte keine weitere Verankerungsbehandlung erforderlich, da der RNAscope Multiplex Fluorescent Reagent Kit V2 Assay die proprietäre Tyramide-Signalverstärkungstechnologie von Akoya Biosciences nutzt, was zur kovalenten Ablagerung von OPAL-Farbstoffmolekülen an benachbarten Proteinen führt. Aliquots von Acryloyl-X wurden in wasserfreiem DMSO in einer Konzentration von 10.0 mg ml gelöst-1 zur Langzeitlagerung bei –20 °C und verdünnt in PBS auf die Endkonzentration von 0.1 mg ml-1 12 h bei Raumtemperatur stehen lassen. Gewebeschnitte wurden dann in eine Gelierlösung bestehend aus 1× PBS, 2 M NaCl, 8.625 % Natriumacrylat (Sigma-Aldrich 408220), 2.500 % Acrylamid (Sigma-Aldrich A3553), 0.100 % eingebettet. N-N′-Methylenbis-(acrylamid) (Sigma-Aldrich 146072), 0.010 % 4-hydroxy-2,2,6,6-tetramethyl-piperidin-1-oxyl (Sigma-Aldrich 176141), 0.200 % N,N,N′,N′-Tetramethylethylendiamin (Sigma-Aldrich T9281) und 0.200 % Ammoniumpersulfat (PanReac AppliChem, A1142). In die Gelierlösung eingebettete Abschnitte wurden dann 4 Minuten lang bei 30 °C inkubiert, um das Eindringen der Gelierlösung in das Gewebe zu ermöglichen. Anschließend wurden um das Gewebe herum Gelierkammern konstruiert, die jeweils aus zwei Deckgläschen als Abstandhalter auf beiden Seiten des Gewebes zur Verhinderung von Kompression und einem dritten Deckgläschen auf der Oberseite des Gewebes bestanden. Darüber hinaus wurden die Schnitte 37 Stunden lang in einem befeuchteten Ofen bei 2 °C inkubiert, um die Gelierung abzuschließen. Als nächstes wurden die Gelierkammern entfernt und die Proben in 8 U ml inkubiert-1 Proteinase K (Sigma-Aldrich P2308) in einem Tris/EDTA-basierten Verdauungspuffer (50 mM Tris (pH 8), 25 mM EDTA, 0.5% Triton X-100 und 0.8 M NaCl) bei 60 °C für 4 h. Nach der Verdauung wurden in Gel eingebettete Gewebeschnitte 60 Minuten lang in doppelt entionisiertes Wasser bei Raumtemperatur gelegt, um eine isotrope Expansion zu ermöglichen. Nach Abschluss der Expansion wurden die Gewebe aus dem doppelt entionisierten Wasser entnommen und zur anschließenden Bildgebung in Kammerobjektträger mit Glasboden (Ibidi µ-Slide-Glasboden mit zwei Vertiefungen; Katalog-Nr. 80287) montiert.
Montage und Erweiterung von Nanolinealen
ExM-kompatible Nanolineale, ausgestattet mit Acryditgruppen, um eine kovalente Bindung an die Polymermatrix während der Gelierung zu ermöglichen, und Biotin-Ankern, um eine Immobilisierung auf einer Rinderserumalbumin (BSA)-Biotin/NeutrAvidin-Oberfläche zu ermöglichen, wurden kundenspezifisch bei GATTAquant DNA Nanotechnologies bestellt. Um die Immobilisierung von Nanolinealen zu ermöglichen, wurden zunächst Glasobjektträger mit BSA-Biotin/NeutrAvidin beschichtet. Genauer gesagt wurden die Glasobjektträger zunächst dreimal mit 1,000 µl PBS gewaschen und anschließend mit 200 µl Pierce BSA, biotinyliert (Thermo Scientific 29130), in einer Konzentration von 1 µg ml inkubiert-1, gelöst in PBS, gefolgt von weiteren dreimaligem Waschen mit 1,000 μl PBS. Die Gewebe wurden dann mit 200 μl NeutrAvidin-Lösung (1 mg ml) inkubiert-1 NeutrAvidin-Protein (Thermo Scientific 31000), gelöst in PBS) für 5 min. Die NeutrAvidin-Lösung wurde durch dreimaliges Auftragen von 1,000 μl PBS, ergänzt mit 10 mM Magnesiumchlorid, gewaschen. ExM-kompatible Nanolineal-Stammlösungen wurden im Verhältnis 1:10 in PBS verdünnt, mit 10 mM Magnesiumchlorid ergänzt und dann auf mit BSA-Biotin/NeutrAvidin beschichtete Glasobjektträger aufgetragen, 30 Minuten lang bei Raumtemperatur inkubiert und anschließend dreimal gewaschen Schritte mit 1,000 μl PBS ergänzt mit 10 mM Magnesiumchlorid. Die Objektträger wurden in PBS, ergänzt mit 10 mM Magnesiumchlorid, für die Bildgebung vor der Expansion montiert.
Nach der Bildaufnahme vor der Erweiterung wurden die Deckgläser entfernt. In Analogie zum oben beschriebenen Protokoll zur Gewebeexpansion wurden die Nanolineale in die ExM-Gelierlösung eingebettet und 4 Minuten lang bei 30 °C inkubiert. Anschließend wurden Gelierkammern gebaut, wonach der Gelierschritt durch Inkubation in einem befeuchteten Ofen durchgeführt wurde bei 37 °C für 2 h. Nach Abschluss der Gelierung wurden die Gelierkammern entfernt und als Verdauungsschritt wurden die Nanolineale denaturiert, um eine anschließende Expansion durch Inkubation in einer 50 %igen Formamidlösung (Sigma-Aldrich F9037) für 2 Stunden bei Raumtemperatur und anschließende Inkubation bei 4 °C zu ermöglichen C für 12 h. Die denaturierten Nanolineale wurden dann 60 Minuten lang bei Raumtemperatur in doppelt entionisiertes Wasser gelegt, um eine isotrope Expansion zu ermöglichen. Nach der Expansion wurden die Proben aus dem doppelt entionisierten Wasser entnommen und für die Bildgebung nach der Expansion in Kammerobjektträger mit Glasboden (Ibidi µ-Slide-Glasboden mit zwei Vertiefungen; Katalog-Nr. 80287) montiert.
Abbildung von Nanolinealen
Die LED-basierte WF-Bildgebung von Nanolinealen vor und nach der Expansion wurde mit dem THUNDER Imager 3D Live Cell und 3D Cell Culture (Leica Microsystems) durchgeführt, der mit einem ×100-Objektiv (numerische Apertur (NA) 1.47) ausgestattet war. LED-Intensität und Belichtungszeiten für jede Bedingung wurden systematisch optimiert. Um die anschließende SRRF-Verarbeitung vor und nach der Erweiterung zu ermöglichen, wurden zeitgestapelte Bilder (wobei jeder Zeitstapel aus 50 Bildern bestand) erhalten. Die konfokale Bildgebung der Nanolineale vor und nach der Expansion wurde mit dem konfokalen Zeiss LSM 800-Mikroskop mit AiryScan unter Verwendung des optimierten ×63-Objektivs (NA, 1.4) bei 12-fachem Digitalzoom und anschließender AiryScan-Verarbeitung mit dem ZEN2.6 (blau) durchgeführt Edition)-Software.
Bewertung der Nanolineal-PSF-Trennung
Um die Trennung des Nanolineal-PSF nach der Bildaufnahme zu bewerten, wurden zeitlich gestapelte Bilddateien aller Gruppen (120–25 nm, vor und nach der Expansion) zunächst pseudonymisiert, um sie einer weiteren unvoreingenommenen quantitativen Analyse durch einen unabhängigen Beobachter ohne Beteiligung an der Probe zu unterziehen Vorbereitung und Bildaufnahme. Aus diesen Zeitstapeln wurden 16–20 Regionen, die ein Nanolineal abdeckten, auf der Grundlage der Rohbilddaten zufällig pro Gruppe ausgewählt, wonach die SRRF-Verarbeitung durchgeführt wurde. Anschließend wurden sowohl Roh- als auch SRRF-verarbeitete Bilder überwachten Histogrammanpassungen unterzogen, um die Nanolineal-PSF-Trennung zu bestimmen, die als zwei Fluoreszenzmaxima definiert wurde, die deutlich durch mindestens ein Pixel ohne Signal getrennt waren.
Bewertung des Expansionsfaktors und Berichterstattung
Um den Expansionsfaktor zu bewerten, wurden die Abstände zwischen den beiden Fluoreszenzsonden der Nanolineale mit dem Plotprofil-Tool ImageJ2 Version 2.3.0/1.53q gemessen. Eine zentral durch beide Fluorophore verlaufende Linie wurde gezeichnet und das Profil der Pixelintensität entlang dieser Linie erstellt. Anschließend wurde der Abstand zwischen den beiden Intensitätsmaxima, die die Zentren der Fluorophore darstellen, berechnet. Wie in einem früheren Bericht6 Neben einer gründlichen Validierung des Expansionsfaktors auf der Nanoskala (unter Verwendung von Nanolinealen) wurden für alle ExSRRF-Bilder korrelative Bilder der interessierenden Region (ROI) vor und nach der Expansion erhalten, um die Abstände nach der Expansion zum Vorfeld zu referenzieren -Expansion biologischer Distanzen, was die Stabilität des Expansionsfaktors im Mikrometerbereich bestätigt.
Bildgebung von Geweben vor und nach der Expansion
Die LED-basierte WF-Bildgebung von Geweben vor und nach der Expansion wurde mit dem THUNDER Imager 3D Live Cell und 3D Cell Culture (Leica Microsystems) durchgeführt. Mit einem 20-fachen Objektiv (NA, 0.40) wurden Gesamtgewebeübersichten vor und nach der Expansion bei geringer Vergrößerung durchgeführt. Bilder mit hoher Vergrößerung vor und nach der Erweiterung wurden mit mehreren Objektiven erhalten, darunter einem 40-fachen Objektiv (NA, 1.10), einem 63-fachen Objektiv (NA, 1.10) und einem 100-fachen Objektiv (NA, 1.47), nachdem die LED-Intensität optimiert wurde Belichtungszeiten. Um die SRRF-Verarbeitung nach der Erweiterung zu ermöglichen, wurden für jeden ROI Zeitstapel (jeweils bestehend aus 20 bis 200 Bildern, abhängig von den experimentellen Anforderungen) erstellt.
Zeitbasierte Bildregistrierung und Bewegungskorrektur
Um mögliche Bewegungen während der Bildgebung zu korrigieren, wurden Bilder innerhalb jedes Zeitstapels zunächst mit scikit-image in Python 3 registriert43 (https://scikit-image.org/) und Bildregistrierungsbibliotheken (https://image-registration.readthedocs.io/en/latest/). Jedes Bild im Stapel wurde mithilfe eines Referenzkanals, der unsere interessierende Hauptstruktur enthielt, separat am ersten Bild im Zeitstapel ausgerichtet. In jedem Bild des Referenzkanals wurden die Strukturen zunächst mit einem Gaußfilter mit einer Standardabweichung von 1 geglättet. Anschließend wurden die unteren 90 Perzentile der Pixelwerte auf 0 gesetzt, wobei nur die oberen 10 Perzentile der Pixelwerte beibehalten wurden. Anschließend wurde das Histogramm jedes Bildes im Zeitstapel angepasst, um es an das Referenzhistogramm anzupassen. Schließlich wurde die Verschiebung zwischen den beiden Bildern mit der Funktion chi ermittelt2 Verschiebung aus der Bildregistrierungsbibliothek, die die Upsampling-Methode der diskreten Fourier-Transformation verwendet. Diese Verschiebung wurde schließlich aus allen Kanälen des Bildes entfernt, die zugeschnitten und aufgefüllt wurden, um die ursprüngliche Größe beizubehalten, und dann in einem Bildstapel wiederhergestellt wurden.
SRRF und NanoJ-SQUIRREL
Die SRRF-Verarbeitung der Rohdaten wurde mit der Fiji-Bildgebungssoftware Version 2.3.0/1.53q (Max-Planck-Institut für molekulare Zellbiologie und Genetik) in Kombination mit dem NanoJ-SRRF-Plug-in durchgeführt.
Für die Nanolineal-SRRF-Verarbeitung vor und nach der Erweiterung wurden zeitgestapelte Rohdateien mit den folgenden SRRF-Einstellungen verarbeitet. Ringradius: 0.5; Radialitätsvergrößerung: 10; Äxte im Ring; 8; zeitliche Analyse; zeitliche Radialität, durchschnittliche Radialität; Positivitätsbeschränkung „deaktiviert“ entfernen; „deaktiviert“ renormalisieren; Farbverlaufsglättung „deaktiviert“; Gewichtung, Intensitätsgewichtung „aktiv“ durchführen; Gradientengewichtung „deaktivieren“; Korrekturen, SRRF-Musterung minimieren „aktiv“; Schnelle Linearisierung SRRF „deaktiviert“.
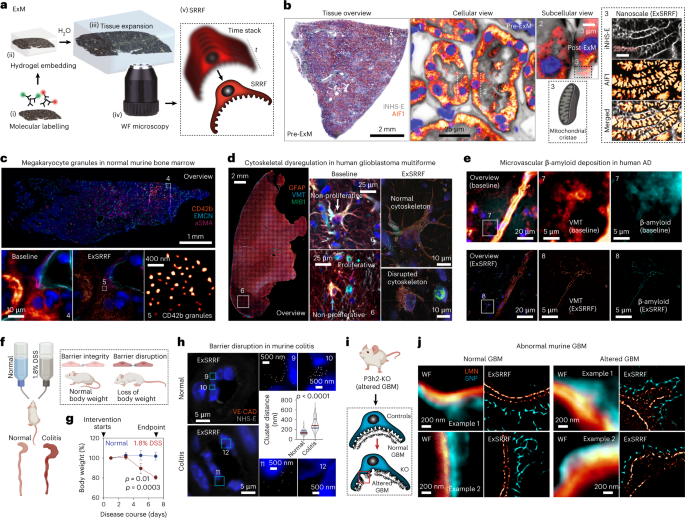
Für alle anderen gewebebasierten Bilder wurden zeitgestapelte Rohdateien oder histogrammbereinigte Dateien mit den folgenden Einstellungen verarbeitet. Ringradius, 0.5–2.0; Radialitätsvergrößerung 3–10 (abhängig von der gewünschten Vergrößerung); Achsen im Ring, 2–8 (je nach gewünschter Vergrößerung); zeitliche Analyse; zeitliche Radialität, durchschnittliche Radialität; Positivitätsbeschränkung „deaktiviert“ entfernen; „deaktiviert“ renormalisieren; Gradientenglättung „aktiv“ machen; Gewichtung, Intensitätsgewichtung „aktiv“ durchführen; Gradientengewichtung „deaktivieren“; Korrekturen, SRRF-Musterung minimieren „aktiv“; Schnelle Linearisierung SRRF „deaktiviert“. Für die Verarbeitung des invertierten NHS-Ester-Kanals (Abb. 1b) wurde das NHS-Ester-Signal zunächst mit der Funktion „Invertieren“ in Fidschi invertiert, woraufhin die SRRF-Verarbeitung durchgeführt wurde (wie oben beschrieben). Zur Bewertung der Qualitätsverbesserung durch den Bildregistrierungsprozess wurde der hochauflösende Algorithmus zur quantitativen Bildbewertung und Meldung von Fehlerorten (SQUIRREL) verwendet. Entsprechende ROIs wurden sowohl in Rohdatensätzen als auch in registrierten Datensätzen ausgewählt. Nach der Verarbeitung mit dem SRRF-Algorithmus wurden die erhaltenen hochauflösenden Bilder mithilfe des SQUIRREL-Algorithmus mit dem ersten Bild jedes zugehörigen Stapels verglichen. Die generierten Fehlerkarten wurden verwendet, um Bereiche mit hoher Diskrepanz visuell hervorzuheben, während auflösungsskalierte Pearson-Koeffizienten für den quantitativen Vergleich zwischen Roh- und registrierten Datensätzen verwendet wurden.
Anpassen der Bildausrichtung zur Figurenvorbereitung
Bilder vor und nach der Erweiterung (Rohbilder und SRRF-verarbeitete Bilder) wurden mit Fidschi gedreht, um eine ähnliche Ausrichtung der Strukturen im zu erhalten X und Y Achsen. Dieser Ansatz erzeugte keine visuellen Artefakte, obwohl diskrete Rotationsartefakte an den Bildrändern in Bereichen ohne das echte Signal nicht in allen Fällen ausgeschlossen werden können.
Quantifizierung der FP- und SD-Breite
Um die SD-Breite in mit Nephrin gefärbten menschlichen Nierenbiopsien zu messen, wurden die ExSRRF-Bilder zunächst einer automatischen Schwellenwertermittlung unter Verwendung des ImageJ-Schwellenwerttools in Kombination mit dem Standardalgorithmus und einer automatischen Anpassung unterzogen. Die SD-Breite wurde dann mit dem ImageJ-Plotprofiltool gemessen. Eine in einem 90°-Winkel durch die Schwellenwert-SD verlaufende Linie wurde an mehreren zufälligen Positionen entlang der SD gezeichnet, gefolgt von einer Diagrammprofilanalyse der Signalbreite. Um die FP-Breite in menschlichen Nierenbiopsien zu messen, wurden ExSRRF-Bilder von Nephrin-gefärbten menschlichen Nierenbiopsieproben zunächst einer schrittweisen ImageJ-basierten Verarbeitung zur indirekten morphologischen Identifizierung und Segmentierung von FPs unterzogen. Zunächst wurde eine Schwellenwertbildung unter Verwendung des Standardalgorithmus im automatischen Anpassungsmodus durchgeführt, gefolgt von einer Bildinvertierung und einer Wassereinzugsgebietssegmentierung, auf deren Grundlage eine weitere überwachte Segmentierung durchgeführt wurde, die zur Identifizierung von durch die SD getrennten FPs führte. Die FP-Breite wurde dann mit dem ImageJ-Plotprofil-Tool gemessen, indem an mehreren zufälligen Positionen eine Linie in einem 90°-Winkel durch den FP gezogen wurde, gefolgt von einer Plotprofilanalyse der Signalbreite.
Automatisierte Quantifizierung der SD-Dichte und -Dilatation
Um die SD-Dichte zu quantifizieren, wurde in Python 3 unter Verwendung der scikit-image-Bibliothek ein mehrstufiger Prozess entwickelt43. Zunächst wurde der ROI extrahiert, in dem die interessierenden Strukturen vorhanden sind. Anschließend wurden die interessierenden Strukturen mithilfe der Graterkennung und Nachbearbeitung extrahiert. Abschließend wurde die Dichte dieser Strukturen innerhalb des extrahierten ROI berechnet. Die Schritte und Parameter in diesem Prozess wurden auf zwei Bildern der IgAN-Proben und einem Bild der MCD-Proben optimiert und erst dann auf alle anderen Bilder ausgeweitet. Die Ergebnisse wurden zunächst visuell ausgewertet, bevor die quantitativen Dichten überprüft wurden.
Um den ROI zu extrahieren, wurde das Bild zunächst auf 25 % seiner Originalgröße heruntergerechnet. Das Bild wurde dann einem Schwellenwert unterzogen, um geringes Rauschen zu entfernen, und mithilfe eines Gaußschen Filters mit einer Standardabweichung von 8 geglättet, gefolgt von einer Otsu-Schwellenwertbildung. Als nächstes wurde die mathematische Morphologie (binäres Füllen von Löchern und binäres Schließen) angewendet. Schließlich wurden alle verbundenen Bereiche extrahiert und nur diejenigen beibehalten, die größer als ein bestimmter Schwellenwert (5,000 Pixel) waren. Die resultierenden ROIs wurden erneut auf die ursprüngliche Bildgröße hochgesampelt.
Die SD-Segmentierung wurde mit Hilfe der Graterkennung mit dem Meijering Ridge Detector durchgeführt44. Die resultierenden Grate wurden mit einem Schwellenwert versehen, um nur Werte größer als 0.2 beizubehalten, und es wurde eine mathematische Morphologie (Öffnung) angewendet. Die SD-Dichten wurden schließlich als Verhältnis der der SD zugeordneten Pixel innerhalb des ROI ermittelt. Darüber hinaus wurde die SD-Dilatation auf ähnliche Weise wie die Trabekeldicke und der Trabekelabstand berechnet45, ein häufig verwendetes Plug-in für die Knochendichteanalyse. Der lokale Abstand an einem Pixel des Bildes ist der Durchmesser des größten Kreises, der in den Raum zwischen den Graten passt, Teil des ROI ist und den Punkt enthält. Das implementierte ImageJ-Makro berechnete den Mittelwert, den Median, die Standardabweichung und den Flächenanteil des Kammabstands. Für diese Studie haben wir den Median pro Bild verwendet.
Automatisierte Quantifizierung von ER-Stress
Um den durch IRI verursachten Schaden zu quantifizieren, wurde in Python 3 unter Verwendung der scikit-image-Bibliothek ein mehrstufiger Prozess entwickelt, der der Berechnung der SD-Dichte und -Dilatation ähnelt43. Zunächst wurde der ROI extrahiert, in dem die interessierenden Strukturen vorhanden sind. Anschließend wurden die interessierenden Strukturen mithilfe der Graterkennung und Nachbearbeitung extrahiert. Abschließend wurde die Dichte dieser Strukturen innerhalb des extrahierten ROI berechnet. Die Schritte und Parameter in diesem Prozess wurden aus der Berechnung der SD-Dichte und -Dilatation angepasst und für ein Bild der Kontrollproben und ein Bild der IRI-Proben optimiert und erst dann auf alle anderen Bilder ausgeweitet. Die Ergebnisse wurden zunächst visuell ausgewertet, bevor die quantitativen Dichten überprüft wurden.
Um den ROI zu extrahieren, wurde das Bild zunächst auf 25 % seiner Originalgröße heruntergerechnet. Das Bild wurde mit einem Gauß-Filter mit einer Standardabweichung von 8 und einem Gauß-Filter mit einer Standardabweichung von 10 geglättet, gefolgt von Otsu-Schwellenwertbildung. Als nächstes wurde die mathematische Morphologie (binäres Füllen von Löchern) angewendet. Schließlich wurden alle verbundenen Bereiche extrahiert und nur diejenigen beibehalten, die größer als ein bestimmter Schwellenwert (5,000 Pixel) waren. Die resultierenden ROIs wurden erneut auf die ursprüngliche Bildgröße hochgesampelt.
Die Segmentierung Calreticulin-basierter ER-Netzwerke wurde mithilfe der Ridge-Detektion mit dem Meijering-Ridge-Detektor durchgeführt44. Die resultierenden Grate wurden mit Schwellenwerten versehen, um nur Werte über 0.25 beizubehalten. Kleine Objekte mit einer Größe von weniger als 125 Pixeln wurden entfernt und eine mathematische Morphologie (Öffnung) angewendet. Die ER-Dichten wurden schließlich als Verhältnis der dem ER zugeordneten Pixel innerhalb des ROI ermittelt. Darüber hinaus wurde die ER-Dilatation auf ähnliche Weise wie die Trabekeldicke und der Trabekelabstand berechnet45, ein häufig verwendetes Plug-in für die Knochendichteanalyse. Der lokale Abstand an einem Pixel des Bildes ist der Durchmesser des größten Kreises, der in den Raum zwischen den Graten passt, Teil des ROI ist und den Punkt enthält. Das implementierte ImageJ-Makro berechnete den Mittelwert, den Median, die Standardabweichung und den Flächenanteil des Kammabstands.
Auswertung von Driftkorrekturen
Die Registrierungen von Zeitstapeln wurden unter Berücksichtigung des Offsets ausgewertet, um den die Frames während des Registrierungsprozesses verschoben werden mussten. Für jeden Frame im Zeitstapel wird der Offset-Abstand (2-Norm) des x und y Offsets wurden mithilfe der linearen Algebra-Funktion in der NumPy-Bibliothek berechnet (https://numpy.org/) unter Verwendung von Python 3. Diese zeitlichen Versätze wurden im mittleren Versatz und im letzten Versatz zusammengefasst und beziehen sich auf den Versatz des letzten Frames, normalerweise den größten Versatz in einem Zeitstapel. Für jeden Zeitpunkt wurden das mittlere Strukturähnlichkeitsindexmaß (MSSIM) und der mittlere quadratische Fehler (MSE) mithilfe der Scikit-Image-Bibliothek berechnet43. Diese Metriken wurden sowohl für Originalbilder als auch für registrierte Bilder in Bezug auf das erste Bild (Referenzbild für die Registrierungen) berechnet, wobei nur die überlappenden Bereiche des Bildes berücksichtigt wurden, um eine Vergleichbarkeit zu ermöglichen. Sie wurden in den mittleren und letzten MSSIMs sowie den mittleren und letzten MSSEs vor und nach der Registrierung für jeden Zeitstapel zusammengefasst. Die Werte nach der Registrierung wurden von denen vor der Registrierung abgezogen, um die Auswirkung der Registrierung zu messen. Bei ähnlicheren Strukturen ist der MSSIM größer, was bedeutet, dass eine negative Änderung auf eine Verbesserung durch Registrierung hinweist, wohingegen der MSE bei ähnlicheren Bildern kleiner ist; Somit deutet eine positive Veränderung auf eine Verbesserung hin.
Eine Standardabweichung (s.d.) im Offset (basierend auf 0.5 × s.d. vom Mittelwert) wurde als bestimmender Faktor verwendet, um die Zeitstapel in zwei Gruppen aufzuteilen: geringe Drift (die überwiegende Mehrheit) und solche mit mehr erforderlicher Registrierung mit Offsets größer als 0.5 × s.d. wurden als hohe Drift definiert. Anschließend wurden die beiden Gruppen hinsichtlich der bei der Registrierung erzielten Verbesserung verglichen. Alle Codes wurden in Python 3 implementiert.
Auswertung der Auflösungsquantifizierung zur zuverlässigen Segmentierung
Um die Schärfe und Eignung der Bilder für die weitere Analyse der Strukturen zu bewerten, wurden die rohen ExM-, ExSRRF- und STED-Bilder mit den auf jedem Bild erkannten anfänglichen Graten unter Verwendung des Strukturähnlichkeitsindexmaßes verglichen. Ein Strukturähnlichkeitsindexmaß näher bei 1 zeigte eine bessere strukturelle Ähnlichkeit zwischen den Bildern und Graten an, was darauf hindeutet, dass eine bessere Übereinstimmung zwischen den berechneten Graten und Strukturen aus den Rohbildern besteht.
Transmissionselektronenmikroskopie
Mäusenierengewebe wurde kurz mit 4.0 % PFA und 2.5 % Glutaraldehyd in 0.1 M Cacodylatpuffer (pH 7.4) in situ bei Raumtemperatur fixiert und dann präpariert, entnommen und in Stücke von 1 mm geschnitten3 und 48 h lang in der gleichen Lösung bei 4 °C fixiert. Die Gewebeblöcke wurden mit 1 % OsO kontrastiert4 (Roth 7436.1) bei Raumtemperatur für 1 h und 1 % Uranylacetat (Polysciences 21447-25) in 70 % Ethanol bei Raumtemperatur für 1 h. Nach der Dehydrierung wurden Gewebeblöcke in Epoxidharz (Durcopan ACM, Sigma-Aldrich 44611) eingebettet und mit einem Leica EM UC50 Ultramikrotom (Leica Microsystems) ultradünne Schnitte mit einer Dicke von 6 nm geschnitten. Die Schnitte wurden mit einem Transmissionselektronenmikroskop Zeiss 910 abgebildet und mit der ITEM-Software Version 5.2 (Build 4768) analysiert.
Menschliche Nierenbiopsien wurden gemäß Standardarbeitsanweisungen während der diagnostischen Aufarbeitung präpariert und zusammen mit Saccharose für 4 Minuten bei 10 °C von 80 % Formaldehyd in einen Cacodylatpuffer überführt. Als nächstes OsO4 wurde 2 Stunden lang aufgetragen, gefolgt von zweimaligem Waschen in Cacodylatpuffer plus Saccharose für 5 Minuten. Anschließend wurde die Probe 1 Stunde lang mit Uranylacetat kontrastiert. Die Probe wurde dann für jeweils 5 Minuten in Ethanolbäder mit steigenden Ethanolkonzentrationen gegeben, gefolgt von Methyl-tert-Butylether zweimal für jeweils 5 min, Methyl-tert-Butylether plus Epoxidmischung (in 1:3 Verdünnung). Anschließend wurden die Proben 60 Stunden lang bei 48 °C und anschließend 100 Stunden lang bei 11.5 °C in eine Epoxidmischung eingebettet. Halbdünne und ultradünne Schnitte wurden auf einem Reichert Jung Ultracut E701704-Mikrotom geschnitten. Die Gitter wurden von Polyscience gekauft. Die Gitter wurden dann mit EM-Instrumenten (EM 109 und EM 902, Zeiss) analysiert, die mit digitalen EM-Kameras (Tröndle) ausgestattet waren. Von jedem Fall wurde ein Glomerulus analysiert.
STED-Mikroskopie
Die Fluoreszenzmarkierung der STED-Proben wurde wie oben beschrieben durchgeführt. Die Bilder wurden mit einem Abberior Instruments FACILITY LINE-Mikroskop aufgenommen, das mit einem inversen IX83-Mikroskop (Olympus), einem ×60-Ölobjektiv (UPlanXApo ×60/1.42-Öl, Olympus) ausgestattet war, unter Verwendung gepulster Anregungslaser bei 488, 561 und 640 nm und a gepulster STED-Laser mit 775 nm sowie ein vierkanaliges easy3D-STED-Instrument der Abberior Expert Line mit einem 775 nm-Verarmungsstrahl (Abberior Instruments), einem ×60-Ölobjektiv (Nikon ×60/1.4) und einem QUAD-Strahlscanner unter Verwendung eines gepulsten 640 -nm-Diodenstrahls, abgereichert mit dem 775 -nm-STED-Strahl und detektiert mit einer Lawinenfotodiode mit einem vorderen 685 ± 70 -nm-Bandpassfilter. Alle Erfassungsvorgänge wurden von der Lightbox-Software Version 16.3.16118 gesteuert. Schließlich wurde die Dekonvolutionstechnik (Richardson-Lucy) verwendet, um die Bildqualität zu verbessern.
3D-gedruckte Bildgebungskammer
NEXTERION-Deckgläschen (Größe 110.000 × 74.000 ± 0.200 mm; Dicke 0.175 ± 0.020 mm; SCHOTT) wurden für die Montage expandierter Gewebe verwendet, die zu groß waren, um in die Ibidi µ-Slide-Kammern mit zwei Vertiefungen und Glasboden zu passen. Eine maßgeschneiderte Montagelösung, einschließlich eines Rahmens, eines elastischen Kissens und eines Deckels für den Rahmen, wurde mit einem 3D-Drucker gedruckt, um die NEXTERION-Deckgläser zu tragen und die Montage im THUNDER Imager 3D Live Cell und 3D Cell Culture (Leica Microsystems) zu ermöglichen.
Der Rahmen trägt das NEXTERION-Deckglas und ermöglicht das Einsetzen in den THUNDER Imager 3D Live Cell und 3D Cell Culture (Leica Microsystems). Das elastische Kissen wird zwischen NEXTERION-Deckglas und Deckel platziert und verhindert, dass das Deckglas zerbricht, wenn es durch den Deckel fixiert wird. Der Deckel für den Rahmen stabilisiert das NEXTERION-Deckglas am Rahmen. Das NEXTERION-Deckglas und das Kissen werden vollständig am Rahmen befestigt, indem diese Keile in Kerben im Rahmen eingesetzt werden. Tinkercad (Autodesk; https://www.tinkercad.com) wurde verwendet, um Designs für alle 3D-gedruckten Teile zu erstellen.
Alle 3D-gedruckten Teile und Konstruktionsmerkmale sind in den erweiterten Datenabbildungen dargestellt. 2 und 3. Der Rahmen und der Deckel wurden mit PolyLite PLA-Filament 1.75 mm (Polymaker) bedruckt. Das Kissen wurde mit NinjaFlex TPU-Filament 1.75 mm (NinjaTek) bedruckt. Für den 5D-Druck wurde Ender-3 Plus (Creality) verwendet. Die in Ultimaker Cura (v. 4.13.1; Ultimaker) verwendeten Einstellungen sind wie folgt. Düsengröße: 0.40 mm; Schichthöhe: 0.16 mm (PLA) und 0.20 mm (TPU); Wandstärke: 1.20 mm (PLA) und 0.80 mm (TPU); Dicke oben/unten: 1.20 mm (PLA) und 0.80 mm (TPU); Düsentemperatur: 220 °C (PLA) und 235 °C (TPU); Betttemperatur: 50 °C; Lüftergeschwindigkeit, 100 %; Druckgeschwindigkeit: 50 mm s-1 (PLA) und 20 mm s-1 (TPU); Druckgeschwindigkeit der ersten Schicht: 25 mm s-1 (PLA) und 10 mm s-1 (TPU); Infil, 10 % und Zickzack; Haftung auf der Bauplatte, keine. Um eine Klebefläche auf dem Bett zu schaffen, wurden Abdeckbänder verwendet.
Statistische Analysen
Alle statistischen Analysen wurden mit GraphPad Prism (Version 9.3.1) durchgeführt. Violindiagramme geben den Medianwert und den Interquartilbereich an. Die Signifikanz wurde anhand der ungepaarten Werte bewertet t-Tests mit Welch-Korrektur zum Vergleich zweier kontinuierlicher Variablen; ein gepaart t-Test auf Vorher/Nachher-Einstellungen; und die Brown-Forsythe-, Welch-ANOVA- und Dunnett-Tests beim Vergleich von drei kontinuierlichen Variablen. Die Betriebskennlinien des Empfängers wurden mit der Wilson/Brown-Methode erstellt (95 %-Konfidenzintervall; Ergebnisse in Prozent ausgedrückt). A p Ein Wert unter 0.05 gilt als statistisch signifikant.
- SEO-gestützte Content- und PR-Distribution. Holen Sie sich noch heute Verstärkung.
- Platoblockkette. Web3-Metaverse-Intelligenz. Wissen verstärkt. Hier zugreifen.
- Quelle: https://www.nature.com/articles/s41565-023-01328-z
- :Ist
- ][P
- $UP
- 000
- 1
- 1.3
- 10
- 100
- 11
- 110
- 2%
- 2012
- 2014
- 2017
- 39
- 3d
- 3D Printing
- 7
- 70
- 8
- 9
- 95%
- a
- oben
- Zugang
- Nach
- Konto
- erreicht
- ACM
- Erwerb
- Ad
- angepasst
- hinzugefügt
- Zusatz
- Bereinigt
- Anpassungen
- advanced
- Nach der
- AL
- Alexa
- Algorithmus
- ausgerichtet
- Alle
- Zulassen
- Obwohl
- Verstärkung
- Analyse
- Moderator
- und
- Tier
- Tiere
- Ein anderer
- Antikörper
- Anwendung
- angewandt
- Anwendung
- Ansatz
- angemessen
- Genehmigung
- genehmigt
- SIND
- Bereich
- Bereiche
- um
- AS
- Bewertung
- damit verbundenen
- At
- autodesk
- Automatisiert
- Lawine
- durchschnittlich
- ACHSEN
- Zurück
- basierend
- BE
- Strahl
- Bevor
- Sein
- unten
- Besser
- zwischen
- Bindung
- Biologie
- Biotechnologie
- KLINGE
- Blockiert
- Blau
- Tafel
- KNOCHEN
- Boden
- Bruch
- kurz
- BSA
- puffern
- bauen
- by
- berechnet
- Kameras
- Krebs
- kann keine
- vorsichtig
- tragen
- Häuser
- Fälle
- verursacht
- Center
- sicher
- Labor-Klimakammer
- Übernehmen
- Kanal
- Kanäle
- Merkmal
- Überprüfung
- Kreis
- Klemme
- klassisch
- klicken Sie auf
- Klinische
- geschlossen
- näher
- Schließen
- Codes
- Zusammenarbeit
- Produktauswahl
- COM
- Kombination
- Ausschuss
- häufig
- COMP
- verglichen
- Vergleich
- Vergleich
- abschließen
- Abschluss
- Konzentration
- Zustand
- Bedingungen
- Vertrauen
- Sie
- betrachtet
- Bestehend
- Baugewerbe
- enthält
- kontinuierlich
- Smartgeräte App
- gesteuert
- Steuerung
- Korrekturen
- Dazugehörigen
- KOVALENT
- Abdeckung
- Abdeckung
- erstellen
- Kultur
- Original
- Kundenspezifische
- Schneiden
- DA
- Unterricht
- technische Daten
- Datensätze
- Tage
- Standard
- definiert
- Dichte
- Abteilung
- Abhängig
- darstellend
- beschrieben
- Design
- Designs
- erkannt
- Entdeckung
- Bestimmen
- Festlegung
- entwickelt
- Entwicklung
- Entwicklungsstörungen
- Abweichung
- DID
- digital
- Verdünnung
- Direkt
- Diskrepanz
- Abstand
- Division
- Frau
- nach unten
- Zeichnung
- gezogen
- Drops
- im
- e
- jeder
- Ausgabe
- entweder
- eingebettet
- ermöglichen
- Endpunkt
- verbesserte
- ausgestattet
- Fehler
- Äther (ETH)
- ethisch
- Ethik
- bewerten
- Bewerten
- ausgeschlossen
- ergänzt
- Expansion
- Experiment
- Experte
- ausgesetzt
- Belichtung
- zum Ausdruck gebracht
- Extrakt
- Einrichtung
- Fan
- Fashion
- FAST
- Eigenschaften
- Fed
- Feige
- Abbildung
- Mappen
- gefüllt
- Filter
- Finale
- Endlich
- Ende
- Vorname
- passen
- fixiert
- Schwankungen
- gefolgt
- Folgende
- folgt
- Nahrung,
- Aussichten für
- Formaldehyd
- fps
- Fraktion
- FRAME
- Frei
- für
- Materials des
- voll
- Funktion
- weiter
- erzeugen
- erzeugt
- Generation
- Genetik
- Glas
- Gold
- größte
- Gruppe an
- Gruppen
- Richtlinien
- Pflege
- Haben
- Höhe
- Hilfe
- GUTE
- Hervorheben
- Bohrungen
- Krankenhaus
- HTTPS
- human
- Login
- Image
- Bilder
- Imaging
- eingetaucht
- Impact der HXNUMXO Observatorien
- umgesetzt
- zu unterstützen,
- Verbesserung
- in
- Einschließlich
- inkubiert
- Inkubation
- unabhängig
- Index
- angegeben
- zeigt
- Individuell
- Anfangs-
- Institut
- Institutionell
- Instrument
- Instrumente
- Interesse
- Intervention
- Inversion
- Beteiligung
- IT
- SEINE
- Aufbewahrung
- Niere
- Nieren
- Ausrüstung
- Kennzeichnung
- grosse
- größer
- höchste
- laser
- -Laser
- Nachname
- Schicht
- geführt
- Gesetzgebung
- Bibliotheken
- Bibliothek
- Line
- LINK
- leben
- aus einer regionalen
- Standorte
- verschlossen
- langfristig
- Sneaker
- Makro
- Main
- Wartung
- Mehrheit
- Landkarten
- Spiel
- mathematisch
- Matrix
- max
- Mittel
- messen
- Medien
- sowie medizinische
- Medizin
- Methode
- Metrik
- Mäuse
- Mikroskop
- Mikroskopie
- minimieren
- Mischung
- Model
- Modell
- MOL
- Molekular-
- überwacht
- mehr
- Bewegung
- mRNA
- mehrere
- Natur
- erforderlich
- Negativ
- Niederlande
- Netzwerke
- Neu
- weiter
- NIH
- Lärm
- normal
- Roman
- numpig
- Ziel
- Objekte
- erhalten
- erhalten
- of
- Offset
- ÖL
- Olymp
- on
- EINEM
- geöffnet
- Eröffnung
- die
- Einkauf & Prozesse
- optisch
- optimiert
- Optimierung
- Original
- Andere
- über Nacht
- Überblick
- Unterlage
- gepaart
- Parameter
- Teil
- Teile
- Pathologie
- Patienten
- PBS
- Pearson
- Prozent
- Stücke
- Pixel
- Ort
- Plattform
- Plato
- Datenintelligenz von Plato
- PlatoData
- erfahren
- Points
- Polymer
- positioniert
- für einige Positionen
- positiv
- Positive Emotionen
- Potenzial
- genau
- Gegenwart
- verhindern
- Verhütung
- früher
- vorher
- primär
- Grundsätze
- Sonde
- Verfahren
- Prozessdefinierung
- Verarbeitung
- Profil
- Profiling
- ProGen
- Eigentums-
- Proteine
- Proteine
- Protokoll
- Protokolle
- vorausgesetzt
- Publikationen
- gekauft
- setzen
- Python
- Qualität
- quantitativ
- F&E
- Hase
- zufällig
- Angebot
- RAT
- Wertung
- Verhältnis
- Roh
- Rohdaten
- Region
- Regionen
- eingetragen
- Registrierung
- Registratur
- zuverlässig
- entfernen
- Entfernt
- berichten
- Reporting
- falls angefordert
- Voraussetzungen:
- Harz
- Auflösung
- Umwelt und Kunden
- diejenigen
- was zu
- Die Ergebnisse
- behalten
- Überprüfen
- bewertet
- Ring
- Anstieg
- RNA
- ROI
- Zimmer
- s
- Salz
- gleich
- Santa
- Skalieren
- Wissenschaft
- SD
- Sekundär-
- Abschnitte
- Segmentierung
- ausgewählt
- getrennt
- Modellreihe
- Serum
- kompensieren
- Einstellung
- Einstellungen
- verschieben
- gezeigt
- Signal
- Bedeutung
- signifikant
- ähnlich
- Größe
- Slides
- klein
- kleinere
- SOFT
- Software
- Lösung
- Lösungen
- Raumfahrt
- spezifisch
- Geschwindigkeit
- gespalten
- Kariert
- Stabilität
- Stapel
- Stacks
- Standard
- Bundesstaat
- State Department
- angegeben
- statistisch
- Schritt
- Shritte
- -bestands-
- gestoppt
- Lagerung
- gelagert
- strukturell
- Struktur
- Studie
- Folge
- Anschließend
- Eignung
- Oberfläche
- Chirurgie
- Systeme und Techniken
- Einnahme
- Target
- Technologie
- AGB
- Tests
- zur Verbesserung der Gesundheitsgerechtigkeit
- Das
- Niederlande
- ihr
- Sie
- Diese
- Dritte
- nach drei
- dreidimensional
- Schwelle
- Durch
- Zeit
- mal
- Gewebe
- zu
- gemeinsam
- auch
- Werkzeug
- Werkzeuge
- Top
- Tracing
- übertragen
- Transformieren
- Behandlungen
- Triton
- was immer dies auch sein sollte.
- Twice
- für
- Universität
- gewöhnlich
- seit
- die
- Bestätigung
- Wert
- Werte
- Variablen
- riesig
- Version
- Pinnwand
- Wasser
- Wochen
- Gewicht
- Wohl
- GUT
- welche
- mit
- .
- ohne
- Arbeiten
- Zephyrnet
- Zhao
- Zoom