Mit ihren neugierigen Augen, der pelzigen Schnauze und dem üppigen Fell hockt die Maus – Spitzname Xiao Zhu oder Kleiner Bambus – flink auf einem Bambusstiel und nimmt eine hübsche Pose für die Kamera ein. Aber diese Maus existiert nicht in der Natur.
Xiao Zhu wird in einem Labor in Peking hergestellt und verschiebt die Grenzen dessen, was für Gentechnik und synthetische Biologie möglich ist. Anstatt die üblichen 20 Chromosomenpaare zu beherbergen, haben die Maus und ihre Geschwisterkohorten nur 19 Paare. Zwei Stücke unterschiedlicher Chromosomen wurden in einem gewagten Experiment künstlich miteinander verschmolzen, bei dem gefragt wurde: Anstatt einzelne DNA-Buchstaben oder mehrere Gene zu optimieren, können wir ein bestehendes genomisches Spielbuch komplett neu abstimmen und gleichzeitig riesige Blöcke genetischen Materials herummischen?
Es ist eine Moonshot-Idee. Wenn das Genom ein Buch ist, ist die Bearbeitung von Genen wie das Lektorat von Texten – hier und da werden Tippfehler geändert oder mehrere grammatikalische Fehler mit sorgfältig platzierten Anpassungen behoben.
Das Engineering auf Chromosomenebene ist eine ganz andere Sache: Es ist, als würde man mehrere Absätze neu anordnen oder ganze Abschnitte eines Artikels verschieben und gleichzeitig hoffen, dass die Änderungen Fähigkeiten hinzufügen, die an die nächste Generation weitergegeben werden können.
Das Leben neu zu programmieren ist nicht einfach. Xiao Zhus DNA-Aufbau besteht aus genetischen Buchstaben, die bereits durch Äonen des evolutionären Drucks optimiert wurden. Es ist keine Überraschung, dass das Herumbasteln an einem etablierten Genombuch oft zu einem Leben führt, das nicht lebensfähig ist. Bisher haben nur Hefen die Rejiggerung ihrer Chromosomen überstanden.
Das neue Studie, veröffentlicht in Wissenschaft, machte die Technologie für Mäuse möglich. Das Team fusionierte künstlich Stücke von Mäusechromosomen. Ein verschmolzenes Paar aus den Chromosomen vier und fünf war in der Lage, Embryonen zu tragen, die sich zu gesunden – wenn auch etwas seltsam verhaltenden – Mäusen entwickelten. Bemerkenswerterweise konnten sich die Mäuse trotz dieser tektonischen Verschiebung zu ihrer normalen Genetik reproduzieren und ihre gentechnisch veränderten Eigenschaften an eine zweite Generation von Nachkommen weitergeben.
„Zum ersten Mal weltweit haben wir eine vollständige chromosomale Umordnung bei Säugetieren erreicht und damit einen neuen Durchbruch in der synthetischen Biologie erzielt.“ sagte Studienautor Dr. Wei Li an der Chinesischen Akademie der Wissenschaften.
In gewisser Weise ahmt die Technik die Evolution in halsbrecherischer Geschwindigkeit nach. Basierend auf vorhandenen Daten zu Mutationsraten würde es im Allgemeinen Millionen von Jahren dauern, bis die hier vorgestellte Art des genetischen Austauschs auf natürliche Weise erreicht wird.
Das Studium ist nicht perfekt. Einige Gene in den gentechnisch veränderten Mäusen waren abnormal heruntergeregelt, was einem Muster ähnelt, das normalerweise bei Schizophrenie und Autismus zu beobachten ist. Und obwohl die Mäuse erwachsen wurden und gesunde Welpen züchten konnten, war die Geburtenrate weitaus niedriger als die ihrer nicht gentechnisch veränderten Artgenossen.
Trotzdem ist die Studie ein Kraftakt, sagte Evolutionsbiologe Dr. Harmit Malik vom Fred Hutchinson Cancer Center in Seattle, der nicht an der Studie beteiligt war. Wir haben jetzt dieses „schöne Toolkit“, um offene Fragen zu genomischen Veränderungen in größerem Maßstab anzugehen und möglicherweise Licht auf Chromosomenerkrankungen zu werfen.
Warten Sie, was sind noch einmal Chromosomen?
Die Arbeit greift auf das langjährige genetische Spielbuch der Evolution zum Aufbau neuer Arten zurück.
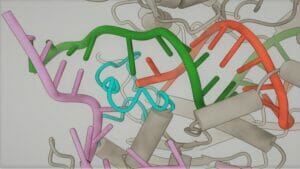
Lassen Sie uns zurückgehen. Unsere Gene sind in DNA-Doppelhelixketten codiert, die Bändern ähneln, die in der Zelle schweben. Es ist nicht platzsparend. Die Lösung der Natur besteht darin, jede Kette um eine Proteinspule zu wickeln, wie Schinkenscheiben, die über einem Mozzarella-Stick gedreht werden. Zusätzliche Drehungen packen diese Strukturen in winzige Pucks – Bildperlen an einer Schnur – die sich dann in Chromosomen wickeln. Unter dem Mikroskop sehen sie meist wie der Buchstabe X aus.
Jede Art trägt eine festgelegte Anzahl von Chromosomen. Menschliche Zellen – mit Ausnahme von Spermien und Eizellen – beherbergen alle 46 einzelne Chromosomen, die in 23 Paaren angeordnet sind und von jedem Elternteil geerbt werden. Labormäuse hingegen haben nur 20 Paare. Der vollständige Chromosomensatz wird als Karyotyp bezeichnet, abgeleitet vom griechischen Wort „Kern“ oder „Samen“.
Das Mischen und Anpassen von Chromosomen ist seit langem Teil der Evolution. Nach aktuellen Schätzungen akkumuliert ein Nagetier im Allgemeinen alle eine Million Jahre etwa 3.5 Chromosomenumlagerungen; einige Segmente werden gelöscht, andere dupliziert oder gemischt. Bei Primaten ist die Änderungsrate etwa halb so hoch. Das Verschieben von Chromosomenbrocken mag für jedes Tier drastisch erscheinen, aber wenn es möglich ist, ebnen die Veränderungen den Weg für die Entwicklung völlig anderer Arten. Unser Chromosom zwei zum Beispiel wurde aus zwei getrennten Chromosom verschmolzen, aber der Tweak ist beim Gorilla, unserem engen evolutionären Cousin, nicht vorhanden.
Die neue Studie zielte darauf ab, eins besser zu machen als die Evolution: Können wir mithilfe der Gentechnik Millionen von Jahren der Evolution auf nur wenige Monate verdichten? Es ist nicht nur aus wissenschaftlicher Neugier: Chromosomenerkrankungen liegen einigen unserer schwierigsten medizinischen Rätsel zugrunde, wie z. B. Leukämie im Kindesalter. Wissenschaftler haben zuvor mit Strahlung eine Chromosomenumlagerung ausgelöst, aber die Ergebnisse waren nicht leicht kontrollierbar, was es den Tieren unmöglich machte, neue Nachkommen zu gebären. Hier gingen Synthetische Biologen gezielter vor.
Der erste Schritt besteht darin, herauszufinden, warum Chromosomen großen Veränderungen in ihrer Organisation widerstehen. Wie sich herausstellt, ist ein großer Schluckauf beim Austauschen – oder Verschmelzen – von Chromosomenstücken eine biologische Eigenart namens Imprinting.
Wir erhalten Chromosomen von beiden Elternteilen, wobei jeder Satz ähnliche Gene enthält. Es ist jedoch nur ein Gerät eingeschaltet. Wie der Prozess des Prägens funktioniert, bleibt mysteriös, aber wir wissen, dass er die Fähigkeit der Kniescheiben embryonaler Zellen beeinträchtigt, sich zu mehreren Arten reifer Zellen zu entwickeln, und ihr Potenzial für die Gentechnik einschränkt.
Zurück in 2018, Dasselbe Team fand heraus, dass das Löschen von drei Genen das prägende biochemische Programm in Stammzellen außer Kraft setzen kann. Hier nutzten sie diese „freigeschalteten“ Stammzellen, um zwei Chromosomenpaare genetisch zusammenzufügen.
Als erstes richteten sie ihr Augenmerk auf die Chromosomen eins und zwei, die größten zwei in einem Mausgenom. Mithilfe von CRISPR schnitt das Team die Chromosomen auseinander, sodass sie genetische Brocken austauschen und sich wieder zu stabilen genetischen Konstrukten formen konnten. Zellen, die die Chromosomenveränderung enthielten, wurden dann in Eizellen – Eizellen – injiziert. Die resultierenden Embryonen wurden zur weiteren Reifung in weibliche Ersatzmäuse transplantiert.
Der Tausch war tödlich. Das künstliche Chromosom, mit Chromosom zwei gefolgt von Chromosom eins oder 2+1, tötete den sich entwickelnden Fötus nur 12 Tage nach der Empfängnis. Dieselben zwei Chromosomen, die in die entgegengesetzte Richtung, 1+2, verschmolzen waren, hatten mehr Glück und brachten lebende Welpen mit nur 19 Chromosomenpaaren hervor. Die Babymäuse waren ungewöhnlich groß für ihre Größe und wirkten in mehreren Tests ängstlicher als ihre normalen Artgenossen.
Besser lief es bei einem zweiten Chromosomenfusionsexperiment. Die Chromosomen 4 und 5 sind viel kleiner und der resultierende Embryo – 4+5 genannt – entwickelte sich zu gesunden Mauswelpen. Obwohl ihnen auch ein Chromosomenpaar fehlte, schienen sie überraschend normal zu sein: Sie waren nicht so ängstlich, hatten ein durchschnittliches Körpergewicht und brachten, wenn sie ausgewachsen waren, Welpen zur Welt, denen ebenfalls ein Chromosomenpaar fehlte.
Mit anderen Worten, das Team konstruierte einen neuen Karyotyp in einer Säugetierart, der über Generationen weitergegeben werden könnte.
Eine ganz neue Welt der Synthetischen Biologie?
Für Malik dreht sich alles um Größe. Durch die Überwindung des Prägungsproblems „ist die Welt ihre Auster, soweit es um Gentechnik geht“, sagte er sagte zu The Scientist.
Das nächste Ziel des Teams ist es, die Technologie einzusetzen, um schwierige Chromosomenerkrankungen zu lösen, anstatt mutierte Arten zu entwerfen. Die künstliche Evolution ist kaum um die Ecke. Aber die Studie zeigt die überraschende Anpassungsfähigkeit von Säugetiergenomen.
„Eines der Ziele der synthetischen Biologie ist es, komplexes vielzelliges Leben mit entworfenen DNA-Sequenzen zu erzeugen“, schreiben die Autoren. „Die Möglichkeit, DNA in großem Maßstab zu manipulieren, auch auf Chromosomenebene, ist ein wichtiger Schritt in Richtung dieses Ziels.“
Bildnachweis: Chinesische Akademie der Wissenschaften