Κλινική αξιολόγηση είναι η αξιολόγηση και ανάλυση των κλινικών δεδομένων ενός ιατροτεχνολογικού προϊόντος για την επαλήθευση της κλινικής ασφάλειας και της απόδοσής του. Η αξιολόγηση βασίζεται σε μια ολοκληρωμένη ανάλυση των κλινικών δεδομένων πριν και μετά τη διάθεση στην αγορά σχετικά με την προβλεπόμενη χρήση. Αυτό περιλαμβάνει δεδομένα ειδικά για τη συσκευή, καθώς και τυχόν δεδομένα που σχετίζονται με συσκευές που αξιώνονται ως ισοδύναμα από τον κατασκευαστή. Η όλη διαδικασία τεκμηριώνεται σε έκθεση κλινικής αξιολόγησης (CER).
Σε αυτήν την ανάρτηση, θα εξετάσουμε τις κύριες απαιτήσεις που σχετίζονται με την έκθεση κλινικής αξιολόγησης, λαμβάνοντας υπόψη δύο βασικούς διαφορετικούς κανονισμούς:
Επίσης, τέσσερα νέα έγγραφα προσθέτουν στην καθοδήγηση σχετικά με τη σύνοψη της ασφάλειας και των κλινικών επιδόσεων για κατασκευαστές και κοινοποιημένους οργανισμούς και επισημαίνουν τις διαφορές μεταξύ του MDR και του το MEDDEV 2.7/1(4):
Γενικές Πληροφορίες για την Κλινική Αξιολόγηση
Ο στόχος της κλινικής αξιολόγησης είναι η συλλογή και ανάλυση δεδομένων προκειμένου να επιβεβαιωθεί ότι για ένα συγκεκριμένο ιατροτεχνολογικό προϊόν υπάρχουν επαρκή στοιχεία για τη συμμόρφωση με τις βασικές απαιτήσεις για ασφάλεια και απόδοση.
Γενικά, αυτή η μεθοδολογική κλινική διερεύνηση πρέπει να εκτελείται μετά την IFU της συσκευής. σε εξαιρετικές περιπτώσεις όπου δεν απαιτείται οδηγία χρήσης, η συλλογή, η αξιολόγηση και η ανάλυση διεξάγονται λαμβάνοντας υπόψη γενικά αναγνωρισμένους τρόπους χρήσης. Η κλινική αξιολόγηση είναι ευθύνη του κατασκευαστή και η έκθεση κλινικής αξιολόγησης αποτελεί στοιχείο της τεχνικής τεκμηρίωσης ενός ιατροτεχνολογικού προϊόντος που πρέπει να περιλαμβάνεται στον τεχνικό φάκελο.
Πότε πραγματοποιείται η κλινική αξιολόγηση και γιατί είναι σημαντική;
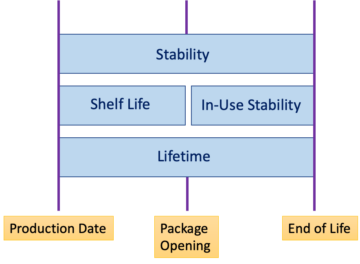
Η κλινική αξιολόγηση διεξάγεται καθ' όλη τη διάρκεια του κύκλου ζωής ενός ιατροτεχνολογικού προϊόντος, ως μια συνεχής διαδικασία. Συνήθως, εκτελείται για πρώτη φορά κατά την ανάπτυξη μιας ιατρικής συσκευής για τον εντοπισμό δεδομένων που πρέπει να δημιουργηθούν για πρόσβαση στην αγορά. Η κλινική αξιολόγηση είναι υποχρεωτική για την αρχική Σήμανση CE και πρέπει να ενημερωθεί ενεργά στη συνέχεια.
Η κλινική αξιολόγηση είναι απαραίτητη και σημαντική γιατί διασφαλίζει ότι η αξιολόγηση της ασφάλειας και της απόδοσης της συσκευής βασίζεται σε επαρκή κλινικά στοιχεία καθ' όλη τη διάρκεια ζωής του ιατροτεχνολογικού προϊόντος στην αγορά. Αυτή η συνεχής διαδικασία επιτρέπει στους κατασκευαστές να παρέχουν στους κοινοποιημένους οργανισμούς και τις αρμόδιες αρχές επαρκή κλινικά στοιχεία για την απόδειξη της συμμόρφωσης της συσκευής με τις Βασικές Απαιτήσεις καθ' όλη τη διάρκεια ζωής της (για παράδειγμα για σήμανση CE, εκπλήρωση απαιτήσεων επιτήρησης και αναφοράς μετά τη διάθεση στην αγορά ή κατά τη διάρκεια της επιτήρησης διαδικασίες).
Ποιος πρέπει να κάνει την Κλινική Αξιολόγηση
Η κλινική αξιολόγηση πρέπει να διεξάγεται από άτομο ή ομάδα με τα κατάλληλα προσόντα. Ως γενική αρχή, οι αξιολογητές θα πρέπει να γνωρίζουν τα ακόλουθα:
- μεθοδολογία έρευνας (συμπεριλαμβανομένου του σχεδιασμού κλινικής έρευνας και της βιοστατιστικής)·
- διαχείριση πληροφοριών (π.χ. επιστημονικό υπόβαθρο ή προσόντα βιβλιοθηκονομίας· εμπειρία με σχετικές βάσεις δεδομένων όπως το Embase και το Medline).
- ρυθμιστικές απαιτήσεις; και
- ιατρική συγγραφή (π.χ. μεταπτυχιακή εμπειρία σε σχετική επιστήμη ή ιατρική, κατάρτιση και εμπειρία στην ιατρική συγγραφή, συστηματική ανασκόπηση και αξιολόγηση κλινικών δεδομένων). εμπειρία εάν ένα πτυχίο δεν αποτελεί προϋπόθεση για μια δεδομένη εργασία.
Ο κύκλος ζωής προϊόντος-ζωής μιας κλινικής αξιολόγησης
CDP (Σχέδιο Κλινικής Ανάπτυξης)
Στην αρχή της διαδικασίας ανάπτυξης, το σχέδιο κλινικής ανάπτυξης καθορίζει τον τρόπο με τον οποίο συλλέγονται επαρκή κλινικά δεδομένα για μετέπειτα κλινική αξιολόγηση. Αυτό μπορεί να περιλαμβάνει διερευνητικές έρευνες, σκοπιμότητα και πιλοτικές μελέτες για επιβεβαιωτικές έρευνες. Σε αυτό το στάδιο μπορεί επίσης να υποβληθεί πρόταση για πιθανές δραστηριότητες PMCF.
CEP (Σχέδιο Κλινικής Αξιολόγησης)
Πριν από τη διεξαγωγή της κλινικής αξιολόγησης, το CEP καθορίζει το εύρος της κλινικής απόδειξης. Τα διαθέσιμα προ και κλινικά δεδομένα, οι εναπομένοντες εναπομένοντες κίνδυνοι, οι νέοι κίνδυνοι (από PMS/PMCF/καταγγελίες) καθώς και όλοι οι άλλοι ισχυρισμοί (επίσης από την εμπορία) λαμβάνονται υπόψη. Δημιουργούνται κλινικά σχετικές ερωτήσεις, καθώς και ανοιχτές ερωτήσεις από τη διαχείριση κινδύνου. Καθορίζεται η στρατηγική αναζήτησης (πηγές, όροι αναζήτησης, κριτήρια επιλογής και αξιολόγησης) που θα εφαρμοστεί για την κλινική αξιολόγηση.
CER (έκθεση κλινικής αξιολόγησης)
Το CER αντιπροσωπεύει τα αποτελέσματα της κλινικής αξιολόγησης. Τα κλινικά δεδομένα συλλέγονται, επιλέγονται, αξιολογούνται και αναλύονται. Ελέγχεται εάν η συσκευή πληροί τις απαιτήσεις για ασφάλεια, απόδοση, ανεπιθύμητες παρενέργειες και την αναλογία οφέλους-κινδύνου που ορίζεται από το MDR. Επιπλέον, οι διαθέσιμες επί του παρόντος εναλλακτικές επιλογές θεραπείας πρέπει επίσης να ληφθούν υπόψη. Τέλος, συζητείται η ανάγκη για περαιτέρω κλινικά δεδομένα (δραστηριότητες PMCF) και μεταβιβάζεται στο PMS.PMS, PMCF, SSCP
PMS (Παρακολούθηση μετά την κυκλοφορία), PMCF Κλινική παρακολούθηση μετά την κυκλοφορία)
Στο Σχέδιο PMS, ο κατασκευαστής ορίζει πώς θα παρακολουθείται η συσκευή μετά την κυκλοφορία στην αγορά και ποια δεδομένα θα συλλέγονται. Ο σχεδιασμός δραστηριοτήτων για συγκεκριμένο προϊόν πρέπει να λαμβάνει υπόψη τα ευρήματα από την κλινική αξιολόγηση και το δυναμικό κινδύνου της συσκευής. Οι μεθοδολογίες για την ανάλυση των δεδομένων και τα κριτήρια για την ανάλυση έχουν καθοριστεί και θα πρέπει να είναι τελευταίας τεχνολογίας. Ο κατασκευαστής είναι υπεύθυνος για τη συλλογή των δεδομένων στην αγορά προληπτικά. PMCF αποτελεί μέρος του προεμμηνορροϊκού συνδρόμου και προορίζεται να καλύψει τα κενά που δεν μπορούσαν να απαντηθούν στο πλαίσιο της κλινικής αξιολόγησης (π.χ. μακροχρόνια συμπεριφορά, παρακολούθηση ανεπιθύμητων ενεργειών και αντενδείξεις).
SSCP (για συσκευές Κλάσης III) (Σύνοψη Ασφάλειας ΚΑΙ Κλινικής Απόδοσης)
An SSCP Η έκθεση πρέπει να συντάσσεται μόνο από κατασκευαστές κατηγορίας III και εμφυτεύσιμων συσκευών. Η αναφορά αναφέρεται στο εγχειρίδιο χρήσης ή στην ετικέτα και διατίθεται δημόσια μέσω EUDAMED. Η αναφορά πρέπει να γίνει κατανοητή από απλούς. Ο σκοπός της αναφοράς είναι να εισαγάγει τη συσκευή στο πλαίσιο της εφαρμογής της και να εξηγήσει εναλλακτικές θεραπευτικές ή διαγνωστικές επιλογές καθώς και τους υπολειπόμενους κινδύνους και τις ανεπιθύμητες ενέργειες. Πριν από τη δημοσίευση, η έκθεση επικυρώνεται από τον κοινοποιημένο οργανισμό.
Προληπτική επιτήρηση μετά τη διάθεση στην αγορά
Η προληπτική φάση PMS είναι εκεί PMCF διενεργούνται δραστηριότητες συμπεριλαμβανομένης της αξιολόγησης των δεδομένων της αγοράς. Οι στρατηγικές που καθορίστηκαν αρχικά στο σχέδιο PMS πρέπει να προσδιορίζουν συμβάντα που μπορούν να αναφερθούν, όπως περιπτώσεις επαγρύπνησης και μπορούν να αναφέρονται εγκαίρως. Το Vigilance περιγράφει την αναφορά σοβαρών περιστατικών και επιτόπιων διορθωτικών ενεργειών ασφάλειας στην αρχή. Για το σκοπό αυτό, κάθε κατασκευαστής χρειάζεται ένα κατάλληλο σύστημα στο οποίο διασφαλίζει ότι είναι δυνατή η αξιολόγηση και ανάλυση τέτοιων γεγονότων και ότι μπορούν να τηρηθούν οι προθεσμίες για την αναφορά τους. Τα αποτελέσματα των δραστηριοτήτων του PMCF τεκμηριώνονται και αναλύονται σε ένα ή περισσότερα PMCF Αναφορές. Τα συμπεράσματα της έκθεσης PMCF πρέπει να λαμβάνουν υπόψη την κλινική αξιολόγηση και τη διαχείριση κινδύνου. Στατιστικά σημαντικές αυξήσεις στη συχνότητα ή τη σοβαρότητα των μη σοβαρών περιστατικών ή των αναμενόμενων ανεπιθύμητων παρενεργειών πρέπει να αναφέρονται στην αρμόδια αρχή εάν επηρεάζουν τη σχέση οφέλους-κινδύνου.
PSUR(IIA, IIB, III) PMS
Ο σκοπός της αναφοράς PMS είναι να αποκτήσει πληροφορίες για τη συμπεριφορά της συσκευής στην αγορά σε ολόκληρο τον κύκλο ζωής του προϊόντος. Έχει δημιουργηθεί μια αναφορά PMS για συσκευές κατηγορίας I και περιλαμβάνει μια σύνοψη των αποτελεσμάτων από δεδομένα αγοράς που συλλέχθηκαν κατά την περίοδο παρατήρησης, τα αποτελέσματα μεταβιβάζονται στην κλινική αξιολόγηση. Η CAPA ορίζεται και επεξηγείται. Αυτά μπορούν στη συνέχεια να χρησιμοποιηθούν για περαιτέρω ανάπτυξη προϊόντος καθώς και για τη διασφάλιση της ασφάλειας και της συμμόρφωσης της συσκευής με τις απαιτήσεις του κανονισμού ανά πάσα στιγμή κατά τη διάρκεια του κύκλου ζωής. ΕΝΑ PSUR (αναφορά περιοδικής ενημέρωσης ασφάλειας) προετοιμάζεται για προϊόντα κατηγορίας IIa, IIb και III και περιλαμβάνει μια περίληψη των αποτελεσμάτων και την CAPA, όπως κάνει η έκθεση PMS. Επιπλέον, η ΕΠΠΑ περιλαμβάνει επίσης τα συμπεράσματα από την αξιολόγηση οφέλους-κινδύνου και τυχόν κρίσιμα αποτελέσματα από PMCF.
Διαδικασία QualityMedDev
Η QualityMedDev ετοίμασε μια διαδικασία κλινικής αξιολόγησης για να ανταποκριθεί στις νέες απαιτήσεις που σχετίζονται με το EU MDR 2017/745. Μη διστάσετε να κάνετε λήψη αυτής της διαδικασίας για να την προσθέσετε στο σύστημα ποιότητας σας.
Ο Πίνακας Περιεχομένων μιας Έκθεσης Κλινικής Αξιολόγησης
- Υπογραφές Υπεύθυνου Προσώπου
- Ιστορικό εγγράφων
- Εισαγωγή και Πεδίο της Κλινικής Αξιολόγησης
- Περιγραφή της Εξεταζόμενης Συσκευής
- Ιστορικό υπόβαθρο
- Τεχνική περιγραφή της συσκευής
- Εξαρτήματα και υλικά που χρησιμοποιούνται για τη συσκευή
- Παραλλαγές της συσκευής που καλύπτονται σε αυτήν την κλινική αξιολόγηση
- Ταξινόμηση της συσκευής
- Προβλεπόμενος Σκοπός Σύμφωνα με το Πληροφοριακό Υλικό του Κατασκευαστή
- Προβλεπόμενη χρήση ως ορίζεται από τον κατασκευαστή
- Ενδείξεις
- Αντενδείξεις
- Ανεπιθύμητες Επιδράσεις
- Προειδοποιήσεις
- Προφυλάξεις
- Περαιτέρω οδηγίες που παρέχονται από τον κατασκευαστή
- Μέθοδοι που πρέπει να εφαρμοστούν για αυτήν την Κλινική Αξιολόγηση
- Δήλωση Πληρότητας θεωρούμενων Δεδομένων
- Περιεχόμενα της Έκθεσης Κλινικής Αξιολόγησης
- αναφορές
συμπεράσματα
Συμπερασματικά, έχουμε περάσει από τις κύριες απαιτήσεις που σχετίζονται με την Έκθεση Κλινικής Αξιολόγησης και τα σχετικά θέματα. Συγκεκριμένα, περάσαμε από τις απαιτήσεις που σχετίζονται με το EU MDR 2017/745 και το MEDDEV 2.7/1(4).
Ενημερωτικό δελτίο QualityMedDev
Η QualityMedDev είναι μια διαδικτυακή πλατφόρμα που παρέχει εκτεταμένη υποστήριξη σε κατασκευαστές ιατρικών συσκευών και εταιρείες συμβούλων στον τομέα της συμμόρφωσης με τους κανονισμούς. Δημοσιεύουμε αναρτήσεις ιστολογίου για θέματα διαχείρισης ποιότητας και θέματα που σχετίζονται με κανονιστικά θέματα και παρέχουμε εκτεταμένη τεκμηρίωση έτοιμη για λήψη για την υποστήριξη της εφαρμογής και της συντήρησης ποιοτικού συστήματος ή πιστοποιητικών που σχετίζονται με προϊόντα. Η QualityMedDev παρέχει συμβουλευτική υπηρεσία για θέματα ποιότητας και κανονιστικών υποθέσεων για κατασκευαστές ιατρικών συσκευών, μην διστάσετε να μάθετε περισσότερα για τις υπηρεσίες μας στο αφιερωμένη σελίδα του ιστότοπου. Υποστηρίζουμε την κατασκευή του ολοκαίνουργιο σύστημα ποιότητας και / ή προετοιμασία του Τεχνική τεκμηρίωση σχετική με ΝΔ.
Δημοσιεύουμε επίσης ένα περιοδικό ενημερωτικό δελτίο με στόχο την ανταλλαγή πληροφοριών σχετικά με τα νέα άρθρα ή έγγραφα που έχουν διατεθεί μέσω του ιστότοπου QualityMedDev.
Εάν θέλετε να μείνετε ενημερωμένοι με τα τελευταία νέα και ανάλυση από τον ρυθμιστικό κόσμο για τον τομέα των ιατρικών συσκευών, εγγραφείτε στο ενημερωτικό δελτίο μας συμπληρώνοντας την παρακάτω φόρμα.
Πηγή: https://www.qualitymeddev.com/2021/07/12/clinical-evaluation/
- πρόσβαση
- Λογαριασμός
- δραστηριοτήτων
- Όλα
- ανάλυση
- Εφαρμογή
- Τέχνη
- εμπορεύματα
- Blog
- Μηνύματα Blog
- σώμα
- περιπτώσεις
- αξιώσεις
- Συλλέγοντας
- Εταιρείες
- Συμμόρφωση
- δόμηση
- συμβουλευτικές
- περιεχόμενα
- ημερομηνία
- βάσεις δεδομένων
- Υπηρεσίες
- Ανάπτυξη
- Συσκευές
- έγγραφα
- EU
- εκδηλώσεις
- Τελικά
- Όνομα
- ακολουθήστε
- μορφή
- εκπλήρωση
- General
- Επισημάνετε
- Πως
- HTTPS
- προσδιορίσει
- Συμπεριλαμβανομένου
- πληροφορίες
- ιδέες
- έρευνα
- IT
- γνώση
- ξεκινήσει
- διαχείριση
- Κατασκευαστής
- αγορά
- Μάρκετινγκ
- υλικά
- ιατρικών
- ιατρική συσκευή
- ιατρική
- παρακολούθηση
- Πλοήγηση
- νέα
- Newsletter
- διαδικτυακά (online)
- ανοίξτε
- Επιλογές
- τάξη
- ΑΛΛΑ
- επίδοση
- πιλότος
- σχεδιασμό
- πλατφόρμες
- συνδέω
- Δημοσιεύσεις
- Προϊόν
- ανάπτυξη προϊόντων
- Προϊόντα
- πρόταση
- δημοσιεύει
- ποιότητα
- Ρυθμιστικές Αρχές
- κανονισμοί
- Κανονιστική Συμμόρφωση
- αναφέρουν
- Εκθέσεις
- απαιτήσεις
- Αποτελέσματα
- ανασκόπηση
- Κίνδυνος
- διαχείριση των κινδύνων
- Ασφάλεια
- Επιστήμη
- Αναζήτηση
- επιλέγονται
- Υπηρεσίες
- Στάδιο
- Εκκίνηση
- Κατάσταση
- παραμονή
- Στρατηγική
- μελέτες
- υποστήριξη
- επιτήρηση
- σύστημα
- Τεχνικός
- Θεραπευτικός
- ώρα
- Θέματα
- Εκπαίδευση
- θεραπεία
- Ενημέρωση
- Ιστοσελίδα : www.example.gr
- WordPress
- κόσμος
- γραφή