23 Δεκεμβρίου 2022 (Ειδήσεις Nanowerk) Οι επιστήμονες χρησιμοποίησαν βλαστοκύτταρα ασθενών και τρισδιάστατη βιοεκτύπωση για να παράγουν οφθαλμικό ιστό που θα βελτιώσει την κατανόηση των μηχανισμών των ασθενειών που τυφλώνουν (Μέθοδοι φύσης, «Ο 3D εξωτερικός φραγμός του αμφιβληστροειδούς αποκαλύπτει τον εξαρτώμενο από RPE χοριοειδικό φαινότυπο σε προχωρημένη εκφύλιση της ωχράς κηλίδας»). Η ερευνητική ομάδα από το Εθνικό Ινστιτούτο Οφθαλμών (NEI), μέρος των Εθνικών Ινστιτούτων Υγείας, εκτύπωσε έναν συνδυασμό κυττάρων που σχηματίζουν το εξωτερικό φράγμα αίματος-αμφιβληστροειδούς - οφθαλμικός ιστός που υποστηρίζει τους φωτοϋποδοχείς του αμφιβληστροειδούς. Η τεχνική παρέχει μια θεωρητικά απεριόριστη παροχή ιστού που προέρχεται από τον ασθενή για τη μελέτη εκφυλιστικών ασθενειών του αμφιβληστροειδούς όπως η ηλικιακή εκφύλιση της ωχράς κηλίδας (AMD).
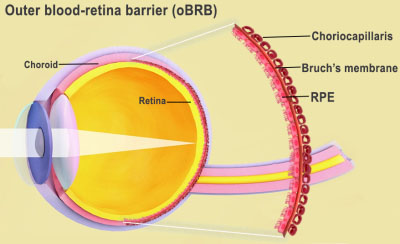
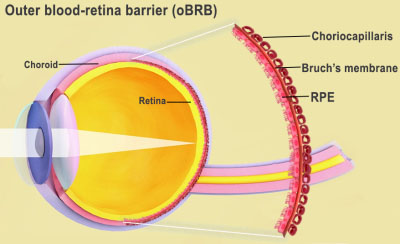 Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς είναι η διαχωριστική επιφάνεια του αμφιβληστροειδούς και του χοριοειδούς, συμπεριλαμβανομένης της μεμβράνης του Bruch και της χοριοτριχοειδής. (Εικόνα: Εθνικό Ινστιτούτο Οφθαλμών) Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς του ματιού περιλαμβάνει το χρωστικό επιθήλιο του αμφιβληστροειδούς, τη μεμβράνη του Bruch και τη χοριοτριχοειδή. Πίστωση εικόνας: National Eye Institute. Ο Bharti και οι συνεργάτες του συνδύασαν τρεις ανώριμους τύπους χοριοειδικών κυττάρων σε μια υδρογέλη: περικύτταρα και ενδοθηλιακά κύτταρα, τα οποία είναι βασικά συστατικά των τριχοειδών αγγείων. και ινοβλάστες, που δίνουν δομή στους ιστούς. Στη συνέχεια, οι επιστήμονες εκτύπωσαν το τζελ σε ένα βιοδιασπώμενο ικρίωμα. Μέσα σε λίγες μέρες, τα κύτταρα άρχισαν να ωριμάζουν σε ένα πυκνό τριχοειδές δίκτυο. Την ένατη ημέρα, οι επιστήμονες έσπειραν επιθηλιακά κύτταρα με χρωστική ουσία αμφιβληστροειδούς στην άλλη πλευρά του ικριώματος. Ο εκτυπωμένος ιστός έφτασε σε πλήρη ωριμότητα την ημέρα 42. Οι αναλύσεις ιστών και οι γενετικές και λειτουργικές εξετάσεις έδειξαν ότι ο εκτυπωμένος ιστός έμοιαζε και συμπεριφέρθηκε παρόμοια με τον φυσικό εξωτερικό φραγμό αίματος-αμφιβληστροειδούς. Υπό το επαγόμενο στρες, ο τυπωμένος ιστός εμφάνισε μοτίβα πρώιμης AMD, όπως εναποθέσεις drusen κάτω από το RPE και εξέλιξη σε όψιμο ξηρό στάδιο AMD, όπου παρατηρήθηκε υποβάθμιση του ιστού. Το χαμηλό οξυγόνο προκάλεσε υγρή εμφάνιση παρόμοια με την AMD, με υπερπολλαπλασιασμό των χοριοειδών αγγείων που μετανάστευσαν στη ζώνη υπο-RPE. Τα φάρμακα Anti-VEGF, που χρησιμοποιούνται για τη θεραπεία της AMD, κατέστειλαν την υπερανάπτυξη και τη μετανάστευση αυτού του αγγείου και αποκατέστησαν τη μορφολογία των ιστών.
Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς είναι η διαχωριστική επιφάνεια του αμφιβληστροειδούς και του χοριοειδούς, συμπεριλαμβανομένης της μεμβράνης του Bruch και της χοριοτριχοειδής. (Εικόνα: Εθνικό Ινστιτούτο Οφθαλμών) Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς του ματιού περιλαμβάνει το χρωστικό επιθήλιο του αμφιβληστροειδούς, τη μεμβράνη του Bruch και τη χοριοτριχοειδή. Πίστωση εικόνας: National Eye Institute. Ο Bharti και οι συνεργάτες του συνδύασαν τρεις ανώριμους τύπους χοριοειδικών κυττάρων σε μια υδρογέλη: περικύτταρα και ενδοθηλιακά κύτταρα, τα οποία είναι βασικά συστατικά των τριχοειδών αγγείων. και ινοβλάστες, που δίνουν δομή στους ιστούς. Στη συνέχεια, οι επιστήμονες εκτύπωσαν το τζελ σε ένα βιοδιασπώμενο ικρίωμα. Μέσα σε λίγες μέρες, τα κύτταρα άρχισαν να ωριμάζουν σε ένα πυκνό τριχοειδές δίκτυο. Την ένατη ημέρα, οι επιστήμονες έσπειραν επιθηλιακά κύτταρα με χρωστική ουσία αμφιβληστροειδούς στην άλλη πλευρά του ικριώματος. Ο εκτυπωμένος ιστός έφτασε σε πλήρη ωριμότητα την ημέρα 42. Οι αναλύσεις ιστών και οι γενετικές και λειτουργικές εξετάσεις έδειξαν ότι ο εκτυπωμένος ιστός έμοιαζε και συμπεριφέρθηκε παρόμοια με τον φυσικό εξωτερικό φραγμό αίματος-αμφιβληστροειδούς. Υπό το επαγόμενο στρες, ο τυπωμένος ιστός εμφάνισε μοτίβα πρώιμης AMD, όπως εναποθέσεις drusen κάτω από το RPE και εξέλιξη σε όψιμο ξηρό στάδιο AMD, όπου παρατηρήθηκε υποβάθμιση του ιστού. Το χαμηλό οξυγόνο προκάλεσε υγρή εμφάνιση παρόμοια με την AMD, με υπερπολλαπλασιασμό των χοριοειδών αγγείων που μετανάστευσαν στη ζώνη υπο-RPE. Τα φάρμακα Anti-VEGF, που χρησιμοποιούνται για τη θεραπεία της AMD, κατέστειλαν την υπερανάπτυξη και τη μετανάστευση αυτού του αγγείου και αποκατέστησαν τη μορφολογία των ιστών.
 Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς του ματιού περιλαμβάνει το χρωστικό επιθήλιο του αμφιβληστροειδούς, τη μεμβράνη του Bruch και τη χοριοτριχοειδή. (Εικόνα: Εθνικό Ινστιτούτο Οφθαλμών) «Με την εκτύπωση κυττάρων, διευκολύνουμε την ανταλλαγή κυτταρικών ενδείξεων που είναι απαραίτητες για την κανονική ανατομία του εξωτερικού φραγμού αίματος-αμφιβληστροειδούς», είπε ο Bharti. «Για παράδειγμα, η παρουσία κυττάρων RPE προκαλεί αλλαγές γονιδιακής έκφρασης στους ινοβλάστες που συμβάλλουν στον σχηματισμό της μεμβράνης του Bruch – κάτι που είχε προταθεί πριν από πολλά χρόνια, αλλά δεν είχε αποδειχθεί μέχρι το μοντέλο μας». Μεταξύ των τεχνικών προκλήσεων που αντιμετώπισε η ομάδα του Bharti ήταν η δημιουργία ενός κατάλληλου βιοαποικοδομήσιμου ικριώματος και η επίτευξη ενός σταθερού μοτίβου εκτύπωσης μέσω της ανάπτυξης μιας ευαίσθητης στη θερμοκρασία υδρογέλης που πέτυχε διακριτές σειρές όταν ήταν κρύο αλλά διαλύονταν όταν το τζελ θερμαινόταν. Η καλή συνοχή της σειράς επέτρεψε ένα πιο ακριβές σύστημα ποσοτικοποίησης των δομών των ιστών. Βελτιστοποίησαν επίσης την αναλογία κυτταρικού μείγματος περικυττάρων, ενδοθηλιακών κυττάρων και ινοβλαστών.
Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς του ματιού περιλαμβάνει το χρωστικό επιθήλιο του αμφιβληστροειδούς, τη μεμβράνη του Bruch και τη χοριοτριχοειδή. (Εικόνα: Εθνικό Ινστιτούτο Οφθαλμών) «Με την εκτύπωση κυττάρων, διευκολύνουμε την ανταλλαγή κυτταρικών ενδείξεων που είναι απαραίτητες για την κανονική ανατομία του εξωτερικού φραγμού αίματος-αμφιβληστροειδούς», είπε ο Bharti. «Για παράδειγμα, η παρουσία κυττάρων RPE προκαλεί αλλαγές γονιδιακής έκφρασης στους ινοβλάστες που συμβάλλουν στον σχηματισμό της μεμβράνης του Bruch – κάτι που είχε προταθεί πριν από πολλά χρόνια, αλλά δεν είχε αποδειχθεί μέχρι το μοντέλο μας». Μεταξύ των τεχνικών προκλήσεων που αντιμετώπισε η ομάδα του Bharti ήταν η δημιουργία ενός κατάλληλου βιοαποικοδομήσιμου ικριώματος και η επίτευξη ενός σταθερού μοτίβου εκτύπωσης μέσω της ανάπτυξης μιας ευαίσθητης στη θερμοκρασία υδρογέλης που πέτυχε διακριτές σειρές όταν ήταν κρύο αλλά διαλύονταν όταν το τζελ θερμαινόταν. Η καλή συνοχή της σειράς επέτρεψε ένα πιο ακριβές σύστημα ποσοτικοποίησης των δομών των ιστών. Βελτιστοποίησαν επίσης την αναλογία κυτταρικού μείγματος περικυττάρων, ενδοθηλιακών κυττάρων και ινοβλαστών.
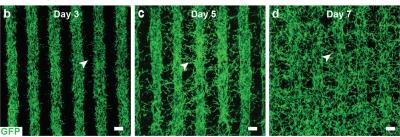 Ανάπτυξη αιμοφόρων αγγείων σε τυπωμένες σειρές μείγματος ενδοθηλίου-περικυττάρου-ινοβλαστών. Την 7η ημέρα, τα αιμοφόρα αγγεία γεμίζουν το κενό μεταξύ των σειρών, σχηματίζοντας ένα δίκτυο τριχοειδών αγγείων. (Εικόνα: Kapil Bharti) Ο συν-συγγραφέας Marc Ferrer, Ph.D., διευθυντής του 3D Tissue Bioprinting Laboratory στο Εθνικό Κέντρο Προώθησης Μεταφραστικών Επιστημών του NIH, και η ομάδα του παρείχαν τεχνογνωσία για τη βιοκατασκευή των εξωτερικών ιστών φραγμού αίματος-αμφιβληστροειδούς " in-a-well», μαζί με αναλυτικές μετρήσεις που επιτρέπουν τον έλεγχο φαρμάκων. «Οι συλλογικές μας προσπάθειες κατέληξαν σε πολύ σχετικά μοντέλα ιστού αμφιβληστροειδούς εκφυλιστικών οφθαλμικών ασθενειών», είπε ο Ferrer. «Τέτοια μοντέλα ιστών έχουν πολλές πιθανές χρήσεις σε μεταφραστικές εφαρμογές, συμπεριλαμβανομένης της θεραπευτικής ανάπτυξης». Ο Bharti και οι συνεργάτες του χρησιμοποιούν εκτυπωμένα μοντέλα φραγμού αίματος-αμφιβληστροειδούς για να μελετήσουν την AMD και πειραματίζονται με την προσθήκη επιπρόσθετων τύπων κυττάρων στη διαδικασία εκτύπωσης, όπως κύτταρα του ανοσοποιητικού, για την καλύτερη ανακεφαλαίωση του εγγενούς ιστού.
Ανάπτυξη αιμοφόρων αγγείων σε τυπωμένες σειρές μείγματος ενδοθηλίου-περικυττάρου-ινοβλαστών. Την 7η ημέρα, τα αιμοφόρα αγγεία γεμίζουν το κενό μεταξύ των σειρών, σχηματίζοντας ένα δίκτυο τριχοειδών αγγείων. (Εικόνα: Kapil Bharti) Ο συν-συγγραφέας Marc Ferrer, Ph.D., διευθυντής του 3D Tissue Bioprinting Laboratory στο Εθνικό Κέντρο Προώθησης Μεταφραστικών Επιστημών του NIH, και η ομάδα του παρείχαν τεχνογνωσία για τη βιοκατασκευή των εξωτερικών ιστών φραγμού αίματος-αμφιβληστροειδούς " in-a-well», μαζί με αναλυτικές μετρήσεις που επιτρέπουν τον έλεγχο φαρμάκων. «Οι συλλογικές μας προσπάθειες κατέληξαν σε πολύ σχετικά μοντέλα ιστού αμφιβληστροειδούς εκφυλιστικών οφθαλμικών ασθενειών», είπε ο Ferrer. «Τέτοια μοντέλα ιστών έχουν πολλές πιθανές χρήσεις σε μεταφραστικές εφαρμογές, συμπεριλαμβανομένης της θεραπευτικής ανάπτυξης». Ο Bharti και οι συνεργάτες του χρησιμοποιούν εκτυπωμένα μοντέλα φραγμού αίματος-αμφιβληστροειδούς για να μελετήσουν την AMD και πειραματίζονται με την προσθήκη επιπρόσθετων τύπων κυττάρων στη διαδικασία εκτύπωσης, όπως κύτταρα του ανοσοποιητικού, για την καλύτερη ανακεφαλαίωση του εγγενούς ιστού.
[Ενσωματωμένο περιεχόμενο]
«Γνωρίζουμε ότι η AMD ξεκινά από τον εξωτερικό φραγμό αίματος-αμφιβληστροειδούς», δήλωσε ο Kapil Bharti, Ph.D., επικεφαλής του τμήματος NEI για την Οφθαλμική και Βλαστοκύτταρα Μεταφραστικής Έρευνας. «Ωστόσο, οι μηχανισμοί έναρξης και εξέλιξης της AMD σε προχωρημένα ξηρά και υγρά στάδια παραμένουν ελάχιστα κατανοητοί λόγω της έλλειψης φυσιολογικά σχετικών ανθρώπινων μοντέλων». Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς αποτελείται από το χρωστικό επιθήλιο του αμφιβληστροειδούς (RPE), που διαχωρίζεται από τη μεμβράνη του Bruch από την πλούσια σε αιμοφόρα αγγεία χοριοτριχοειδή. Η μεμβράνη του Bruch ρυθμίζει την ανταλλαγή θρεπτικών ουσιών και αποβλήτων μεταξύ της χοριοτριχοειδούς και της RPE. Στην AMD, εναποθέσεις λιποπρωτεϊνών που ονομάζονται drusen σχηματίζονται έξω από τη μεμβράνη του Bruch, εμποδίζοντας τη λειτουργία του. Με την πάροδο του χρόνου, το RPE καταρρέει οδηγώντας σε εκφυλισμό των φωτοϋποδοχέων και απώλεια όρασης. Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς είναι η διαχωριστική επιφάνεια του αμφιβληστροειδούς και του χοριοειδούς, συμπεριλαμβανομένης της μεμβράνης του Bruch και της χοριοτριχοειδής. (Εικόνα: Εθνικό Ινστιτούτο Οφθαλμών) Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς του ματιού περιλαμβάνει το χρωστικό επιθήλιο του αμφιβληστροειδούς, τη μεμβράνη του Bruch και τη χοριοτριχοειδή. Πίστωση εικόνας: National Eye Institute. Ο Bharti και οι συνεργάτες του συνδύασαν τρεις ανώριμους τύπους χοριοειδικών κυττάρων σε μια υδρογέλη: περικύτταρα και ενδοθηλιακά κύτταρα, τα οποία είναι βασικά συστατικά των τριχοειδών αγγείων. και ινοβλάστες, που δίνουν δομή στους ιστούς. Στη συνέχεια, οι επιστήμονες εκτύπωσαν το τζελ σε ένα βιοδιασπώμενο ικρίωμα. Μέσα σε λίγες μέρες, τα κύτταρα άρχισαν να ωριμάζουν σε ένα πυκνό τριχοειδές δίκτυο. Την ένατη ημέρα, οι επιστήμονες έσπειραν επιθηλιακά κύτταρα με χρωστική ουσία αμφιβληστροειδούς στην άλλη πλευρά του ικριώματος. Ο εκτυπωμένος ιστός έφτασε σε πλήρη ωριμότητα την ημέρα 42. Οι αναλύσεις ιστών και οι γενετικές και λειτουργικές εξετάσεις έδειξαν ότι ο εκτυπωμένος ιστός έμοιαζε και συμπεριφέρθηκε παρόμοια με τον φυσικό εξωτερικό φραγμό αίματος-αμφιβληστροειδούς. Υπό το επαγόμενο στρες, ο τυπωμένος ιστός εμφάνισε μοτίβα πρώιμης AMD, όπως εναποθέσεις drusen κάτω από το RPE και εξέλιξη σε όψιμο ξηρό στάδιο AMD, όπου παρατηρήθηκε υποβάθμιση του ιστού. Το χαμηλό οξυγόνο προκάλεσε υγρή εμφάνιση παρόμοια με την AMD, με υπερπολλαπλασιασμό των χοριοειδών αγγείων που μετανάστευσαν στη ζώνη υπο-RPE. Τα φάρμακα Anti-VEGF, που χρησιμοποιούνται για τη θεραπεία της AMD, κατέστειλαν την υπερανάπτυξη και τη μετανάστευση αυτού του αγγείου και αποκατέστησαν τη μορφολογία των ιστών.
Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς είναι η διαχωριστική επιφάνεια του αμφιβληστροειδούς και του χοριοειδούς, συμπεριλαμβανομένης της μεμβράνης του Bruch και της χοριοτριχοειδής. (Εικόνα: Εθνικό Ινστιτούτο Οφθαλμών) Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς του ματιού περιλαμβάνει το χρωστικό επιθήλιο του αμφιβληστροειδούς, τη μεμβράνη του Bruch και τη χοριοτριχοειδή. Πίστωση εικόνας: National Eye Institute. Ο Bharti και οι συνεργάτες του συνδύασαν τρεις ανώριμους τύπους χοριοειδικών κυττάρων σε μια υδρογέλη: περικύτταρα και ενδοθηλιακά κύτταρα, τα οποία είναι βασικά συστατικά των τριχοειδών αγγείων. και ινοβλάστες, που δίνουν δομή στους ιστούς. Στη συνέχεια, οι επιστήμονες εκτύπωσαν το τζελ σε ένα βιοδιασπώμενο ικρίωμα. Μέσα σε λίγες μέρες, τα κύτταρα άρχισαν να ωριμάζουν σε ένα πυκνό τριχοειδές δίκτυο. Την ένατη ημέρα, οι επιστήμονες έσπειραν επιθηλιακά κύτταρα με χρωστική ουσία αμφιβληστροειδούς στην άλλη πλευρά του ικριώματος. Ο εκτυπωμένος ιστός έφτασε σε πλήρη ωριμότητα την ημέρα 42. Οι αναλύσεις ιστών και οι γενετικές και λειτουργικές εξετάσεις έδειξαν ότι ο εκτυπωμένος ιστός έμοιαζε και συμπεριφέρθηκε παρόμοια με τον φυσικό εξωτερικό φραγμό αίματος-αμφιβληστροειδούς. Υπό το επαγόμενο στρες, ο τυπωμένος ιστός εμφάνισε μοτίβα πρώιμης AMD, όπως εναποθέσεις drusen κάτω από το RPE και εξέλιξη σε όψιμο ξηρό στάδιο AMD, όπου παρατηρήθηκε υποβάθμιση του ιστού. Το χαμηλό οξυγόνο προκάλεσε υγρή εμφάνιση παρόμοια με την AMD, με υπερπολλαπλασιασμό των χοριοειδών αγγείων που μετανάστευσαν στη ζώνη υπο-RPE. Τα φάρμακα Anti-VEGF, που χρησιμοποιούνται για τη θεραπεία της AMD, κατέστειλαν την υπερανάπτυξη και τη μετανάστευση αυτού του αγγείου και αποκατέστησαν τη μορφολογία των ιστών.
 Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς του ματιού περιλαμβάνει το χρωστικό επιθήλιο του αμφιβληστροειδούς, τη μεμβράνη του Bruch και τη χοριοτριχοειδή. (Εικόνα: Εθνικό Ινστιτούτο Οφθαλμών) «Με την εκτύπωση κυττάρων, διευκολύνουμε την ανταλλαγή κυτταρικών ενδείξεων που είναι απαραίτητες για την κανονική ανατομία του εξωτερικού φραγμού αίματος-αμφιβληστροειδούς», είπε ο Bharti. «Για παράδειγμα, η παρουσία κυττάρων RPE προκαλεί αλλαγές γονιδιακής έκφρασης στους ινοβλάστες που συμβάλλουν στον σχηματισμό της μεμβράνης του Bruch – κάτι που είχε προταθεί πριν από πολλά χρόνια, αλλά δεν είχε αποδειχθεί μέχρι το μοντέλο μας». Μεταξύ των τεχνικών προκλήσεων που αντιμετώπισε η ομάδα του Bharti ήταν η δημιουργία ενός κατάλληλου βιοαποικοδομήσιμου ικριώματος και η επίτευξη ενός σταθερού μοτίβου εκτύπωσης μέσω της ανάπτυξης μιας ευαίσθητης στη θερμοκρασία υδρογέλης που πέτυχε διακριτές σειρές όταν ήταν κρύο αλλά διαλύονταν όταν το τζελ θερμαινόταν. Η καλή συνοχή της σειράς επέτρεψε ένα πιο ακριβές σύστημα ποσοτικοποίησης των δομών των ιστών. Βελτιστοποίησαν επίσης την αναλογία κυτταρικού μείγματος περικυττάρων, ενδοθηλιακών κυττάρων και ινοβλαστών.
Ο εξωτερικός φραγμός αίματος-αμφιβληστροειδούς του ματιού περιλαμβάνει το χρωστικό επιθήλιο του αμφιβληστροειδούς, τη μεμβράνη του Bruch και τη χοριοτριχοειδή. (Εικόνα: Εθνικό Ινστιτούτο Οφθαλμών) «Με την εκτύπωση κυττάρων, διευκολύνουμε την ανταλλαγή κυτταρικών ενδείξεων που είναι απαραίτητες για την κανονική ανατομία του εξωτερικού φραγμού αίματος-αμφιβληστροειδούς», είπε ο Bharti. «Για παράδειγμα, η παρουσία κυττάρων RPE προκαλεί αλλαγές γονιδιακής έκφρασης στους ινοβλάστες που συμβάλλουν στον σχηματισμό της μεμβράνης του Bruch – κάτι που είχε προταθεί πριν από πολλά χρόνια, αλλά δεν είχε αποδειχθεί μέχρι το μοντέλο μας». Μεταξύ των τεχνικών προκλήσεων που αντιμετώπισε η ομάδα του Bharti ήταν η δημιουργία ενός κατάλληλου βιοαποικοδομήσιμου ικριώματος και η επίτευξη ενός σταθερού μοτίβου εκτύπωσης μέσω της ανάπτυξης μιας ευαίσθητης στη θερμοκρασία υδρογέλης που πέτυχε διακριτές σειρές όταν ήταν κρύο αλλά διαλύονταν όταν το τζελ θερμαινόταν. Η καλή συνοχή της σειράς επέτρεψε ένα πιο ακριβές σύστημα ποσοτικοποίησης των δομών των ιστών. Βελτιστοποίησαν επίσης την αναλογία κυτταρικού μείγματος περικυττάρων, ενδοθηλιακών κυττάρων και ινοβλαστών.
 Ανάπτυξη αιμοφόρων αγγείων σε τυπωμένες σειρές μείγματος ενδοθηλίου-περικυττάρου-ινοβλαστών. Την 7η ημέρα, τα αιμοφόρα αγγεία γεμίζουν το κενό μεταξύ των σειρών, σχηματίζοντας ένα δίκτυο τριχοειδών αγγείων. (Εικόνα: Kapil Bharti) Ο συν-συγγραφέας Marc Ferrer, Ph.D., διευθυντής του 3D Tissue Bioprinting Laboratory στο Εθνικό Κέντρο Προώθησης Μεταφραστικών Επιστημών του NIH, και η ομάδα του παρείχαν τεχνογνωσία για τη βιοκατασκευή των εξωτερικών ιστών φραγμού αίματος-αμφιβληστροειδούς " in-a-well», μαζί με αναλυτικές μετρήσεις που επιτρέπουν τον έλεγχο φαρμάκων. «Οι συλλογικές μας προσπάθειες κατέληξαν σε πολύ σχετικά μοντέλα ιστού αμφιβληστροειδούς εκφυλιστικών οφθαλμικών ασθενειών», είπε ο Ferrer. «Τέτοια μοντέλα ιστών έχουν πολλές πιθανές χρήσεις σε μεταφραστικές εφαρμογές, συμπεριλαμβανομένης της θεραπευτικής ανάπτυξης». Ο Bharti και οι συνεργάτες του χρησιμοποιούν εκτυπωμένα μοντέλα φραγμού αίματος-αμφιβληστροειδούς για να μελετήσουν την AMD και πειραματίζονται με την προσθήκη επιπρόσθετων τύπων κυττάρων στη διαδικασία εκτύπωσης, όπως κύτταρα του ανοσοποιητικού, για την καλύτερη ανακεφαλαίωση του εγγενούς ιστού.
Ανάπτυξη αιμοφόρων αγγείων σε τυπωμένες σειρές μείγματος ενδοθηλίου-περικυττάρου-ινοβλαστών. Την 7η ημέρα, τα αιμοφόρα αγγεία γεμίζουν το κενό μεταξύ των σειρών, σχηματίζοντας ένα δίκτυο τριχοειδών αγγείων. (Εικόνα: Kapil Bharti) Ο συν-συγγραφέας Marc Ferrer, Ph.D., διευθυντής του 3D Tissue Bioprinting Laboratory στο Εθνικό Κέντρο Προώθησης Μεταφραστικών Επιστημών του NIH, και η ομάδα του παρείχαν τεχνογνωσία για τη βιοκατασκευή των εξωτερικών ιστών φραγμού αίματος-αμφιβληστροειδούς " in-a-well», μαζί με αναλυτικές μετρήσεις που επιτρέπουν τον έλεγχο φαρμάκων. «Οι συλλογικές μας προσπάθειες κατέληξαν σε πολύ σχετικά μοντέλα ιστού αμφιβληστροειδούς εκφυλιστικών οφθαλμικών ασθενειών», είπε ο Ferrer. «Τέτοια μοντέλα ιστών έχουν πολλές πιθανές χρήσεις σε μεταφραστικές εφαρμογές, συμπεριλαμβανομένης της θεραπευτικής ανάπτυξης». Ο Bharti και οι συνεργάτες του χρησιμοποιούν εκτυπωμένα μοντέλα φραγμού αίματος-αμφιβληστροειδούς για να μελετήσουν την AMD και πειραματίζονται με την προσθήκη επιπρόσθετων τύπων κυττάρων στη διαδικασία εκτύπωσης, όπως κύτταρα του ανοσοποιητικού, για την καλύτερη ανακεφαλαίωση του εγγενούς ιστού.
- SEO Powered Content & PR Distribution. Ενισχύστε σήμερα.
- Platoblockchain. Web3 Metaverse Intelligence. Ενισχύθηκε η γνώση. Πρόσβαση εδώ.
- πηγή: https://www.nanowerk.com/news2/gadget/newsid=62077.php
- 10
- 11
- 3d
- 7
- 9
- a
- επιτευχθεί
- απέναντι
- Πρόσθετος
- εκ των προτέρων
- προηγμένες
- AMD
- μεταξύ των
- Αναλυτικός
- ανατομία
- και
- εφαρμογές
- φράγμα
- ξεκίνησε
- Καλύτερα
- μεταξύ
- Βιοκατασκευή
- αίμα
- Διακοπή
- που ονομάζεται
- Κύτταρα
- Κέντρο
- προκλήσεις
- Αλλαγές
- Συν-Συγγραφέας
- συνεργατική
- συναδέλφους
- συνδυασμός
- σε συνδυασμό
- εξαρτήματα
- συνεπής
- περιεχόμενο
- συμβάλλει
- δημιουργία
- μονάδες
- Ημερομηνία
- ημέρα
- Ημ.
- καταθέσεις
- Ανάπτυξη
- Διευθυντής
- ασθένειες
- διακριτή
- κάτω
- φάρμακο
- Ναρκωτικά
- στεγνώσει
- Νωρίς
- προσπάθειες
- ενσωματωμένο
- ενεργοποιήσετε
- Αιθέρας (ΕΤΗ)
- παράδειγμα
- ανταλλαγή
- εξειδίκευση
- μάτι
- διευκολύνοντας
- συμπληρώστε
- Αναρρίπτω
- μορφή
- σχηματισμός
- από
- πλήρη
- λειτουργία
- λειτουργικός
- παραγωγής
- Δώστε
- καλός
- Ανάπτυξη
- κεφαλές
- Υγεία
- Ωστόσο
- HTTPS
- ανθρώπινος
- εικόνα
- in
- Συμπεριλαμβανομένου
- Ινστιτούτο
- περιβάλλον λειτουργίας
- Κλειδί
- Ξέρω
- εργαστήριο
- Έλλειψη
- Αργά
- που οδηγεί
- κοίταξε
- off
- Χαμηλός
- πολοί
- ώριμος
- ωριμότητα
- μετρήσεις
- Μέσο
- μετανάστευση
- μίγμα
- μοντέλο
- μοντέλα
- περισσότερο
- εθνικός
- ντόπιος
- απαραίτητος
- δίκτυο
- κανονικός
- βελτιστοποιημένη
- εκτός
- Οξυγόνο
- μέρος
- ασθενής
- πρότυπο
- πρότυπα
- Πλάτων
- Πληροφορία δεδομένων Plato
- Πλάτωνα δεδομένα
- παίχτης
- δυναμικού
- παρουσία
- διαδικασια μας
- παράγει
- εξέλιξη
- αποδεδειγμένη
- παρέχεται
- παρέχει
- αναλογία
- φθάσει
- παραμένουν
- έρευνα
- ερευνητές
- Retina
- Πλούσιος
- ΣΕΙΡΑ
- Είπε
- ΕΠΙΣΤΗΜΕΣ
- επιστήμονες
- προσυμπτωματικού ελέγχου
- Τμήμα
- Ομοίως
- κάτι
- Χώρος
- Στάδιο
- στάδια
- ξεκινά
- Στέλεχος
- στρες
- δομή
- Μελέτη
- τέτοιος
- κατάλληλος
- προμήθεια
- Υποστηρίζει
- σύστημα
- Τεχνικός
- Δοκιμές
- Η
- θεραπευτική
- τρία
- Μέσω
- ώρα
- προς την
- θεραπεία
- τύποι
- υπό
- κατανόηση
- κατανοητή
- απεριόριστες
- χρήση
- Σκάφος
- Βίντεο
- όραμα
- Απόβλητα
- Ποιό
- Ο ΟΠΟΊΟΣ
- θα
- εντός
- χρόνια
- YouTube
- zephyrnet
Περισσότερα από Νανοχόκ
Το εμβόλιο νανοσωματιδίων θα μπορούσε να περιορίσει τη μετάσταση του καρκίνου στους πνεύμονες στοχεύοντας μια πρωτεΐνη
Κόμβος πηγής: 2334022
Σφραγίδα ώρας: 18 Οκτωβρίου 2023
Η απεικόνιση δείχνει πώς τα μικρόβια που λειτουργούν με ηλιακή ενέργεια μετατρέπουν το CO2 σε βιοπλαστικό
Κόμβος πηγής: 2190146
Σφραγίδα ώρας: 28 Ιουλίου 2023
Ο ευρυζωνικός αισθητήρας nanogap χρυσού φέρνει επανάσταση στις δοκιμές υλικών και στην ανίχνευση ιών
Κόμβος πηγής: 2548927
Σφραγίδα ώρας: 17 Απριλίου 2024
Καθοδήγηση του σχεδιασμού συσκευών πυριτίου με βελτιωμένη απόδοση
Κόμβος πηγής: 2230051
Σφραγίδα ώρας: 23 Αυγούστου 2023
Συστοιχίες κβαντικών ράβδων θα μπορούσαν να βελτιώσουν τις τηλεοράσεις ή τις συσκευές εικονικής πραγματικότητας
Κόμβος πηγής: 2211758
Σφραγίδα ώρας: 12 Αυγούστου 2023
Πρόληψη λοιμώξεων ιατρικών εμφυτευμάτων με επικαλύψεις MOF που παράγουν μονοξείδιο του αζώτου
Κόμβος πηγής: 2321383
Σφραγίδα ώρας: 11 Οκτωβρίου 2023
Το Hubble ανακάλυψε απροσδόκητα διπλό κβάζαρ στο μακρινό σύμπαν
Κόμβος πηγής: 2048568
Σφραγίδα ώρας: 5 Απριλίου 2023
Το ρομπότ «χωρίς εγκέφαλο» μπορεί να πλοηγηθεί σε πολύπλοκα εμπόδια (με βίντεο)
Κόμβος πηγής: 2261657
Σφραγίδα ώρας: 9 Σεπτεμβρίου 2023
Οι επιστήμονες ανακαλύπτουν μια νέα μέθοδο για την παραγωγή μεταλλικών νανοσωματιδίων για χρήση ως καταλύτες
Κόμβος πηγής: 2418737
Σφραγίδα ώρας: 28 Δεκεμβρίου 2023
Ένα νέο βιοεμπνευσμένο ρομπότ γαιοσκώληκα για μελλοντικές υπόγειες εξερευνήσεις
Κόμβος πηγής: 1986009
Σφραγίδα ώρας: 1 Μαρτίου, 2023
Το AtomAI φέρνει τη βαθιά μάθηση στο λογισμικό ανάλυσης δεδομένων μικροσκοπίας
Κόμβος πηγής: 2231641
Σφραγίδα ώρας: 24 Αυγούστου 2023
Τα μικρόβια που αγαπούν τα μέταλλα θα μπορούσαν να αντικαταστήσουν τη χημική επεξεργασία σπάνιων γαιών
Κόμβος πηγής: 2305393
Σφραγίδα ώρας: 2 Οκτωβρίου 2023