03. märts 2023 (Nanowerki uudised) Looma aju koosneb kümnetest miljarditest neuronitest või närvirakkudest, mis täidavad keerulisi ülesandeid, nagu emotsioonide töötlemine, õppimine ja otsuste tegemine, suheldes üksteisega neurotransmitterite kaudu. Need väikesed signaalmolekulid hajuvad – liiguvad kõrge kontsentratsiooniga piirkondadest madala kontsentratsiooniga piirkondadesse – neuronite vahel, toimides keemiliste sõnumitoojatena. Teadlased usuvad, et see hajuv liikumine võib olla aju parima funktsiooni keskmes. Seetõttu on nad püüdnud mõista spetsiifiliste neurotransmitterite rolli, tuvastades nende vabanemise ajus, kasutades amperomeetrilisi ja mikrodialüüsi meetodeid. Need meetodid ei anna aga piisavalt teavet, mistõttu on vaja paremaid tuvastustehnikaid. Sel eesmärgil töötasid teadlased välja optilise kujutise meetodi, mille puhul valgu sondid muudavad spetsiifilise neurotransmitteri tuvastamisel oma fluorestsentsi intensiivsust. Hiljuti on Jaapani Shibaura Tehnoloogiainstituudi teadlaste rühm professor Yasuo Yoshimi juhtimisel seda ideed edasi viinud. Nad on edukalt sünteesinud fluorestseeruvaid molekulaarselt trükitud polümeerseid nanoosakesi (fMIP-NP), mis toimivad sondidena spetsiifiliste neurotransmitterite – serotoniini, dopamiini ja atsetüülkoliini – tuvastamiseks. Nimelt on selliste sondide väljatöötamist seni peetud keeruliseks. Nende murranguline töö, mis avaldati ajakirjas nanomaterjalid ("Fluorestseeruvate molekulaarselt trükitud polümeersete nanoosakeste süntees, mis tuvastavad kõrge selektiivsusega väikeseid neurotransmittereid, kasutades reguleeritud pinnatihedusega immobiliseeritud malle").
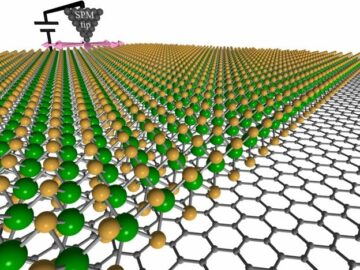
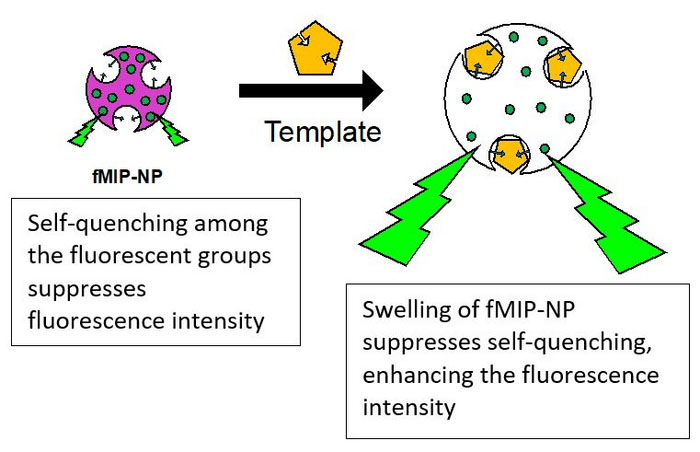 on sünteesinud fluorestseeruvad molekulaarselt trükitud polümeersed nanoosakesed (fMIP-NP), mis toimivad sondidena spetsiifiliste väikeste neurotransmitterite, nagu serotoniin, dopamiin ja atsetüülkoliin, tuvastamiseks. (Pilt: prof. Yasuo Yoshimi, SIT) Prof Yoshimi selgitab lühidalt fMIP-NP sünteesi põhialuseid. "See hõlmab mitut sammu. Esiteks kinnitatakse tuvastatav sihtmärk-neurotransmitter klaashelmeste pinnale. Järgmisena polümeriseerivad erinevate funktsioonidega monomeerid (polümeeride ehitusplokid) - tuvastamine, ristsidumine ja fluorestsents - helmeste ümber, ümbritsedes neurotransmitterit. Saadud polümeer pestakse seejärel välja, et saada nanoosake, mille neurotransmitteri struktuur on õõnsusena trükitud. See sobib ainult sihtmärk-neurotransmitteriga, nagu ainult konkreetne võti saab luku avada. Seega saavad fMIP-NP-d tuvastada ajus neile vastavad neurotransmitterid. Kui sihtmärk-neurotransmitterid mahuvad õõnsusse, paisuvad fMIP-NP-d ja muutuvad suuremaks. Teadlased viitavad sellele, et see suurendab fluorestseeruvate monomeeride vahelist kaugust, mis omakorda vähendab nende vastastikmõju, sealhulgas isekustutamist, mis pärsib fluorestsentsi. Selle tulemusena suureneb fluorestsentsi intensiivsus, mis näitab neurotransmitterite olemasolu. Teadlased parandasid oma tuvastamise selektiivsust, reguleerides fMIP-NP sünteesi ajal klaashelmeste pinnal olevat neurotransmitteri tihedust. Lisaks leiti, et neurotransmitterite fikseerimise materjali valik mängib tuvastamise spetsiifilisuses otsustavat rolli. Teadlased leidsid, et segatud silaan on neurotransmitterite, serotoniini ja dopamiini kinnitamiseks klaashelmeste pinnale parem kui puhas silaan. Segatud silaani abil sünteesitud fMIP-NP-d tuvastasid spetsiifiliselt serotoniini ja dopamiini. Seevastu need, mis sünteesiti puhta silaani abil, andsid mittespetsiifilised fMIP-NP-d, mis reageerisid mittesihtmärk-neurotransmitteritele, identifitseerides need valesti serotoniini ja dopamiinina. Samuti leiti, et polü([2-(metakrüloüüloksü)etüül]trimetüülammooniumkloriid (METMAC)-ko-metakrüülamiid), kuid mitte METMAC homopolümeer, on neurotransmitteri atsetüülkoliini efektiivne näiv matriit. Kui esimene tootis fMIP-NP-sid, mis tuvastasid selektiivselt atsetüülkoliini, siis viimane põhjustas reageerimata nanoosakesi. Need tulemused näitavad fMIP-NP-de teostatavust meie ajus vabanevate neurotransmitterite selektiivsel tuvastamisel. "Aju pildistamine selle uue tehnikaga võib paljastada seose neurotransmitterite difusiooni ja ajutegevuse vahel. See omakorda võib aidata meil ravida neuroloogilisi haigusi ja isegi luua täiustatud arvuteid, mis jäljendavad inimese ajufunktsioone,“ ütles professor Yoshimi, kes on uuenduslikust uurimistööst entusiastlik.
on sünteesinud fluorestseeruvad molekulaarselt trükitud polümeersed nanoosakesed (fMIP-NP), mis toimivad sondidena spetsiifiliste väikeste neurotransmitterite, nagu serotoniin, dopamiin ja atsetüülkoliin, tuvastamiseks. (Pilt: prof. Yasuo Yoshimi, SIT) Prof Yoshimi selgitab lühidalt fMIP-NP sünteesi põhialuseid. "See hõlmab mitut sammu. Esiteks kinnitatakse tuvastatav sihtmärk-neurotransmitter klaashelmeste pinnale. Järgmisena polümeriseerivad erinevate funktsioonidega monomeerid (polümeeride ehitusplokid) - tuvastamine, ristsidumine ja fluorestsents - helmeste ümber, ümbritsedes neurotransmitterit. Saadud polümeer pestakse seejärel välja, et saada nanoosake, mille neurotransmitteri struktuur on õõnsusena trükitud. See sobib ainult sihtmärk-neurotransmitteriga, nagu ainult konkreetne võti saab luku avada. Seega saavad fMIP-NP-d tuvastada ajus neile vastavad neurotransmitterid. Kui sihtmärk-neurotransmitterid mahuvad õõnsusse, paisuvad fMIP-NP-d ja muutuvad suuremaks. Teadlased viitavad sellele, et see suurendab fluorestseeruvate monomeeride vahelist kaugust, mis omakorda vähendab nende vastastikmõju, sealhulgas isekustutamist, mis pärsib fluorestsentsi. Selle tulemusena suureneb fluorestsentsi intensiivsus, mis näitab neurotransmitterite olemasolu. Teadlased parandasid oma tuvastamise selektiivsust, reguleerides fMIP-NP sünteesi ajal klaashelmeste pinnal olevat neurotransmitteri tihedust. Lisaks leiti, et neurotransmitterite fikseerimise materjali valik mängib tuvastamise spetsiifilisuses otsustavat rolli. Teadlased leidsid, et segatud silaan on neurotransmitterite, serotoniini ja dopamiini kinnitamiseks klaashelmeste pinnale parem kui puhas silaan. Segatud silaani abil sünteesitud fMIP-NP-d tuvastasid spetsiifiliselt serotoniini ja dopamiini. Seevastu need, mis sünteesiti puhta silaani abil, andsid mittespetsiifilised fMIP-NP-d, mis reageerisid mittesihtmärk-neurotransmitteritele, identifitseerides need valesti serotoniini ja dopamiinina. Samuti leiti, et polü([2-(metakrüloüüloksü)etüül]trimetüülammooniumkloriid (METMAC)-ko-metakrüülamiid), kuid mitte METMAC homopolümeer, on neurotransmitteri atsetüülkoliini efektiivne näiv matriit. Kui esimene tootis fMIP-NP-sid, mis tuvastasid selektiivselt atsetüülkoliini, siis viimane põhjustas reageerimata nanoosakesi. Need tulemused näitavad fMIP-NP-de teostatavust meie ajus vabanevate neurotransmitterite selektiivsel tuvastamisel. "Aju pildistamine selle uue tehnikaga võib paljastada seose neurotransmitterite difusiooni ja ajutegevuse vahel. See omakorda võib aidata meil ravida neuroloogilisi haigusi ja isegi luua täiustatud arvuteid, mis jäljendavad inimese ajufunktsioone,“ ütles professor Yoshimi, kes on uuenduslikust uurimistööst entusiastlik.
 on sünteesinud fluorestseeruvad molekulaarselt trükitud polümeersed nanoosakesed (fMIP-NP), mis toimivad sondidena spetsiifiliste väikeste neurotransmitterite, nagu serotoniin, dopamiin ja atsetüülkoliin, tuvastamiseks. (Pilt: prof. Yasuo Yoshimi, SIT) Prof Yoshimi selgitab lühidalt fMIP-NP sünteesi põhialuseid. "See hõlmab mitut sammu. Esiteks kinnitatakse tuvastatav sihtmärk-neurotransmitter klaashelmeste pinnale. Järgmisena polümeriseerivad erinevate funktsioonidega monomeerid (polümeeride ehitusplokid) - tuvastamine, ristsidumine ja fluorestsents - helmeste ümber, ümbritsedes neurotransmitterit. Saadud polümeer pestakse seejärel välja, et saada nanoosake, mille neurotransmitteri struktuur on õõnsusena trükitud. See sobib ainult sihtmärk-neurotransmitteriga, nagu ainult konkreetne võti saab luku avada. Seega saavad fMIP-NP-d tuvastada ajus neile vastavad neurotransmitterid. Kui sihtmärk-neurotransmitterid mahuvad õõnsusse, paisuvad fMIP-NP-d ja muutuvad suuremaks. Teadlased viitavad sellele, et see suurendab fluorestseeruvate monomeeride vahelist kaugust, mis omakorda vähendab nende vastastikmõju, sealhulgas isekustutamist, mis pärsib fluorestsentsi. Selle tulemusena suureneb fluorestsentsi intensiivsus, mis näitab neurotransmitterite olemasolu. Teadlased parandasid oma tuvastamise selektiivsust, reguleerides fMIP-NP sünteesi ajal klaashelmeste pinnal olevat neurotransmitteri tihedust. Lisaks leiti, et neurotransmitterite fikseerimise materjali valik mängib tuvastamise spetsiifilisuses otsustavat rolli. Teadlased leidsid, et segatud silaan on neurotransmitterite, serotoniini ja dopamiini kinnitamiseks klaashelmeste pinnale parem kui puhas silaan. Segatud silaani abil sünteesitud fMIP-NP-d tuvastasid spetsiifiliselt serotoniini ja dopamiini. Seevastu need, mis sünteesiti puhta silaani abil, andsid mittespetsiifilised fMIP-NP-d, mis reageerisid mittesihtmärk-neurotransmitteritele, identifitseerides need valesti serotoniini ja dopamiinina. Samuti leiti, et polü([2-(metakrüloüüloksü)etüül]trimetüülammooniumkloriid (METMAC)-ko-metakrüülamiid), kuid mitte METMAC homopolümeer, on neurotransmitteri atsetüülkoliini efektiivne näiv matriit. Kui esimene tootis fMIP-NP-sid, mis tuvastasid selektiivselt atsetüülkoliini, siis viimane põhjustas reageerimata nanoosakesi. Need tulemused näitavad fMIP-NP-de teostatavust meie ajus vabanevate neurotransmitterite selektiivsel tuvastamisel. "Aju pildistamine selle uue tehnikaga võib paljastada seose neurotransmitterite difusiooni ja ajutegevuse vahel. See omakorda võib aidata meil ravida neuroloogilisi haigusi ja isegi luua täiustatud arvuteid, mis jäljendavad inimese ajufunktsioone,“ ütles professor Yoshimi, kes on uuenduslikust uurimistööst entusiastlik.
on sünteesinud fluorestseeruvad molekulaarselt trükitud polümeersed nanoosakesed (fMIP-NP), mis toimivad sondidena spetsiifiliste väikeste neurotransmitterite, nagu serotoniin, dopamiin ja atsetüülkoliin, tuvastamiseks. (Pilt: prof. Yasuo Yoshimi, SIT) Prof Yoshimi selgitab lühidalt fMIP-NP sünteesi põhialuseid. "See hõlmab mitut sammu. Esiteks kinnitatakse tuvastatav sihtmärk-neurotransmitter klaashelmeste pinnale. Järgmisena polümeriseerivad erinevate funktsioonidega monomeerid (polümeeride ehitusplokid) - tuvastamine, ristsidumine ja fluorestsents - helmeste ümber, ümbritsedes neurotransmitterit. Saadud polümeer pestakse seejärel välja, et saada nanoosake, mille neurotransmitteri struktuur on õõnsusena trükitud. See sobib ainult sihtmärk-neurotransmitteriga, nagu ainult konkreetne võti saab luku avada. Seega saavad fMIP-NP-d tuvastada ajus neile vastavad neurotransmitterid. Kui sihtmärk-neurotransmitterid mahuvad õõnsusse, paisuvad fMIP-NP-d ja muutuvad suuremaks. Teadlased viitavad sellele, et see suurendab fluorestseeruvate monomeeride vahelist kaugust, mis omakorda vähendab nende vastastikmõju, sealhulgas isekustutamist, mis pärsib fluorestsentsi. Selle tulemusena suureneb fluorestsentsi intensiivsus, mis näitab neurotransmitterite olemasolu. Teadlased parandasid oma tuvastamise selektiivsust, reguleerides fMIP-NP sünteesi ajal klaashelmeste pinnal olevat neurotransmitteri tihedust. Lisaks leiti, et neurotransmitterite fikseerimise materjali valik mängib tuvastamise spetsiifilisuses otsustavat rolli. Teadlased leidsid, et segatud silaan on neurotransmitterite, serotoniini ja dopamiini kinnitamiseks klaashelmeste pinnale parem kui puhas silaan. Segatud silaani abil sünteesitud fMIP-NP-d tuvastasid spetsiifiliselt serotoniini ja dopamiini. Seevastu need, mis sünteesiti puhta silaani abil, andsid mittespetsiifilised fMIP-NP-d, mis reageerisid mittesihtmärk-neurotransmitteritele, identifitseerides need valesti serotoniini ja dopamiinina. Samuti leiti, et polü([2-(metakrüloüüloksü)etüül]trimetüülammooniumkloriid (METMAC)-ko-metakrüülamiid), kuid mitte METMAC homopolümeer, on neurotransmitteri atsetüülkoliini efektiivne näiv matriit. Kui esimene tootis fMIP-NP-sid, mis tuvastasid selektiivselt atsetüülkoliini, siis viimane põhjustas reageerimata nanoosakesi. Need tulemused näitavad fMIP-NP-de teostatavust meie ajus vabanevate neurotransmitterite selektiivsel tuvastamisel. "Aju pildistamine selle uue tehnikaga võib paljastada seose neurotransmitterite difusiooni ja ajutegevuse vahel. See omakorda võib aidata meil ravida neuroloogilisi haigusi ja isegi luua täiustatud arvuteid, mis jäljendavad inimese ajufunktsioone,“ ütles professor Yoshimi, kes on uuenduslikust uurimistööst entusiastlik.
- SEO-põhise sisu ja PR-levi. Võimenduge juba täna.
- Platoblockchain. Web3 metaversiooni intelligentsus. Täiustatud teadmised. Juurdepääs siia.
- Allikas: https://www.nanowerk.com/nanotechnology-news2/newsid=62497.php
- 1
- 10
- 11
- 7
- 9
- a
- MEIST
- tegevus
- Lisaks
- edasijõudnud
- ja
- loom
- ümber
- Uskuma
- Parem
- vahel
- suurem
- miljardeid
- Plokid
- Aju
- Ajutegevus
- lühidalt
- Ehitus
- Rakke
- keskus
- muutma
- keemiline
- valik
- suhtlemine
- keeruline
- arvutid
- kontsentratsioon
- kaaluda
- kontrast
- Vastav
- võiks
- looma
- otsustav
- kuupäev
- näitama
- Tihedus
- kujutavad
- tuvastatud
- Detection
- arenenud
- arenev
- erinev
- raske
- Diffusion
- haigused
- kaugus
- ajal
- iga
- Tõhus
- emotsioone
- tõhustatud
- entusiastlik
- Isegi
- Selgitab
- kaugele
- esimene
- sobima
- fikseeritud
- endine
- edasi
- avastatud
- Alates
- funktsioon
- funktsioonid
- Põhialused
- saama
- klaas
- murranguline
- Grupp
- süda
- aitama
- Suur
- aga
- HTTPS
- inim-
- idee
- identifitseerimiseks
- pilt
- Imaging
- paranenud
- in
- Kaasa arvatud
- valesti
- kasvanud
- Tõstab
- info
- uuenduslik
- Instituut
- interaktsioonid
- hõlmab
- IT
- Jaapan
- ajakiri
- otsuseid
- Võti
- õppimine
- Led
- Madal
- Tegemine
- materjal
- meetod
- meetodid
- Kesk-
- võib
- liikumine
- liikuma
- mitmekordne
- Neuronid
- neurotransmitter
- Uus
- järgmine
- eelkõige
- saama
- avatud
- optiline
- Muu
- eriline
- täitma
- Platon
- Platoni andmete intelligentsus
- PlatoData
- mängima
- polümeer
- polümeerid
- olemasolu
- töötlemine
- Toodetud
- Õpetaja
- Valk
- anda
- avaldatud
- hiljuti
- vähendab
- piirkondades
- reguleeritud
- suhe
- vabastama
- vabastatud
- teadustöö
- Teadlased
- kaasa
- tulemuseks
- Tulemused
- avalduma
- Roll
- Ütlesin
- teadlased
- selektiivne
- teenima
- väike
- So
- nii kaugel
- konkreetse
- eriti
- spetsiifilisus
- Sammud
- struktuur
- Edukalt
- selline
- parem
- Pind
- sihtmärk
- ülesanded
- tehnikat
- Tehnoloogia
- šabloon
- malle
- .
- oma
- seetõttu
- et
- käsitlema
- Pöörake
- mõistma
- us
- kaudu
- kuigi
- WHO
- will
- Töö
- sephyrnet
Veel alates Nanowerk
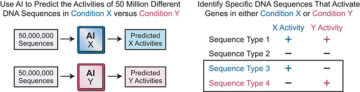
Tehisintellekt katalüüsib geenide aktiveerimise uuringuid ja paljastab haruldasi DNA järjestusi
Allikasõlm: 2101659
Ajatempel: Võib 19 2023
3D-prinditud alumiiniumsulam, millel on enneolematu väsimuskindlus
Allikasõlm: 2346768
Ajatempel: Oktoober 24, 2023
Äsja avastatud süsinikmonooksiidi ja põgenemise vahe võib aidata tuvastada elamiskõlblikke eksoplaneete
Allikasõlm: 2471166
Ajatempel: Veebruar 6, 2024
Teadlased lõid maailma väikseima jõulurekordi (videoga)
Allikasõlm: 1850116
Ajatempel: Detsember 22, 2022
Vedelmetallid raputavad sajandivanuseid keemiatehnoloogia protsesse
Allikasõlm: 2375301
Ajatempel: November 9, 2023
Täiustatud andmetöötlus toob nanostruktureeritud pindadele autonoomseid uuringuid
Allikasõlm: 2365769
Ajatempel: November 4, 2023