Sissejuhatus
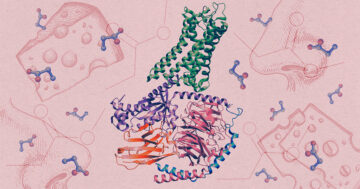
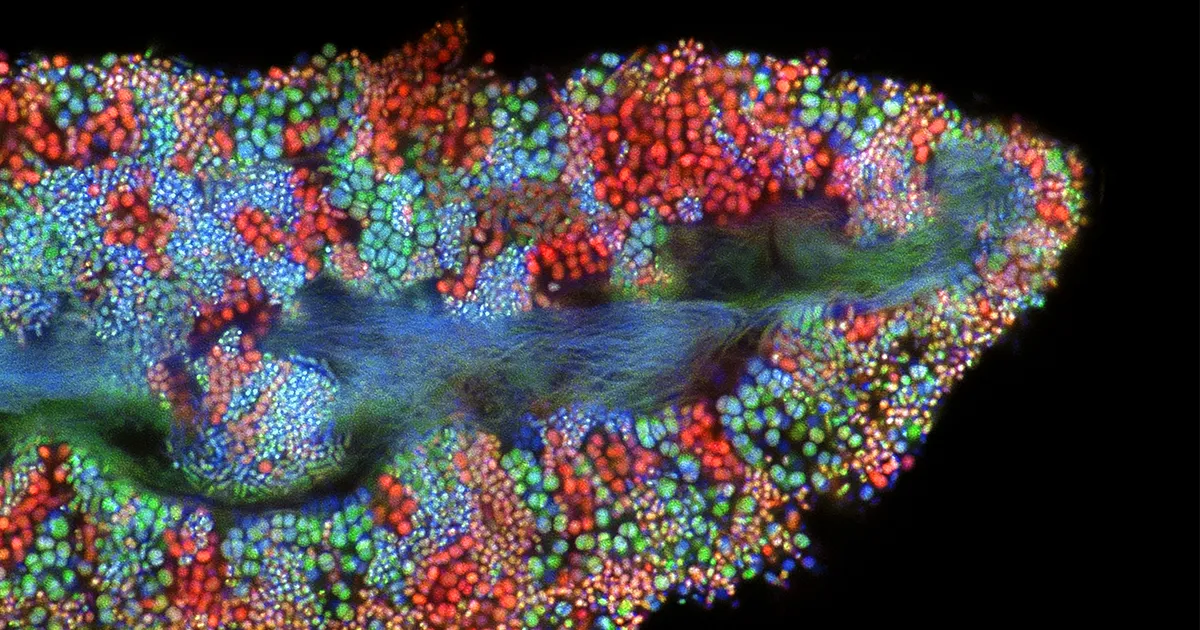
Meie keha koosneb umbes 30 triljonist inimrakust, kuid neis on ka umbes 39 triljonit mikroobirakku. Need kubisevad bakterite, viiruste, algloomade ja seente kogukonnad meie soolestikus, suus, nahal ja mujal – mida ühiselt nimetatakse inimese mikrobioomiks – ei koosne ainult vabalaadijatest ja varitsevatest patogeenidest. Selle asemel, nagu teadlased üha enam hindavad, moodustavad need mikroobid meie tervise jaoks olulised ökosüsteemid. Üha rohkem uurimusi püüavad mõista, kuidas nende delikaatsete süsteemide häired võivad röövida meilt vajalikke toitaineid, segada meie toidu seedimist ja võib-olla vallandada meie keha ja vaimu vaevusi.
Kuid me teame oma mikrobioomist ikka veel nii vähe, et hakkame alles vastama palju põhimõttelisemale küsimusele: kust need mikroobid pärinevad? Kas need võivad levida teistelt inimestelt nagu külmetusviirus või kõhutõbi?
Nüüd on inimese mikrobioomi leviku suurim ja põhjalikum analüüs andnud mõned olulised vihjed. Itaalia Trento ülikooli genoomikute juhitud uuringud on leidnud vihjeid selle kohta, et mikrobioomorganismid hüppavad palju inimeste vahel, eriti nende seas, kes veedavad palju aega koos. Leiud, avaldati jaanuaris aastal loodus, täidab olulised lüngad meie arusaamas sellest, kuidas inimesed oma mikrobiome kokku panevad ja neid kogu elu jooksul ümber sõnastavad.
Teised teadlased on uuringut kiitnud. Jose Clemente LitranSiinai mäel asuva Icahni meditsiinikooli geneetika ja genoomiteaduste dotsent tunnustas tööd kui silmapaistvat ja ütles, et see on esimene selge mõõde selle kohta, kui palju jagamist pereliikmete või koos elavate inimeste vahel oodata.
Uuring õhutab ka intrigeerivaid spekulatsioone selle kohta, kas mikroobid võivad suurendada või vähendada meie riske haigestuda sellistesse haigustesse nagu diabeet või vähk – ja seeläbi tuua ülekantav mõõde haigustele, mida tavaliselt nakkavateks ei peeta. Sest Brett Finlay, Briti Columbia ülikooli mikrobioloogiaprofessor, kes kirjutas kommentaar eest teadus aastal 2020 selle võimaluse kohta, "panivad leiud viimase naela kirstu, et mittenakkushaigusi ei tohiks nii nimetada".
Mõõtmatu mitmekesisus
Mikrobioomid on nagu sõrmejäljed: nii mitmekesised, et kahel inimesel ei saa olla identseid. Nad on ka uskumatult dünaamilised – kasvavad, kahanevad ja arenevad inimese elu jooksul nii palju, et lapse mikrobioom näeb suureks saades välja drastiliselt erinev. Käputäis mikroobiliike leidub läänestunud ühiskondades enam kui 90% inimestest, kuid enamik liike leidub 20–90% inimestest. (Isegi Escherichia coli, mis on ilmselt ainus soolebakter, mida enamik inimesi nimetada oskab, jääb alla 90% sageduse.) Uuringud näitavad, et mitteläänestunud ühiskondades on veelgi suurem mikroobide mitmekesisus ja varieeruvamad mikrobioomid.
Populatsioonis on kahel juhuslikult valitud isendil tavaliselt vähem kui pool nende mikrobioomiliikidest ühised – keskmiselt on soolestiku mikroobide kattuvus 30–35%. Mikrobioloogid vaidlevad selle üle, kas on olemas "tuum" mikroobiliikide kogum, mis on kõigil tervetel inimestel, kuid kui see on olemas, on see tõenäoliselt ühekohaline protsent koguarvust.
Sissejuhatus
Mikroobide inimeste vahel liikumise sageduse kindlaksmääramine on aga palju suurem probleem kui liikide otsimine. Üks liik võib koosneda paljudest erinevatest tüvedest või geneetilistest variantidest. Seetõttu peavad teadlased suutma tuvastada üksikuid tüvesid, vaadates mikrobioomiproovides olevaid geene. Ja inimese mikrobioomis võib esineda 2–20 miljonit unikaalset mikroobigeeni, kusjuures mikroobid muudavad oma geene pidevalt ümber, muteeruvad ja arenevad.
Seetõttu on mikrobioomi rakkude arvukuse leviku õppimine "palju keerulisem kui ühe patogeeni leviku jälgimise õppimine", ütles. Mireia Valles-Colomer, Trento ülikooli järeldoktor ja uue uuringu esimene autor. Kuni viimase ajani oli tüvede jälgimine populatsiooni kaudu võimatu.
2010is, millal Nicola Segata alustas Harvardi ülikooli järeldoktorina inimmikrobioomi projekti massiivsete geneetiliste andmekogumite analüüsimist, kuid olemasolevatel tööriistadel puudus resolutsioon, mis oli vajalik inimeste mikrobioomides leiduvate liikide kindlaksmääramiseks. Nad suutsid tuvastada üldise taksonoomilise rühma, kuhu mikroorganism kuulus, kuid see oli nagu kellegi asukoha kitsendamine USA Kesk-Lääne poole.
Järgmise paari aasta jooksul leidsid mitmed laborid tõendeid selle kohta, et sotsiaalne suhtlus ja läheduses elamine mõjutasid primaatide mikrobioomid ja hiired. Inimeste kohta tehtud uuringud suhteliselt isoleeritud populatsioonid Paapua Uus-Guineas ja mujal leiti samuti mikroobide jagamise allkirju. Mõned leidsid isegi võimaliku jälgi ülekanne lemmikloomadelt. Kuid nende uuringute piirangute tõttu ei olnud selge, kui palju levikut toimus ja kas see juhtus kõikjal samal määral.
See muutus pärast seda, kui Segata asutas 2013. aastal Trento ülikoolis oma labori. Ta hakkas koos oma meeskonnaga looma ja viimistlema metagenoomika tööriistu, mis suudaksid eristada sama liigi tüvesid, mis võimaldas uurida mikrobioomi ülekannet üksikasjalikumalt.
Segata alustas selle küsimuse uurimist 2018. aastal, analüüsides emade ja nende imikute mikroobe. Tema grupi leiud ja mitmed teised uuringud kinnitasid varasemaid kahtlusi, et emalt lapsele levib massiliselt palju, nii et ema "järeldab sündides mikrobioomi", ütles Segata. Hiljutine töö on näidanud, et emad jätkavad vormivad mikrobiome nende väikelastest mõne aasta jooksul.
Kuid mikrobioomi mitmekesisus muutub lapsepõlve ja täiskasvanuea vahel märkimisväärselt, nii et see varane pärand emadelt "ei selgita mikroobe, mida me täiskasvanutel näeme," ütles Segata. Järelkatsetes välistasid teadlased suures osas võimaluse, et uued mikroobid pärinesid toidust, mida inimesed sõid, sest need mikroobid ei suutnud soolestikku kuigi hästi koloniseerida.
Nii et "see peab olema ülekanne," ütles Segata. "Peab olema, et see, mis meil on soolestikus, tuleb teiste inimeste soolestikust."
Pere ja sõpradega jagamine
Mikrobioomide uue globaalse analüüsi jaoks lihvisid Segata, Valles-Colomer ja nende kolleegid oma tööriistu piisavalt, et ära tunda varem tundmatud liigid ja sama liigi erinevad tüved. Neid tööriistu kasutades uurisid nad enam kui 9,700 väljaheite- ja süljeproovi 20 riigist viiel kontinendil, mis esindasid väga mitmekesise eluviisiga kogukondi ning hõlmasid kogu inimese eluea ja paljusid erinevaid elukorraldusi. Nad jälgisid perede, toakaaslaste, naabrite ja külade vahel enam kui 800,000 XNUMX mikroobitüve ning arvutasid välja, kui suur protsent jagatud liikidest oli sama tüvi.
Nagu nad eeldasid, leidsid nad, et kõige rohkem jagati tüvesid emade ja imikute vahel esimesel eluaastal – umbes 50% imikute soolestikus leiduvatest ühistest liikidest olid tüved, mis levisid emalt. Ema mõju vähenes aja jooksul – langedes 27%-lt 3-aastaselt 14%-le 30-aastaselt –, kuid ei kadunud. Näidati, et mõned Hiina eakad inimesed jagavad endiselt oma ellujäänud saja-aastaseid emasid.
Sissejuhatus
eest Veena TanejaMayo kliiniku immunoloog, kes uuringus ei osalenud, oli üks üllatavamaid näpunäiteid tulemustes see, et kuigi vaginaalselt sündinud imikud jagasid oma emaga rohkem pingeid kui C-sektsiooniga sündinud imikud, kadus see erinevus kolme võrra. eluaastat. "Inimesed teevad sellest suure numbri," ütles ta, et C-sektsiooni kaudu sündinud lapsed võivad teatud haigustesse rohkem ohustada. Kuid leiud viitavad sellele, et võib-olla ei tohiks see olla suur asi.
(Seda seisukohta kinnitas uus uuring avaldati sel kuul aastal Rakkude host ja mikrob. Uuringus leiti, et C-sektsiooni kaudu sündinud lapsed said vähem oma ema mikrobioome kui vaginaalselt sündinud lapsed, kuid nad ei jäänud sellest ilma, sest nad said rinnapiimast rohkem mikroobe.)
Vananedes pärineb suur osa meie mikrobioomidest jätkuvalt inimestelt, kellega koos või läheduses elame. Pole üllatav, et Segata ja kolleegide uuring näitas, et abikaasadel ja teistel füüsiliselt intiimsetel partneritel oli palju mikroobe: 13% nende ühisest soolestiku liikidest olid sama tüve, nagu ka 38% nende jagatud suuliikidest.
Kuid platooniliselt koos elanud inimesed ei jäänud palju maha, 12% jagatud sooleliikide ja 32% jagatud suu kaudu. Seda seetõttu, et nagu Segata, Valles-Colomer ja nende meeskond leidsid, oli kõige olulisem ülekande määraja koos veedetud aeg. Ühe katuse all elavad inimesed jagasid kõige rohkem pingeid, kuid isegi samas külas elavatel inimestel oli rohkem ühiseid pingeid kui inimestel, keda lahutab suurem vahemaa. Tüvede jagamise sagedus oli erinevates ühiskondades ühtlane, kuid meeskond kinnitas varasemaid järeldusi, et mitteläänemaade inimestel on tavaliselt mitmekesisemad mikrobioomid.
Teadlased leidsid ka, et ühised tüved võivad aja jooksul kaduda. Koos üles kasvanud kaksikutel oli umbes 30% pinge jagamise tase, mis langes pärast 10-aastast lahus elamist umbes 30%-ni.
Segata peab tõenäoliseks, et enamik teisi jagatud liikide tüvesid pärinevad ka teistelt inimestelt - peamiselt lähedastelt kontaktidelt, nagu sõbrad või töökaaslased, aga võib-olla ka inimestelt, kellega kohtume palju lühidalt ja juhuslikumalt. (Lemmikloomad ei ole aga tõenäoliselt suured panustajad: Segata ütles, et loomadel on enamasti mikroobiliike, mis tavaliselt ei koloniseeri ega püsi meie sees.)
Leiud on seni tugevaimad tõendid selle kohta, et me jagame osa oma mikrobioomidest inimestega, kellega koos kõige rohkem aega veedame. Asjaolu, et autorid suutsid näha seda leviku mustrit kogu maailmas, mitte ainult ühes populatsioonis, oli rabav, ütlesid. Ilana Brito, Cornelli ülikooli biomeditsiinitehnika dotsent. Need andmekogumid on äärmiselt mürarikkad, nendes erinevates organismides toimub palju mutatsioone, lisas ta. Kuid meeskond avastas edukalt "signaali üle müra".
Pole selge, kuidas mikrobioomorganismid inimeste vahel levivad. Suudlemine ja seks seletavad osa sellest, kuid mikroobid võivad edasi kanduda ka köha ja aevastamise kaudu väljutatavate tilkade kaudu või koguda neid saastunud pindadelt. Samuti on veel palju õppida selle kohta, millised mikroobid levivad teistest kergemini. Sellele küsimusele vastamine on kriitiline, et mõista, millised on mikrobioomiorganismide leviku idee.
Tervise või haiguse levik
Nüüd, kui jagamise ulatus on paljastanud ainulaadsete mikroobide leviku mustrid, saame uurida, mis juhtub haigustega. "Selles mõttes arvan, et see töö on tõesti põhiline, " ütles Clemente.
Mõnel haigusel, mida tavaliselt nakkavaks ei peeta, võib nakkav aspekt tähelepanuta jätta. Uuringud on leidnud Finlay ütles, et paljudel inimestel, kellel on haigused, mis ei levi inimeselt inimesele, on mikrobioomid, mis tunduvad olevat "segi keeratud".
mõned E. coli tüved võivad näiteks vabastada toksiine, mis võivad suurendada vähiriski. Teatud kolorektaalvähiga inimesed, kelle mikrobioom sisaldab rohkem a Fusobakter liikidel on tavaliselt a halvem prognoos ja halvemad tulemused raviga. Soolestiku mikroobid, mis mõjutavad glükoosi ja insuliini taset organismis, on seotud rasvumise ja selliste seisunditega nagu metaboolne sündroom ja isegi II tüüpi diabeet. Tasakaalustamata soolestiku mikrobioom on seotud neurodegeneratsiooniga ja teoreetiliselt arvatakse, et see võib mängida rolli sellistes ajuseisundites nagu Alzheimeri tõbi.
Sissejuhatus
"Kui need haigused sõltuvad vähemalt osaliselt mikrobiomist ja siis on mikrobioom vähemalt osaliselt edasi kanduv, muutuvad need haigused vähemalt osaliselt edasikanduvaks," ütles Segata.
Kuid "raske küsimus on mõista, kui palju teatud mikrobioom aitab kaasa [haiguse] riskile, " ütles Clemente. Isegi enamik selliseid seoseid leidvaid uuringuid ei suuda eristada, kas mikroobid põhjustavad haigust või leiavad, et haigusriskis inimest on lihtsam koloniseerida.
Kui "halvad" mikroobid, mis suurendavad mittenakkuslike terviseprobleemide riski, võivad inimeste vahel edasi kanduda, siis teoreetiliselt võivad neid riske alandavad "head" mikroobid samuti levida. Mõned uuringud näitavad, et mikroobid võivad olla kaitsvad, eriti varases eas, selliste haiguste eest nagu astma ja allergiad. Tervete mikrobioomide tükkide tahtlik jagamine, näiteks läbi väljaheidete siirdamine, on osutunud hämmastavalt edukaks teatud haiguste ja infektsioonide (nt bakterite) ravimisel Clostridium difficile.
Me arenesime oma mikroobipopulatsioonide säilitamiseks, sest saame neist palju kasu, ütles Jens Walter, Corki ülikooli kolledži ja APC Microbiome Irelandi ökoloogia, toidu ja mikrobioomi professor. Seetõttu ei veena Walterit hüpotees, et meie ühised mikroobid võivad põhjustada haigusi, ja teda tõmbab rohkem vastupidine idee, mida mõnikord nimetatakse "vanad sõbrad" või hügieenihüpotees. See viitab sellele, et kogu evolutsiooni vältel võisid meie mikrobioomid aidata kaasa meie immuunsüsteemi reaktsioonide treenimisele. Antibiootikumide ja antiseptikumide kasutamise kaasaegne kasv ning meie suurem üldine puhtus võivad seetõttu muuta mikrobiomi koostist ja tekitada meie jaoks rohkem tervisehaavu.
Võrreldes sajanditaguse ajaga ei levita me tänapäeva maailmas kindlasti mikroobe kergemini, ütles Walter. Põletikuline soolehaigus, hulgiskleroos, reumatoidartriit ja I tüüpi diabeet – mida kõiki peetakse pigem immunoloogilisteks häireteks kui nakkushaigusteks – on enam levinud lääneriikides, kus kasutatakse laialdaselt antibiootikume ja antiseptikume.
Jagamise kasulikud või kahjulikud mõjud võivad sõltuda sellest, milliseid liike ja tüvesid jagatakse, mis on siiski natuke must kast. Samuti peaksime Brito sõnul arvestama, et meie tervist ei mõjuta mitte üksikud organismid meie mikrobioomis, vaid pigem nende kogukonnad, mis koos edasi kanduvad. Teatud organismid võivad ühes kogukonna kontekstis olla olulisemad kui teises.
Segata, Valles-Colomer ja nende meeskond analüüsisid oma uuringus ainult terveid inimesi, kuid käimasolevates uuringutes rakendavad nad oma metagenoomilisi tööriistu haigustega inimeste andmekogumitele, et näha, kas need leiud valgustavad seoseid tervise ja mikrobioomide vahel.
Samuti võtavad nad praegu andmeid kolmest päevakeskusest - imikutelt ja nende vanematelt, õdedelt-vendadelt, lemmikloomadelt ja õpetajatelt. Teadlased loodavad välja selgitada, kuidas mikroobid edasi kanduvad ja kui kaua kulub teatud soolestiku ja suuõõne mikroobide inimeste vahel hüppamiseks.
Mikrobioomorganismide leviku jälgimine jäeti pikka aega tähelepanuta, sest "me ei uskunud, et see meie tervist nii palju mõjutab," ütles Valles-Colomer. Nüüd, kui meil on tehnikad mikrobioomi uurimiseks, "näeme, et see on seotud peaaegu iga haigusega".
Toimetaja märkus: Segata ja tema grupi uurimused on saanud rahastuse Simons Foundation, mis seda ka rahastab toimetuse poolest sõltumatu ajakiri. Simonsi fondi rahastamisotsused ei mõjuta meie katvust.
- SEO-põhise sisu ja PR-levi. Võimenduge juba täna.
- Platoblockchain. Web3 metaversiooni intelligentsus. Täiustatud teadmised. Juurdepääs siia.
- Allikas: https://www.quantamagazine.org/global-microbiome-study-gives-new-view-of-shared-health-risks-20230314/
- :on
- ][lk
- $ UP
- 000
- 1
- 2018
- 2020
- 2023
- 35%
- 39
- 9
- a
- Võimalik
- MEIST
- üle
- lisatud
- täiskasvanutele
- mõjutada
- pärast
- vastu
- Eesmärgid
- Materjal: BPA ja flataatide vaba plastik
- Allergia
- Kuigi
- vahel
- summa
- analüüs
- analüüsides
- ja
- loomad
- Teine
- vastus
- Antibiootikumid
- lahus
- Rakendades
- hindama
- OLEME
- AS
- aspekt
- Partner
- seotud
- ühendused
- At
- autor
- autorid
- saadaval
- keskmine
- laps
- Bakterid
- BE
- sest
- muutuma
- hakkas
- taga
- kasulik
- kasu
- vahel
- Suur
- biomeditsiiniline
- sünd
- Natuke
- Must
- keha
- sündinud
- Kast
- Aju
- lühidalt
- tooma
- Briti
- Briti Columbia
- Bug
- by
- arvutatud
- kutsutud
- CAN
- vähk
- Põhjus
- põhjustades
- Rakke
- Centers
- Sajand
- kindel
- Vaidluste lahendamine
- Hiina
- valitud
- selge
- kliinik
- lähedal
- kolleegidega
- kollektiivselt
- kolledž
- Columbia
- Tulema
- tulevad
- ühine
- Ühenduste
- kogukond
- terviklik
- Tingimused
- läbi
- Kinnitama
- KINNITATUD
- Side
- Arvestama
- kaaluda
- järjepidev
- pidevalt
- sidemed
- kontekst
- jätkama
- pidev
- toetajad
- Köha
- võiks
- riikides
- katmine
- kattes
- looma
- loomine
- kriitiline
- Praegu
- andmed
- andmekogumid
- kuupäev
- tegelema
- arutelu
- otsused
- kindlasti
- Kraad
- sõltuv
- detail
- Diabeet
- DID
- erinevus
- erinev
- raske
- mõõde
- kaovad
- haigus
- haigused
- häired
- häired
- eristama
- jaotus
- mitu
- mitmekesisus
- Ära
- alla
- drastiliselt
- koostatud
- langes
- dünaamiline
- Ajalugu
- Varajane
- lihtsam
- kergesti
- ökosüsteemid
- mõju
- eakas
- mujal
- kohtumine
- Inseneriteadus
- piisavalt
- eriti
- oluline
- asutatud
- Eeter (ETH)
- Isegi
- tõend
- evolutsioon
- arenenud
- areneb
- näide
- olemas
- ootama
- oodatav
- Selgitama
- selgitades
- äärmiselt
- juga
- peredele
- pere
- pereliikmete
- kaugele
- mees
- vähe
- Joonis
- täitma
- lõplik
- leidma
- esimene
- toit
- eest
- vorm
- imeline
- avastatud
- Sihtasutus
- Sagedus
- sõbrad
- Alates
- kütused
- täis
- põhiline
- rahastamise
- raha
- Üldine
- Geneetika
- saama
- GitHub
- annab
- Globaalne
- maakera
- suurem
- suuresti
- Grupp
- Grupi omad
- Kasvama
- Kasvavad
- Pool
- käputäis
- juhtus
- Juhtub
- juhtub
- Raske
- Harvardi
- Harvardi ülikool
- Olema
- Tervis
- tervislik
- Held
- aitas
- vihjed
- lootes
- võõrustaja
- Kuidas
- Kuidas
- aga
- http
- HTTPS
- inim-
- Inimestel
- i
- idee
- identiques
- identifitseerima
- Immuunsüsteemi
- mõjud
- oluline
- võimatu
- in
- Suurendama
- üha rohkem
- uskumatult
- sõltumatud
- eraldi
- inimesed
- Infektsioonid
- mõju
- pärimine
- selle asemel
- suhtlemist
- segab
- intiimne
- seotud
- Iirimaa
- isoleeritud
- IT
- Itaalia
- Jaanuar
- hüppama
- Suudlevad
- Teadma
- labor
- suurelt jaolt
- suurim
- Õppida
- õppimine
- Led
- Tase
- taset
- elu
- elu
- nagu
- Tõenäoliselt
- piirangud
- seotud
- vähe
- elama
- Elab
- elu-
- liising
- Pikk
- kaua aega
- Vaata
- otsin
- Partii
- tehtud
- säilitada
- tegema
- meik
- palju
- palju inimesi
- suur
- küsimus
- Mayo kliinik
- mõõtma
- meditsiin
- liikmed
- hiired
- mikrobioloogia
- Mikrobiome
- võib
- Milk
- miljon
- mõtetes
- Kaasaegne
- kuu
- rohkem
- kõige
- ema
- MOUNT
- mitmekordne
- Hulgiskleroos
- nimi
- Lähedal
- Vajadus
- vaja
- naabrid
- Uus
- järgmine
- müra
- Rasvumine
- of
- on
- ONE
- jätkuv
- vastupidine
- Muu
- teised
- vanemad
- partnerid
- osad
- Muster
- mustrid
- Inimesed
- inimeste
- protsent
- inimene
- Majapidamine
- Füüsiliselt
- valitud
- tükki
- Platon
- Platoni andmete intelligentsus
- PlatoData
- mängima
- rahvastik
- populatsioonid
- võimalus
- võimalik
- esitada
- levinud
- eelmine
- varem
- eelkõige
- tõenäoliselt
- sond
- Probleem
- probleeme
- Õpetaja
- projekt
- teeb ettepaneku
- Kaitsev
- tõestatud
- tingimusel
- avaldatud
- Kvantamagazin
- küsimus
- tõstma
- valik
- pigem
- saadud
- hiljuti
- hiljuti
- tunnistama
- vabastama
- esindavad
- teadustöö
- Teadlased
- resolutsioon
- Revealed
- Oht
- riskide
- Roll
- katus
- s
- Ütlesin
- Sülg
- sama
- Kool
- teadus
- TEADUSED
- teadlased
- nägemine
- tunne
- komplekt
- Komplektid
- mitu
- Sugu
- Jaga
- jagatud
- jagamine
- Lühike
- peaks
- näidatud
- Signaali
- Allkirjad
- märgatavalt
- lihtsalt
- ühekordne
- suur
- nahk
- libisemine
- So
- sotsiaalmeedia
- mõned
- sille
- konkreetse
- kulutama
- kasutatud
- laiali
- Spreading
- alustatud
- Käivitus
- Veel
- Tüved
- uuringud
- Uuring
- edukas
- Edukalt
- selline
- üllatav
- süsteem
- süsteemid
- võtab
- õpetajad
- meeskond
- tehnikat
- et
- .
- oma
- Neile
- sellega
- seetõttu
- Need
- asi
- Mõtlema
- Mõtleb
- kolm
- Läbi
- läbi kogu
- seotud
- aeg
- et
- tänane
- kokku
- töövahendid
- Summa
- jälgida
- Jälgimine
- Rong
- ravimisel
- ravi
- vallandada
- triljon
- Kaksikud
- tüüpiliselt
- meie
- all
- mõistma
- mõistmine
- ainulaadne
- Ülikool
- us
- kasutama
- tavaliselt
- eri
- väga mitmekesine
- kaudu
- vaade
- Küla
- praktiliselt
- viirus
- viirused
- Haavatavused
- webp
- Hästi
- M
- kas
- mis
- WHO
- will
- koos
- Töö
- maailm
- oleks
- aasta
- aastat
- sephyrnet