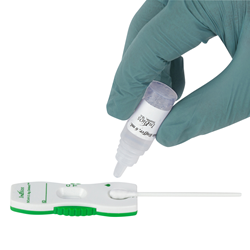
SCoV-2 Ag Detect Rapid Test
سیاتل (PRWEB) اوت 22، 2021
InBios International Inc.، یکی از توسعه دهندگان پیشرو در تست های تشخیصی بیماری های عفونی نوظهور، امروز اعلام کرد که مطالعات آزمایشگاهی نشان می دهد که SCoV-2 Ag Detect Rapid Test نوع دلتا (نسب B.1.617.2) را که مسئول افزایش سریع عفونت ها و مرگ و میرها در ایالات متحده و سراسر جهان است، شناسایی خواهد کرد. مطالعات اولیه نشان میدهد که آزمایش آنتیژن نقطه مراقبت InBios، نوع دلتا را با نرخهایی مشابه ایزوله USA-WA1-2020 که برای توسعه سنجش استفاده شد، شناسایی میکند.
دکتر Syamal Raychaudhuri، مدیر ارشد علمی InBios گفت: «داشتن یک آزمایش سریع که بتواند به سرعت و با دقت نوع دلتا را تشخیص دهد بسیار مهم است، زیرا ثابت شده است که این نوع بسیار قابل انتقال است و به سرعت گسترش می یابد. ما خوشحالیم که مطالعات نشان میدهند که آزمایش سریع ما میتواند یک ابزار تشخیصی عالی برای تشخیص نوع دلتا باشد، که ثابت میکند در حال حاضر بزرگترین چالش در مبارزه با COVID-19 است.
با توجه به مراکز کنترل و پیشگیری از بیماری، نوع دلتا در مقایسه با سایر انواع، حتی در افراد واکسینه شده، عفونی تر است و منجر به افزایش انتقال می شود. نوع دلتا که برای اولین بار در هند شناسایی شد، اکنون تخمین زده می شود که 86 درصد از کل موارد توالی کووید-19 در ایالات متحده را تشکیل می دهد.
InBios SCoV-2 Ag Detect Rapid Test مجوز استفاده اضطراری (EUA) را از سازمان غذا و داروی ایالات متحده (FDA) در می 2021 دریافت کرد. بودجه برای دستیابی به EUA برای آزمایش سریع تشخیص SCoV-2 Ag تا حدی از یک قرارداد 12.7 میلیون دلاری با فعالیت توسعه مواد پزشکی ارتش ایالات متحده تامین می شود. با بودجه ارائه شده توسط آژانس بهداشت دفاعی (DHA) از طریق قانون CARES و اداره تحقیقات و توسعه زیست پزشکی پیشرفته وزارت بهداشت و خدمات انسانی (HHS) (BARDA) که در سال 2020 اعطا شد. آزمایش ساده و سریع است - ثبت اختراع در انتظار طراحی دارای یک سواب مستقیم بینی به فرمت کاست است. این نیاز به ابزار دقیق یا مرحله رسانه حمل و نقل ندارد و می تواند در محل انجام شود و نتایج در حدود 20 دقیقه تحویل داده شود.
این محصول تاییدیه یا تاییدیه FDA را دریافت نکرده است، اما توسط FDA تحت یک EUA برای استفاده توسط آزمایشگاه های مجاز مجاز شده است. این محصول فقط برای تشخیص پروتئین های SARS-CoV-2 مجاز است، نه برای هیچ ویروس یا پاتوژن دیگری. استفاده اضطراری از این محصول فقط برای مدت زمان اعلام شرایطی مجاز است که مجوز استفاده اضطراری از تشخیص آزمایشگاهی را برای تشخیص و/یا تشخیص COVID-19 طبق بخش 564(b)(1) فدرال توجیه می کند. قانون غذا، دارو و آرایشی، 21 U.S.C. § 360bbb-3(b)(1)، مگر اینکه اعلامیه فسخ شود یا مجوز زودتر لغو شود.
برای اطلاعات بیشتر در مورد آزمایشات کووید-19 InBios، به این آدرس مراجعه کنید: http://www.inbios.com/covid-19/.
برای کسب اطلاعات بیشتر در مورد COVID-19 ، لطفا مراجعه کنید http://www.cdc.gov or http://www.who.int.
درباره InBios: InBios International Inc. متخصص در طراحی، توسعه و ساخت سنجشهای تشخیصی بیماریهای عفونی نوظهور و تهدیدات زیستی است. InBios واقع در سیاتل، واشنگتن، محصولات با کیفیت برتر را ارائه می دهد که دقیق، آسان برای استفاده و مقرون به صرفه هستند. InBios سازگار با GMP، ثبت FDA، مجوز USDA و گواهی ISO 13485:2016 است. برای اطلاعات بیشتر مراجعه کنید http://www.inbios.com
مقاله در مورد رسانه های اجتماعی یا ایمیل به اشتراک بگذارید:
