Vezető feltalálók
Előnyök
- A DNS mint építőelem
- Széles körű alkalmazások
- Alacsony költség nagy potenciállal

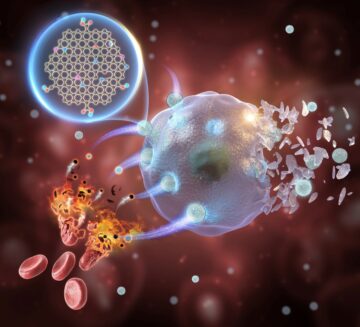
A DNS nanostruktúrák sejt- és szövetáteresztő képességükkel, biokompatibilitásukkal és nagyfokú programozhatóságukkal nanoméretű szinten ígéretes jelöltek, mint új típusú gyógyszerszállító eszközök, rendkívül specifikus diagnosztikai eszközök és eszközök annak megfejtésére, hogy a biomolekulák hogyan változtatják dinamikusan alakjukat és kölcsönhatásba lépnek egymással és a jelölt gyógyszerekkel. A Wyss Institute kutatói változatos, multifunkcionális DNS-nanotechnológiai eszközök sorozatát kínálják egyedi képességekkel és potenciállal a klinikai és orvosbiológiai kutatási területek széles körében.
DNS nanotechnológiai eszközök terápiás gyógyszerszállításhoz
A DNS-nanostruktúrák a jövőben széles körben felhasználhatók különféle biológiailag aktív molekulák, például gyógyszerek, immunerősítő antigének és adjuvánsok szállítására és bemutatására az emberi szervezetben lévő célsejtek és szövetek számára.
DNS origami, mint a rákvakcinák nagy pontosságú bejuttatási összetevői
A Wyss Intézet fejlődött rák elleni védőoltások az immunterápia javítására. Ezek a megközelítések beültethető vagy injektálható bioanyag-alapú állványokat használnak, amelyek tumorspecifikus antigéneket mutatnak be, és biomolekulákat, amelyek dendrites immunsejteket (DC-ket) vonzanak az állványba, és aktiválják őket, hogy felszabadulásuk után tumorellenes T-sejtes válaszokat tudjanak szervezni a daganatok ellen. ugyanazokat az antigéneket hordozzák. A leghatékonyabb aktiválás érdekében a DC-knek valószínűleg tumorantigénekkel és immunerősítő CpG adjuváns molekulákkal kell rendelkezniük bizonyos arányokban (sztöchiometriákban) és konfigurációkban, amelyek megfelelnek a sejtfelszínükön lévő receptormolekulák sűrűségének és eloszlásának.
Kifejezetten kifejlesztett DNS origami, úgy programozva, hogy merev négyzetrácsos tömbökké álljon össze hogy a tumorantigéneket és adjuvánsokat a DC-kben nanoméretű precízióval együtt jelenítik meg a bioanyag állványokon belül, potenciálisan növelhetik a terápiás rákvakcinák hatékonyságát, és tovább funkcionalizálhatók rákellenes gyógyszerekkel.
Kémiai módosítási stratégia a gyógyszert szállító DNS nanostruktúrák védelmére
A DNS-nanostruktúrák, mint például az önszerveződő DNS-origami ígéretes eszközök a gyógyszerek és a diagnosztika szállításában. Rugalmasan funkcionalizálhatók kis molekulájú és fehérje gyógyszerekkel, valamint olyan tulajdonságokkal, amelyek megkönnyítik a célsejtekbe és szövetekbe való eljuttatásukat. Lehetőségüket azonban gátolja a test szöveteiben és vérében való korlátozott stabilitásuk. A DNS-nanostruktúrák rendkívüli ígéretének beteljesítése érdekében a Wyss kutatói kifejlesztettek egy egyszerű, hatékony és méretezhető kémiai térhálósító megközelítés amelyek biztosítják a DNS-nanostruktúrák számára a szükséges stabilitást a gyógyszerek és a diagnosztika hatékony hordozójaként.
Két egyszerű költséghatékony lépésben a Wyss megközelítése először a kis molekulájú, nem feltűnő közömbösítő szer, PEG-oligolizin, amely több pozitív töltést hordoz, a DNS origami struktúrák lefedésére. Ellentétben az általánosan használt Mg2+ionok, amelyek mindegyike csak két negatív változást semlegesít a DNS-struktúrákban, a PEG-oligolizin egyszerre több negatív töltést is lefed, így stabil „elektrosztatikus hálót” képez, amely mintegy 400-szorosára növeli a DNS nanostruktúrák stabilitását. Ezután az a kémiai térhálósítás A glutáraldehid néven ismert reagens további stabilizáló kötéseket vezet be az elektrosztatikus hálóba, ami további 250-szeresére növeli a DNS nanostruktúrák stabilitását, meghosszabbítva felezési idejüket olyan tartományba, amely kompatibilis a klinikai alkalmazások széles skálájával.
DNS nanotechnológiai eszközök, mint ultraérzékeny diagnosztikai és analitikai eszközök
A detektálható DNS-nanostruktúrák létrehozása betegségre vagy kórokozó-specifikus nukleinsavakra válaszul elvileg lehetőséget kínál a nagyon hatékony biomarker-detektálásra különböző mintákban. Egy szintetikus oligonukleotid egyetlen molekula kötődése a célnukleinsavhoz sokkal nagyobb struktúrák létrejöttét eredményezheti kisebb szintetikus DNS-egységek, például DNS-lapok vagy téglák, nagyobb struktúrákká való kooperatív összeállításával, amelyeket aztán egyszerű laboratóriumi vizsgálatokkal lehet megjeleníteni. Azonban ezeknek a megközelítéseknek a központi akadálya a (1) nem specifikus kötődés és (2) a nem specifikus magképző események előfordulása specifikus célnukleinsav hiányában, amelyek téves pozitív eredményekhez vezethetnek. A Wyss DNS nanotechnológusai két külön alkalmazható, de kombinálható megoldást dolgoztak ki ezekre a problémákra.
Biomarker molekulák digitális számlálása DNS nanoswitch katenánokkal
Az ultra-nagy érzékenységű és specifitású biomarkerek kezdeti kimutatásának (megkötésének) lehetővé tétele érdekében a Wyss kutatói kifejlesztettek egy DNS-nanokapcsoló típust, amelyet nagyobb katenánként (latinul) terveztek. catenaláncot jelent), mechanikusan összekapcsolt, gyűrű alakú alstruktúrákból áll össze, amelyek olyan specifikus funkciókkal rendelkeznek, amelyek együttesen lehetővé teszik egyetlen biomarker molekulák kimutatását és megszámlálását. A „DNA Nanoswitch Catenane” szerkezetben egy hosszabb szintetikus DNS-szál mindkét vége két antitest-fragmenshez kapcsolódik, amelyek mindegyike specifikusan kötődik ugyanannak az érdeklődésre számot tartó biomarkermolekulának különböző részeihez, ezáltal lehetővé téve a magas célspecificitást és -érzékenységet.
Ez az áthidaló esemény azt okozza, hogy a szál „gazdagyűrűvé” zárul, amelyet különböző régiókban különböző „vendéggyűrűkkel” zárnak össze. A gazdagyűrű bezárása a vendéggyűrűket olyan konfigurációba kapcsolja, amely lehetővé teszi egy új DNS-szál szintézisét. Az újonnan szintetizált diagnosztikai szál ezután egyértelműen kimutatható egyetlen digitális molekulaszámként, miközben az antitest fragmentum/biomarker komplex megzavarása új biomarker számlálási ciklust indít el. Mind a célkötő specifitása, mind a célspecifikus DNS-szál szintézise lehetővé teszi több DNS nanoswitch katenán kombinációját is, hogy egyidejűleg számoljanak különböző biomarker molekulákat egyetlen multiplex reakcióban.
Az ultraszenzitív diagnosztikához kívánatos a leggyorsabb amplifikáció és a legalacsonyabb a hamis magképződés aránya. A DNS-nanotechnológiai megközelítések képesek ezt enzimmentesen, alacsony költséggel megvalósítani.
WILLIAM SHIH
Gyors amplifikációs platform különféle biomarkerekhez
A gyors, alacsony költségű és enzimmentes detektálási és amplifikációs platform elkerüli a nem specifikus gócképződést és amplifikációt, és lehetővé teszi sokkal nagyobb mikronméretű struktúrák önösszeállítását egyetlen magból percek alatt. A módszer, az ún.Keresztező nanomag-észlelés” lehetővé teszi a szalagok ultra-kooperatív összeállítását egyetlen biomarker kötési eseménytől kezdve. A mikron léptékű struktúrák sűrűn egyszálú „DNS-lécekből” vannak szőve, amikor is a bejövő léc „keresztezve” átkígyózik hat vagy több korábban befogott léc fölé és alá egy növekvő szalagvégen, gyenge, de nagyon specifikus kölcsönhatásokat hozva létre. kölcsönható DNS-léceivel. Az összeállítási folyamat magképzése szigorúan a célmag-specifikus, és az összeszerelés egylépéses reakcióban körülbelül 15 perc alatt további reagensek hozzáadása nélkül, széles hőmérséklet-tartományban végrehajtható. Szabványos laboratóriumi berendezésekkel az összeállított szerkezetek gyorsan láthatóvá válnak vagy más módon kimutathatók, például nagy áteresztőképességű fluoreszcens lemezleolvasó vizsgálatokkal.

AKTUÁLIS LEHETŐSÉG – INDÍTÁS
Keresztező nanomag-észlelés: nanotechnológiás fertőző betegségek diagnosztikája
Enzimmentes DNS-nanotechnológia a fertőző betegségek biomarkereinek gyors, ultraérzékeny és alacsony költségű kimutatására, széles körű hozzáféréssel az ellátási pontokban.
A Crisscross Nanoseed Detection módszerben a DNS-összeállítási folyamat a DNS nanoswitch katenánok működéséhez is köthető, amelyek nagyon specifikusan detektálnak egy biomarker molekulát, ami a molekuláris rekord megőrzéséhez vezet. Minden fennmaradt rekord képes magába építeni egy keresztezett nanoszerkezet összeállítását, kombinálva a nagy specifikus kötődést az amplifikációval a biomarkerek kimutatása érdekében.
A Wyss kutatói jelenleg a COVID-19-et okozó SARS-CoV-2 vírus és más kórokozók multiplexelhető, alacsony költségű diagnosztikájaként fejlesztik ezt a megközelítést, amely gyorsabban és olcsóbban adhat pontos eredményeket, mint a jelenleg használt technikák.
Nanoméretű eszközök a fehérjék szerkezetének és azonosságának meghatározására egymolekulás szinten
A nyomelemekből származó fehérjék azonosításának és mennyiségi meghatározásának képessége jelentős hatással lenne mind az alapkutatásra, mind a klinikai gyakorlatra, az egyes sejteken belüli fehérjeexpresszió változásainak nyomon követésétől egészen a betegségek új biomarkereinek felfedezéséig. Ezenkívül a szerkezetük és kölcsönhatásaik meghatározásának képessége új utakat nyitna meg a gyógyszerek felfedezése és jellemzése előtt. Az elmúlt évtizedekben a DNS-elemzés és a szekvenálás fejlődése vitathatatlanul forradalmasította az orvostudományt – a fehérjeanalízis ezzel egyenértékű fejlesztése azonban továbbra is kihívást jelent. Míg az olyan módszerek, mint a tömegspektrometria a fehérje azonosítására és a krioEM a szerkezet meghatározására, gyorsan fejlődtek, továbbra is kihívások vannak a felbontás és a heterogén minták nyomkövetési képessége tekintetében.
Ennek a kihívásnak a megválaszolása érdekében a Wyss Institute kutatói új megközelítést dolgoztak ki, amely a DNS nanotechnológiát egymolekulás manipulációval kombinálja, lehetővé téve a fehérjék és más makromolekulák szerkezeti azonosítását és elemzését. A „DNS Nanoswitch Calipers” (DNC-k) nagy felbontású megközelítést kínálnak az „ujjlenyomat-fehérjékhez” azáltal, hogy távolságokat mérnek és geometriákat határoznak meg az oldatban lévő egyes fehérjéken belül. A DNC-k olyan nanoeszközök, amelyeket arra terveztek, hogy mérjék a kívánt célmolekulákhoz kapcsolt DNS-fogantyúk közötti távolságot. A DNC állapotok a segítségével aktiválhatók és kiolvashatók egymolekulás erőspektroszkópia, amely lehetővé teszi több abszolút távolságmérés elvégzését minden egyes molekulán.
A DNC-k széles körben adaptálhatók a kutatás előmozdítására különböző területeken, beleértve a szerkezetbiológiát, a proteomikát, a diagnosztikát és a gyógyszerkutatást.
Minden technológia fejlesztés alatt áll, és elérhető az ipari együttműködésekhez.
.wordads-ad-wrapper { display:none; betűtípus: normál 11px Arial, sans-serif; betűköz: 1px; szöveg-dekoráció: nincs; szélesség: 100%; margó: 25px auto; párnázás: 0; } .wordads-ad-title { margin-bottom: 5px; } .wordads-ad-controls { margin-top: 5px; szöveg igazítása: jobbra; } .wordads-ad-controls span { kurzor: mutató; } .wordads-ad { width: fit-content; margó: 0 auto; }
- SEO által támogatott tartalom és PR terjesztés. Erősödjön még ma.
- Platoblockchain. Web3 metaverzum intelligencia. Felerősített tudás. Hozzáférés itt.
- Forrás: https://genesisnanotech.wordpress.com/2023/01/16/dna-nanotechnology-tools-from-design-to-applications-current-opportunities-and-collaborations-wyss-institute-harvard-university/
- 1
- 11
- a
- képesség
- Rólunk
- Abszolút
- megközelíthetőség
- pontos
- Akció
- aktív
- igazítani
- mellett
- További
- előre
- fejlett
- Után
- ellen
- lehetővé téve
- lehetővé teszi, hogy
- elemzés
- Analitikai
- és a
- Másik
- alkalmazható
- alkalmazások
- Alkalmazása
- megközelítés
- megközelít
- területek
- összeszerelt
- Assembly
- auto
- elérhető
- alapvető
- között
- Nagy
- kötődik
- kötés
- biológia
- biomarker
- orvosbiológiai
- vér
- test
- Kötvények
- fellendítésére
- széles
- Épület
- hívott
- Rák
- jelölt
- jelöltek
- képességek
- szállítás
- okai
- okozó
- Cellák
- központi
- lánc
- kihívás
- kihívások
- változik
- Változások
- díjak
- kémiai
- Klinikai
- közel
- záró
- együttműködések
- kombináció
- kombájnok
- kombinálása
- általában
- összeegyeztethető
- bonyolult
- alkatrészek
- Configuration
- kontraszt
- szövetkezet
- Költség
- költséghatékony
- kiadások
- tudott
- terjed
- burkolatok
- Covid-19
- cpg
- teremtés
- Jelenlegi
- Jelenleg
- évtizedek
- Megfejtés
- szállít
- kézbesítés
- Design
- tervezett
- észlelt
- Érzékelés
- meghatározás
- Határozzuk meg
- meghatározó
- fejlett
- fejlesztése
- Fejlesztés
- fejlesztések
- Eszközök
- különböző
- digitális
- felfedezés
- betegség
- kijelző
- távolság
- terjesztés
- számos
- dna
- gyógyszer
- gyógyszerkutatási
- Kábítószer
- minden
- Hatékony
- hatékonyan
- lehetővé
- lehetővé teszi
- lehetővé téve
- vége
- felszerelés
- Egyenértékű
- esemény
- események
- példa
- tapasztalat
- kiterjedő
- rendkívüli
- megkönnyítése
- gyorsabb
- leggyorsabb
- Jellemzők
- Fájlok
- vezetéknév
- Kényszer
- ból ből
- eleget tesz
- funkciós
- további
- Továbbá
- jövő
- generáció
- Ad
- Növekvő
- Vendég
- Fogantyúk
- Harvard
- Harvard Egyetem
- segít
- Magas
- nagy felbontású
- nagyon
- vendéglátó
- Hogyan
- azonban
- HTTPS
- emberi
- Azonosítás
- azonosítani
- Identitás
- Hatás
- javul
- in
- Beleértve
- Növeli
- egyéni
- ipar
- kezdetben
- Intézet
- kölcsönhatásba
- kölcsönható
- kölcsönhatások
- kamat
- Bevezetett
- IT
- ismert
- laboratórium
- nagyobb
- latin
- vezet
- vezető
- szint
- Valószínű
- Korlátozott
- összekapcsolt
- hosszabb
- készült
- Manipuláció
- mód
- Margó
- Tömeg
- max-width
- eszközök
- intézkedés
- mérések
- mérő
- orvostudomány
- Találkozik
- módszer
- mód
- jegyzőkönyv
- molekuláris
- molekula
- ellenőrzés
- több
- a legtöbb
- többszörös
- nanotechnológia
- Természet
- Szükség
- negatív
- háló
- Új
- normális
- akadály
- ajánlat
- Ajánlatok
- ONE
- nyitva
- Lehetőségek
- Alkalom
- Más
- másképp
- Overcome
- különös
- alkatrészek
- múlt
- emelvény
- Plató
- Platón adatintelligencia
- PlatoData
- pozitív
- potenciális
- gyakorlat
- Pontosság
- be
- korábban
- alapelv
- problémák
- folyamat
- programozott
- ígéret
- biztató
- védelme
- Fehérje
- Fehérjék
- ad
- amely
- hatótávolság
- gyors
- gyorsan
- Arány
- reakció
- Olvass
- Olvasó
- rekord
- tekintettel
- régiók
- Regisztráció
- engedje
- marad
- maradt
- kutatás
- kutatók
- Felbontás
- válasz
- Eredmények
- forradalmasította
- szalag
- merev
- Gyűrű
- azonos
- SARS koronavírus-2
- skálázható
- mag
- Érzékenység
- beállítások
- formák
- Egyszerű
- egyszerre
- egyetlen
- SIX
- kicsi
- kisebb
- So
- megoldások
- Megoldások
- különleges
- kifejezetten
- sajátosság
- Stabilitás
- stabil
- standard
- Kezdve
- kezdődik
- Államok
- Lépései
- Stratégia
- szerkezeti
- struktúra
- ilyen
- kíséret
- felületi
- szintetikus
- cél
- technikák
- Technologies
- A
- azok
- Gyógyászati
- szövetek
- nak nek
- együtt
- szerszámok
- nyom
- szállítható
- típusok
- alatt
- megértés
- egyedi
- egységek
- egyetemi
- használ
- vakcinák
- fajta
- Járművek
- vírus
- ami
- míg
- széles körben
- belül
- nélkül
- WordPress
- Munka
- lenne
- zephyrnet