皮膚がん患者向けに設計された非常に効果的な手術用包帯は、手術後の治癒過程を早める可能性があります。 英国と中国の研究者によって開発されたこの包帯は、光熱効果を利用して腫瘍の再発を防ぎます。
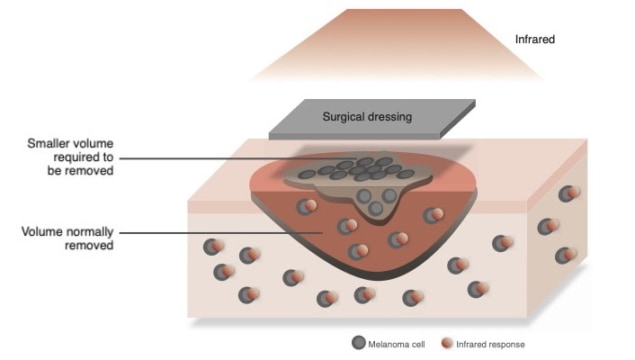
光熱療法 (PTT) は、皮膚がんを治療するための有望な技術として浮上しています。 これには、光を熱に変換する導電性ナノ材料を腫瘍に注入し、特定の波長で照射して癌細胞を殺すことが含まれます。 大きな腫瘍の場合、この治療は手術と組み合わせて実施する必要があり、感染を防ぐために外科用包帯で治療する必要がある傷が残ります。
最近では、PTT が外科用包帯に直接組み込まれている、より高度な治療法が提案されています。 これらの材料が皮膚の治癒を促進し、治療後の腫瘍の再発を防ぐことが期待されています. これらの包帯の理論化された設計は、光熱材料還元グラフェン酸化物 (rGO) に基づいています。 この材料は、酸素含有基を単層グラフェンシートに結合し、酸素含有量を減らすプロセスにかけることによって合成できます。
現在、この技術は大きな障害に直面しています: rGO は生細胞に対して有毒であり、外科用包帯に直接使用することはできません。 還元プロセスの前に、酸化グラフェンをペプチドやタンパク質などの生体分子と組み合わせることで、生体適合性を高めることができます。 ただし、その光熱応答を強化するために、材料は過酷な還元プロセスに耐えなければなりません。純粋なエタノールの環境で、180°C を超える温度で密封された反応器で実行されます。 材料の酸化グラフェンを還元すると同時に、それに付着しているより繊細な生体分子構造も破壊します。
率いるチームは、 ウー・ユアンハオ ノッティンガム大学の教授らは、還元プロセスをより低い温度で行うことを可能にする新しい技術を開発しました。 これには、「エラスチン様リコンビマー」(ELR)と呼ばれるタンパク質バイオポリマーに包まれたグラフェン酸化物フレークのアセンブリが含まれます。これは、皮膚の修復を促進し、傷を癒す能力で知られています。 チームは、これらの構造間の分子相互作用を制御することにより、ELR シェルに囲まれた多層酸化グラフェン コアを生成しました。
その後、研究者はこの構造を 70% エタノールを含む消毒剤にさらしました。 通常、この液体はバクテリアやウイルスのタンパク質の殻を通り抜けます。 この場合、それは ELR シェルをまっすぐ通過して、内部の純粋な酸化グラフェンと相互作用しました。 これにより、チームは、ELR の構造を損なわずに、85°C というはるかに低い温度で還元プロセスを開始することができました。
全体として、最終的な構造は、rGO の高い PTT 効率と組織再生を促進する能力を兼ね備えています。 追加のボーナスとして、材料はエタノールで処理して滅菌されています.

マウスの腫瘍を除去する XNUMX 極光熱療法
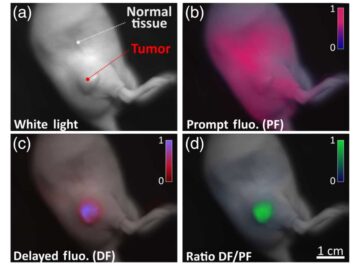
研究者は、以下を使用してアプローチを検証しました インビボの マウスでの実験では、包帯が腫瘍の再発を防ぎ、腫瘍切除後の創傷治癒を促進できることが示されました。 この材料は、15 時間ごとに近赤外光に 48 秒間さらすだけで効果を発揮します。
Wu のチームは、独自の包帯が、皮膚がん患者が自宅で提供できる実用的な手術後の治療につながることを期待しています。つまり、手術による傷の治癒を早め、皮膚の再生に伴う腫瘍の再発を防ぎます。
研究はで説明されています 高度機能材料.