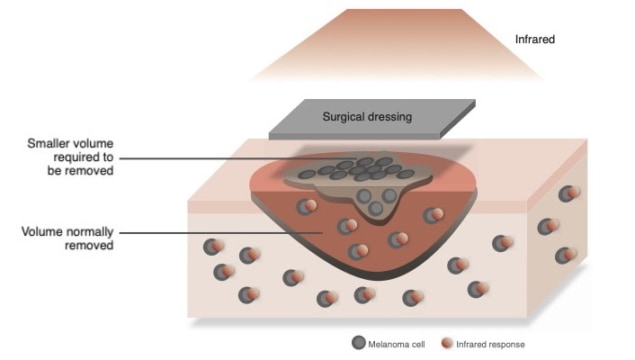
En svært effektiv kirurgisk bandasje designet for pasienter med hudkreft kan fremskynde helingsprosessen etter operasjonen. Bandasjen er utviklet av forskere i Storbritannia og Kina, og utnytter også fototermiske effekter for å forhindre at svulster dukker opp igjen.
Fototermisk terapi (PTT) har dukket opp som en lovende teknikk for behandling av hudkreft. Det innebærer å injisere svulster med ledende nanomaterialer som omdanner lys til varme, og deretter belyse dem med spesifikke bølgelengder for å drepe kreftceller. For store svulster må denne behandlingen utføres i kombinasjon med kirurgi, og etterlater sår som må behandles med kirurgiske bandasjer for å forhindre infeksjon.
Nylig har det blitt foreslått mer avanserte behandlingsmetoder der PTT integreres direkte i kirurgiske bandasjer. Håpet er at disse materialene kan fremme helbredelse i huden, samtidig som de hindrer svulster i å dukke opp igjen etter behandling. De teoretiserte designene for disse bandasjene er basert på det fototermiske materialet redusert grafenoksid (rGO). Dette materialet kan syntetiseres ved å binde oksygenholdige grupper til enkeltlags grafenark, og deretter utsette dem for en prosess som reduserer oksygeninnholdet.
For øyeblikket står denne teknikken overfor en stor veisperring: rGO er giftig for levende celler, noe som betyr at den ikke kan brukes direkte i kirurgiske bandasjer. Før reduksjonsprosessen kan grafenoksid gjøres mer biokompatibelt ved å kombinere det med biomolekyler som peptider og proteiner. Men for å forbedre sin fototermiske respons, må materialet da tåle en hard reduksjonsprosess: utført i en forseglet reaktor ved temperaturer over 180°C, i et miljø med ren etanol. Mens det reduserer materialets grafenoksid, ødelegger dette også de mer delikate biomolekylære strukturene knyttet til det.
Teamet, ledet av Yuanhao Wu ved University of Nottingham, har nå utviklet en ny teknikk som gjør at reduksjonsprosessen kan skje ved lavere temperaturer. Det involverer en samling av grafenoksidflak, innkapslet i en proteinbiopolymer kalt "elastin-like recombinamer" (ELR), som er kjent for sin evne til å fremme hudreparasjon og helbrede sår. Ved å kontrollere de molekylære interaksjonene mellom disse strukturene, produserte teamet en flerlags grafenoksidkjerne, omgitt av et ELR-skall.
Etterpå utsatte forskerne denne strukturen for et desinfeksjonsmiddel som inneholdt 70 % etanol. Vanligvis vil denne væsken trenge rett gjennom bakterier og proteinskall til virus. I dette tilfellet passerte den rett gjennom ELR-skallet for å samhandle med det rene grafenoksidet inni. Dette tillot teamet å utløse reduksjonsprosessen ved langt lavere temperaturer på 85 °C, samtidig som ELRs struktur ble intakt.
Til sammen kombinerte den endelige strukturen den høye PTT-effektiviteten til rGO med kapasiteten til å fremme vevsregenerering. Som en ekstra bonus ble materialet sterilisert gjennom behandling med etanol.

Tre-spiss fototermisk terapi eliminerer svulster hos mus
Forskerne validerte sin tilnærming ved hjelp av in vivo eksperimenter på mus, som viser at bandasjene kunne forhindre tilbakefall av svulster og fremme sårheling etter svulstreseksjon. Materialet trengte bare 15 s eksponering for nær-infrarødt lys hver 48. time for å være effektivt.
Wus team håper at de unike bandasjene kan føre til praktiske behandlinger etter operasjonen som pasienter med hudkreft kan levere hjemme: både fremskynde helingen av operasjonssårene deres, og forhindre at svulster dukker opp igjen når huden deres regenererer.
Studien er beskrevet i Avanserte funksjonelle materialer.