Черепно-мозговая травма (ЧМТ), вызванная внезапным толчком или ударом по голове, требует скорейшей диагностики. Чтобы предотвратить необратимый ущерб, жизненно важные решения о лечении должны быть приняты в течение «золотого часа» после травмы. Однако диагностировать ЧМТ на месте оказания медицинской помощи сложно, полагаясь на наблюдения бригад скорой помощи с последующими радиологическими исследованиями, такими как МРТ или КТ, по прибытии в больницу.
Чтобы обеспечить более своевременное вмешательство, исследователи из Бирмингемский университет разрабатывают портативное диагностическое устройство, которое выявляет ЧМТ, направляя в глаз безопасный лазер. Устройство, описанное в Наука развивается, предназначен для использования сразу после получения травмы – будь то на обочине дороги, на поле боя или на спортивной площадке – для оценки пациентов на ЧМТ, определения тяжести травмы и соответствующего лечения.
Безопасное для глаз устройство (EyeD) основано на рамановской спектроскопии – оптическом методе, который использует неупругое рассеяние лазерного света для исследования молекулярного состава. Он работает путем воздействия на роговицу лазера класса 635 с длиной волны 1 нм. Коллимированный луч затем фокусируется на сетчатке с помощью собственной оптики глаза. Чтобы направить лазер на интересующую область, система EyeD одновременно выполняет визуализацию глазного дна и спектроскопический анализ с помощью камеры смартфона для визуализации задней части глаза.
Спектры комбинационного рассеяния, собранные с сетчатки и зрительного нерва, анализируются на наличие биохимических изменений, специфичных для ЧМТ, с использованием алгоритма искусственной нейронной сети SKiNET в качестве инструмента поддержки принятия решений. Поскольку сетчатка и зрительный нерв очень тесно связаны с мозгом, изменения биомаркеров после травмы будут отражать биохимические изменения в микроокружении мозга.
«Наше устройство позволит проводить раннюю диагностику ЧМТ путем непосредственной оценки острых дистресс-изменений в режиме реального времени в живой ткани нейроретинального нерва/зрительного нерва. Это позволяет нам опрашивать ткани центральной нервной системы напрямую и неинвазивно», — объясняет руководитель группы. Пола Гольдберг Оппенгеймер. «Анализ нейросетчатки как проекции центральной нервной системы открывает окно в биохимию мозга».
Спектроскопические исследования
Чтобы проверить работу своего устройства визуализации, Оппенгеймер и его коллеги сконструировали тканевый фантом, который имитирует физические размеры и оптические характеристики глаза, обеспечивая при этом реалистичную рамановскую сигнатуру сетчатки. Фантом включает в себя линзу, точечное отверстие диаметром 4 мм, представляющее собой нерасширенный зрачок, и держатель образца ткани сетчатки.
Команда продемонстрировала, что устройство EyeD может эффективно фокусировать лазерный луч в нужном месте на сетчатке. Спектры, измеренные от фантома ткани, разрешили основные полосы комбинационного рассеяния в области высоких волновых чисел, что можно использовать для различения ряда типов тканей.
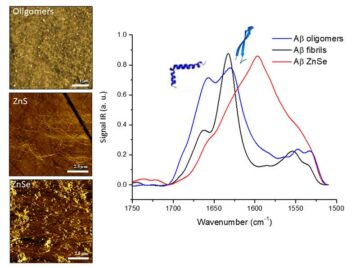
Затем исследователи использовали прототип устройства для анализа образцов сетчатки глаз свиней, которые похожи на человеческие глаза по размеру, структуре, развитию и составу. Они собрали 510 измерений из 39 образцов сетчатки TBI и 12 контрольных образцов, записывая спектры вблизи диска зрительного нерва. В целом в спектрах КР наблюдалось несколько характерных полос в области 1200–1700 см.-1 область отпечатков пальцев, а также усиление полос с высокими волновыми числами в диапазоне 2800–3200 см.-1 область.

Использование SKiNET для создания самооптимизирующихся карт (SOM), показывающих кластеризацию спектров комбинационного рассеяния сетчатки, выявило четкое разделение между сетчаткой с ЧМТ и контрольными образцами. Это происходит потому, что спектры комбинационного рассеяния отражают биохимические изменения в глазу после ЧМТ. Например, ЧМТ увеличивает содержание липидов и белков в глазу, в результате чего возникающие из них пики становятся более выраженными в спектрах комбинационного рассеяния света.
Наиболее значимые спектральные изменения в ответ на ЧМТ были обусловлены вкладом липидов головного мозга кардиолипина и цитохрома С, что проявлялось в увеличении отношения 2930 к 2850 см-XNUMX.-1 пик в спектрах комбинационного рассеяния света. Исследователи использовали отдельные особенности соотношения пиков 2850/2930 и интенсивности шести характерных пиков из спектров ЧМТ, чтобы сформировать классификацию SKiNET, в результате чего получился спектроскопический штрих-код для обнаружения ЧМТ.
Чтобы оценить способность системы EyeD дифференцировать ЧМТ по изменениям сетчатки, они рассчитали площадь под кривой (AUC) для каждого пика и соотношение пиков 2930/2850, а также построили график истинно положительных результатов в сравнении с ложноотрицательными показателями. Использование оптимизации SKiNET с 10-кратной перекрестной проверкой обучающих данных привело к точности классификации 90.7±0.9%. Этот результат указывает на то, что изменения пикового соотношения 2930/2850 после ЧМТ могут стать ценным индикатором для отличия ЧМТ от здоровых людей.
«Использование одновременной рамановской спектроскопии и визуализации глазного дна в виде недорогого портативного устройства открывает первый реальный путь к неинвазивной диагностике ЧМТ на месте», — говорит Оппенгеймер. Мир физики.

При сотрясении мозга глаза — это окна в мозг
Следующим шагом станет оптимизация прототипа для клинической проверки. Чтобы облегчить клинический перевод, исследователи планируют заменить автономный спектрометр компактным спектрометром на устройстве и считыванием данных на смартфоне, что позволит фотографировать глазное дно и рамановскую спектроскопию с помощью одного экрана смартфона.
«В настоящее время мы разрабатываем удобное для пользователя развертываемое устройство, интегрированное с нашим алгоритмом искусственной нейронной сети для автоматической интерпретации результатов без необходимости поддержки специалиста и быстрой классификации спектральных данных», — говорит Оппенгеймер. «[Мы также] клинически оцениваем удобство использования устройства на здоровых добровольцах и пациентах, чтобы продемонстрировать его потенциал для диагностики в реальном времени. После установления переносимости и удобства использования устройства мы приступаем к первой оценке на людях и небольшому клиническому исследованию».
- SEO-контент и PR-распределение. Получите усиление сегодня.
- PlatoData.Network Вертикальный генеративный ИИ. Расширьте возможности себя. Доступ здесь.
- ПлатонАйСтрим. Интеллект Web3. Расширение знаний. Доступ здесь.
- ПлатонЭСГ. Углерод, чистые технологии, Энергия, Окружающая среда, Солнечная, Управление отходами. Доступ здесь.
- ПлатонЗдоровье. Биотехнологии и клинические исследования. Доступ здесь.
- Источник: https://physicsworld.com/a/handheld-device-uses-eye-safe-retinal-spectroscopy-to-diagnose-brain-injury/
- :является
- 1
- 10
- 12
- 39
- 90
- a
- способность
- AC
- соответственно
- точность
- приобретение
- острый
- дополнение
- После
- против
- алгоритм
- позволять
- Позволяющий
- причислены
- скорая помощь
- американские
- an
- анализировать
- анализ
- и
- Применение
- МЫ
- ПЛОЩАДЬ
- около
- прибытие
- искусственный
- AS
- оценить
- Оценка
- At
- Auc
- Автоматизированный
- b
- назад
- основанный
- Battlefield
- BE
- Ширина
- , так как:
- становиться
- между
- биомаркеры
- Бирмингем
- Мозг
- by
- рассчитанный
- камера
- CAN
- вызванный
- Причинение
- центральный
- изменения
- характеристика
- характеристика
- класс
- классификация
- Очистить
- нажмите на
- Клинический
- клинически
- Закрыть
- тесно
- кластеризации
- коллеги
- собранный
- компактный
- композиция
- сама концепция
- Условия
- содержание
- взносы
- контроль
- контрольная
- может
- Создайте
- Компьютерная томография
- В настоящее время
- кривая
- повреждение
- данным
- решение
- решения
- демонстрировать
- убивают
- описано
- Проект
- желанный
- обнаружение
- Определять
- развивающийся
- Развитие
- устройство
- диагностировать
- диагностирование
- диагностика
- диагностический
- Диагностика
- дифференцировать
- трудный
- размеры
- направлять
- непосредственно
- выделить
- бедствие
- два
- каждый
- простота
- фактически
- включить
- позволяет
- позволяет
- Проект и
- усиление
- налаживание
- оценки
- оценка
- пример
- Объясняет
- Глаза
- Глаза
- Особенности
- отпечаток пальца
- Во-первых,
- Фокус
- внимание
- следует
- после
- футбол
- Что касается
- форма
- от
- здоровый
- держатель
- Больница
- Однако
- HTTPS
- человек
- изображение
- Изображениями
- Влияние
- in
- включает в себя
- Увеличение
- Увеличивает
- указывает
- Индикаторные
- информация
- травма
- интегрированный
- интерпретация
- вмешательство
- в
- Исследования
- вопрос
- IT
- ЕГО
- JPG
- лазер
- лидер
- объектив
- легкий
- связанный
- жизнью
- бюджетный
- сделанный
- основной
- проявляется
- Карты
- макс-ширина
- измеренный
- размеры
- молекулярный
- БОЛЕЕ
- самых
- МРТ
- множество
- должен
- сеть
- нервный
- нейронной сети
- неврологический
- следующий
- номер
- наблюдения
- of
- Предложения
- on
- на
- открытый
- оптический
- оптика
- оптимизация
- Оптимизировать
- or
- Возникнув
- наши
- выходы
- общий
- собственный
- в упаковке
- путь
- пациентов
- Вершина горы
- производительность
- выполняет
- фантом
- фотография
- физический
- Физика
- Мир физики
- Pitch
- план
- Платон
- Платон Интеллектуальные данные
- ПлатонДанные
- плюс
- портативный
- должность
- возможное
- потенциал
- присутствие
- предотвращать
- зонд
- Проекция
- выраженный
- свойства
- Белкове продукты
- прототип
- обеспечивать
- приводит
- обеспечение
- быстро
- быстро
- Стоимость
- соотношение
- реальные
- реального времени
- реалистичный
- запись
- отражать
- область
- опираясь
- замещать
- представляющий
- требуется
- исследователи
- решен
- ответ
- результат
- привело
- Сетчатка
- Показали
- безопасный
- говорит
- сканирует
- Наука
- экран
- выбранный
- несколько
- строгость
- показал
- показ
- подпись
- значительный
- аналогичный
- одновременный
- одновременно
- одинарной
- ШЕСТЬ
- Размер
- смартфон
- So
- Скоро
- специалист
- Спектральный
- Спектроскопия
- Спорт
- автономные
- Шаг
- Структура
- такие
- внезапный
- поддержка
- система
- осязаемый
- цель
- целевое
- команда
- техника
- Технологии
- тестXNUMX
- который
- Ассоциация
- Местоположение
- их
- тогда
- Эти
- они
- этой
- Через
- миниатюрами
- время
- своевременно
- туалетная бумага
- в
- переносимость
- инструментом
- к
- Обучение
- Переводы
- лечение
- суд
- правда
- Типы
- под
- на
- us
- юзабилити
- использование
- используемый
- удобно
- использования
- через
- Проверка
- ценный
- изменения
- с помощью
- визуализации
- волонтеры
- we
- были
- будь то
- , которые
- в то время как
- будете
- окно
- окна
- в
- без
- работает
- Мир
- уступая
- зефирнет