细胞培养
棕色脂肪细胞是从 B. Spiegelman(哈佛大学)善意提供的永生化棕色前脂肪细胞小鼠细胞系中分化出来的,如前所述19。 前脂肪细胞在生长培养基(Dulbecco 改良 Eagle 培养基、高葡萄糖 (Gibco)、补充有 50% 胎牛血清 (Sigma-Aldrich)、20 mM HEPES (Sigma-Aldrich))中维持并以低汇合度 (<20%) 扩增。和 100 U 毫升 - 1 青霉素-链霉素 (Gibco))。 为了分化,前脂肪细胞用磷酸盐缓冲溶液 (PBS)(Gibco,pH 7.4,1×)洗涤两次,用 TrypLE Express 解离,并以约 23,000 个细胞 cm-XNUMX 的密度接种 - 2 在生长培养基中。 24小时后将培养基更换为分化培养基(Dulbecco's改良Eagle's培养基,高葡萄糖,补充有10%胎牛血清、20nM胰岛素、1nM三碘甲状腺原氨酸和100Uml - 1 青霉素-链霉素)并将细胞培养 2 天。 然后通过添加诱导培养基(补充有0.125 mM吲哚美辛、0.5 μM地塞米松和0.5 mM异丁基甲基黄嘌呤的分化培养基)诱导细胞分化2天,之后将培养基更换为分化培养基另外两天。 分化的脂肪细胞用饥饿培养基(Dulbecco's改良的Eagle's培养基,低葡萄糖(Gibco),补充葡萄糖至终浓度8mM,0.5%牛血清白蛋白(Sigma-Aldrich)和100Uml洗涤一次。 - 1 青霉素-链霉素)并在饥饿培养基中孵育 2 小时,然后用胰岛素 NanoRods 或在饥饿培养基中稀释的 NanoRods 处理正文中指定的时间。 处理后,将细胞在 PBS 中洗涤一次,并收获细胞以分离用于免疫印迹的蛋白质或用于基因表达的 RNA。 对于通过 DNA-PAINT 进行的 IR 分析,如上所述,通过以下修改来分化前脂肪细胞。 用诱导培养基处理后,用 TrypLE Express 解离细胞并接种到 μ-Slide 18 孔玻璃底孔 (ibidi) 的分化培养基中。 2天后,将细胞与饥饿培养基一起孵育2小时,然后用饥饿培养基中的10nM胰岛素处理10分钟。 在对照实验中,省略了胰岛素的添加。 治疗前,对分化的脂肪细胞进行目视分析,以评估细胞表面密度并评价细胞的分化程度,然后随机分配至治疗组和对照组。
细胞在含有 5% CO 的潮湿气氛中维持、扩增和分化2 37°C。
红外DNA-PAINT
分化的脂肪细胞用预热的 12% 多聚甲醛的 PBS 溶液在室温 (RT) 下固定 4 分钟,用 PBS 洗涤 90 次,用封闭液 (3.0% 胎牛血清/0.1% Triton X) 在室温下封闭 100 分钟-4 PBS 中)并与兔抗 IR β 抗体(Cell Signaling (8B1);在封闭溶液中按 300:2 稀释)在 4 °C 下孵育 1 天。 然后用 PBS 洗涤细胞 200 次,并与在封闭缓冲液 (Massive Photonics) 中以 1:80 稀释的纳米体 FluoTag-XM-QC 抗兔 IgG (Massive Photonics) 一起在室温下孵育 1 小时。 用 PBS 洗涤 5 次后,将细胞与 10 nm 金纳米颗粒(Sigma-Aldrich;在封闭缓冲液中按 5:3 稀释)孵育 XNUMX 分钟。 将细胞用 PBS 洗涤一次,并与在图像缓冲液 (Massive Photonics) 中稀释的 XNUMX nM CyXNUMXb 标记链 (Massive Photonics) 一起孵育。
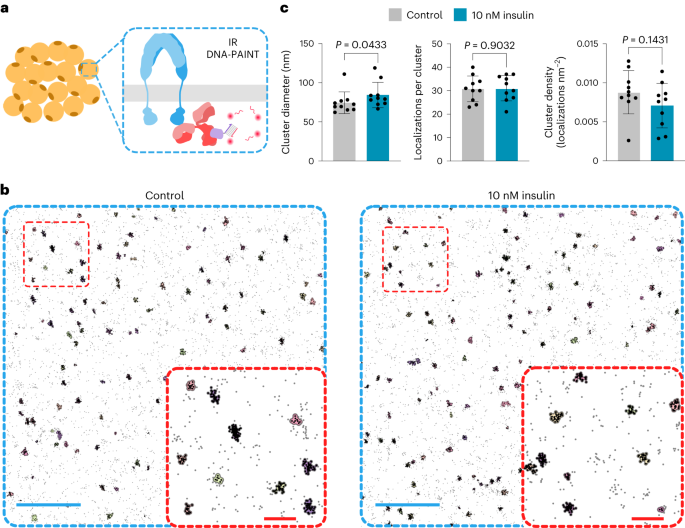
成像在配备 Perfect Focus 系统(Nikon Instruments)的 Nikon ECLIPSE Ti-E 显微镜上进行,采用物镜型全内反射荧光配置,使用带有油浸的 iLAS2 圆形全内反射荧光模块(Gataca Systems) 1.49 数值孔径 CFI Plan Apo 全内反射荧光 ×100 物镜(Nikon Instruments),配备 ×1.5 辅助 Optovar 放大倍率,对应于最终像素尺寸 87 nm。 使用的激光器是 OBIS 561 nm LS 150 mW(相干),具有定制 iLas 输入扩束光学器件 (Cairn),针对缩小视场超分辨率成像进行了优化。 荧光光束首先穿过滤光片立方体(89901,Chroma Technology),其中包含激发四带滤光片、四带二向色滤光片和四带发射滤光片(ZET405/488/561/640x、ZET405/488/561/640bs 和 ZET405) /488/561/640m,Chroma 技术)。 然后用发射滤光片(ET595/50m,Chroma Technology)对荧光光进行光谱过滤,并在 iXon Ultra 888 电子倍增电荷耦合器件相机(Andor)上成像。 Micro-Manager 软件 v. 1.4 用于采集 12,000 个帧,读出帧为 10 MHz,曝光时间为 130 ms,无电子倍增增益。 在每种条件下对来自三个独立实验的总共十个细胞进行了成像(补充说明 和补充图。 1).
INS-DNA 生产和纯化
胰岛素(默克,1 毫克/毫升 - 1)与二苯并环辛炔-磺基-反应N-羟基琥珀酰亚胺酯(DBCO-磺基-NHS,Click Chemistry Tools;690 µM),溶于 100 mM Na2CO3 在室温下缓冲液(pH 11.5)20 分钟。 然后通过添加 Tris 碱(Sigma-Aldrich,5 mM)猝灭反应 100 分钟。 将溶液用 400 µl 100 mM Na 洗涤 XNUMX 次2CO3 使用带有 0.5 kDa 截留膜 (Merck) 的 Amicon Ultra 3 ml 离心过滤器装置。 在每个洗涤步骤中,柱以 10× 旋转 14,000 分钟g。 最后的洗涤步骤后,将胰岛素-DBCO (690 µM) 与叠氮化物修饰的 DNA(Biomers,35 µM;补充表 3) 在 100 mM Na 中2CO3 并在室温下反应 3 小时。 通过添加NaN猝灭反应3 (Sigma-Aldrich,6.9 mM)。 样品在天然聚丙烯酰胺凝胶(6×TAE 中的 19% 1:1 聚丙烯酰胺,20 分钟,200 V,TAE 电泳缓冲液)上运行,并根据制造商的说明用 SYBR Gold (Thermo Fisher) 染色,以确认 INS- DNA的形成。 使用 ImageQuant LAS 4000 凝胶成像仪进行成像。 胰岛素-DBCO-磺基-NHS 缀合方案经过优化,可促进 ssDNA 寡核苷酸与 B 链的赖氨酸 29(B29 赖氨酸)的结合(与 氨基基团相比) N 胰岛素A链和B链的末端。 B29胺的pKa值高于两者的胺 N 终点(11.2 对比 8.6 和 6.8)。 在高 pH 值下,交联剂的 NHS 基团预计会优先与最基本的胺基反应,即 B29 赖氨酸胺32。 因此,优化pH反应条件以促进单一INS-DNA产物。
INS-DNA 反应混合物通过反相高效液相色谱 C 纯化18 色谱柱(Agilent Poroshell 120 EC-C18)在 Amersham Pharmacia Biotech AKTA Ettan LC 上。 在梯度曲线中使用缓冲液 A(50 mM 三乙胺乙酸盐)和缓冲液 B(90% 乙腈和 10% 缓冲液 A),其中缓冲液 B 的百分比在 30 分钟内从 50% 增加到 20%。 收集级分并在真空浓缩器 (Thermo Scientific SpeedVac Savant DNA 120) 上高温旋转 30 分钟,以除去高效液相色谱缓冲液的挥发性成分。 使用带有 0.5 kDa 截留膜 (Merck) 的 Amicon Ultra 3 ml 离心过滤器单元,通过在 10× 下旋转 14,000 次 XNUMX 分钟,将选定的峰缓冲液交换到 PBS 中g 每次用 400 µl PBS 洗涤。 纯化级分的样品在天然聚丙烯酰胺凝胶上运行并用 SYBR Gold (Thermo Fisher) 染色以可视化纯化的 INS-DNA。 通过三种方法分析每种制剂的缀合物的最终纯度: 将十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(Invitrogen,4-12% Bolt 凝胶)上的银染色条带强度(Pierce 银染色试剂盒)与胰岛素标准品(Merck)进行比较,通过 Qubit ssDNA 检测试剂盒(Qubit 4 荧光计,Invitrogen)比较天然聚丙烯酰胺凝胶电泳上的 SYBR Gold 带强度与 DNA 标准品(Integrated DNA Technologies)的比较。 INS-DNA 的最终浓度是根据 Qubit ssDNA 测量值计算的。 纯化的 INS-DNA 冷冻并保存在 -20 °C 直至进一步使用。
纳米棒和胰岛素纳米棒的生产
通过将支架质粒 DNA(p7560,Tilibit,10 nM)与适当的主链(Integrated DNA Technologies,100 nM)混合来制备折纸结构(补充表 4–9)在折叠缓冲液中(5.0 mM Tris,pH 8.5 (Sigma-Aldrich)、1.0 mM EDTA (Panreac AppliChem) 和 12.5 mM MgCl2 (西格玛-奥德里奇))。 然后将混合物放入热循环仪(MJ Research PTC-225 梯度热循环仪)中,并通过加热至 80.0 °C 5 分钟进行退火,在 60.0 分钟内以每分钟 1.0 °C 的速度冷却至 20 °C,然后缓慢冷却至 20.0 °C。 °C,每分钟 0.5 °C。 使用带有 0.5 kDa 截留膜 (Merck) 的 Amicon Ultra 100 ml 离心过滤装置,以 2× 旋转 14,000 分钟 XNUMX 次,去除多余的订书钉g 每次用 400 µl 折叠缓冲液洗涤。 通过测量 260 nm 处的 DNA 吸光度(Thermo Scientific NanoDrop 2000)来确定纯化结构的浓度。 然后将纯化的 INS-DNA 以 3 倍化学计量过量添加到 NanoRod 结构上可用的延伸链结合位点,并在热循环仪中通过加热至 37.0°C 1 小时、以每分钟 22.0°C 冷却至 0.1°C 进行退火,在 22.0°C 下孵育 14 小时,并以每分钟 4.0°C 的速度冷却至 0.1°C。 使用带有 0.5 kDa 截留膜 (Merck) 的 Amicon Ultra 100 ml 离心过滤器装置去除未结合的 INS-DNA,以 2× 旋转 14,000 次,每次 XNUMX 分钟g 每次用 400 µl PBS + 10 mM MgCl 清洗2。 胰岛素纳米棒储存在 4°C 下直至进一步使用。
琼脂糖凝胶电泳
通过在冰上 4 V 下运行琼脂糖凝胶上的样品 70 小时来分析 NanoRod 结构。凝胶由 2× TBE 缓冲液 (Panreac AppliChem) 中的 0.5% 琼脂糖 (Thermo Scientific TopVision Agarose) 加 10 mM MgCl 组成2 (Sigma-Aldrich) 和 1× SYBR Safe DNA 染色剂 (Invitrogen)。 使用 ImageQuant LAS 4000 凝胶成像仪进行成像。
动态光散射
NanoRod 和胰岛素 NanoRod 样品在 PBS + 10 mM MgCl 中制备2,使用 0.1 µm 膜(Merck)过滤注射器并在 Zetasizer Ultra 仪器(Malvern Panalytical)上进行分析。 在 25 °C 下在低容量池 (ZSU1002) 中进行三次测量,然后取平均值。
NanoRod 的 oxDNA 模拟
使用 oxDNA 粗粒度模型分析 NR、NR-1、NR-2、NR-4、NR-7 和 NR-15 结构(https://oxdna.org/)。 使用 vHelix 创建具有从胰岛素掺入位点延伸的 dsDNA 链的 NanoRod 结构,并使用 tacoxDNA 网站将其转换为 oxDNA 格式(http://tacoxdna.sissa.it/)。 结构已提交给 oxDNA.org Web服务器用于37℃下的模拟,1为盐浓度,1×108 广告的时间步长t 值为 0.0001,并使用默认参数进行初步松弛步骤。 使用 oxView 工具对模拟进行可视化并制作视频(https://oxdna.org/).
负染色 TEM
将纯化的 NanoRods (10 nM) 分配在辉光放电碳支撑铜 TEM 网格(TEM-CF200CU50,Thermo Fisher Scientific)上,并在除去溶液之前孵育 60 秒。 然后用 10 µl 5% w/v 甲酸双氧铀将网格染色 2 秒,随后将其除去。 染色过程重复七次,TEM 网格在成像前风干 30 分钟。 在 Talos 120C G2(120 kV,Ceta-D 探测器)上以 ×92,000 进行近场视图成像。 使用 ImageJ 软件 (v1.53) 处理原始图像。
AFM
NanoRod 结构在云母盘上成像,该云母盘用环氧树脂粘合剂固定在显微镜载玻片的中心,并用 Reprorubber 连接到载玻片的塑料环封闭。 将纳米结构在 TE-Mg 缓冲液(1 mM Tris 碱、5 mM EDTA、1 mM MgCl2,pH 8.0)并将 10 µl 移液至新鲜劈开的云母上。 30 秒后,加入 4 µl 5 mM NiSO4 添加并再孵育4.5分钟。 然后用 1.0 ml 0.1 µm 过滤的 TE-Mg 缓冲液冲洗表面,然后将 1.5 ml 过滤的 TE-Mg 缓冲液添加到云母盘中进行成像。 使用 JPK Instruments NanoWizard 3 Ultra 原子力显微镜在交流模式下使用 Bruker AC40 悬臂在液体中进行成像。
胰岛素 NanoRod 纳米结构的 DNA-PAINT
µ-Slide 18 孔玻璃底孔 (ibidi) 用异丙醇清洗并用 NXNUMX 干燥2。 将孔用 1 mg ml - 1 生物素牛血清白蛋白 (Thermo Fisher) 溶于缓冲液 A(10 mM Tris-HCl、100 mM NaCl 和 0.05% (v/v) Tween 20,pH 8.0),室温 5 分钟,用缓冲液 A 洗涤 0.5 次,并与XNUMX毫克毫升 - 1 中性抗生物素蛋白 (Thermo Fisher) 在缓冲液 A 中室温放置 5 分钟。 然后用缓冲液 A 洗涤孔三次,然后用缓冲液 B(5 mM Tris-HCl、10 mM MgCl2、1 mM EDTA 和 0.05% (v/v) Tween 20(pH 8.0)。 然后,500 pM NanoRods 掺入四个生物素标记的 DNA 链(扩展数据图 XNUMX)。 2a),INS-DNA含有9个核苷酸的PAINT对接序列(DS1;补充表 3),添加到每个孔中5分钟。 用缓冲液 B 清洗孔 1 次。然后,加入 647 nM Atto-1N 成像链(ISXNUMX;补充表 10)在补充有氧清除剂(原儿茶酸(Sigma)、原儿茶酸3,4-双加氧酶(Sigma)和Trolox(Sigma))的缓冲液B中添加到每个孔中。 对于双交换 PAINT,三个对接序列(DS2;补充表 10)被添加到纳米棒的两端。 如前所述制备样品,在每次成像采集之间用缓冲液 B 将孔清洗十次。 每次成像采集均使用不同的 Atto-647N 成像器链(IS1 和 IS2;补充表 10)。 Micro-Manager 软件用于采集 9,000 个帧,读出帧为 10 MHz,曝光时间为 200 ms,无电子倍增增益(补充说明 和补充图。 2 和 3).
SPR
使用 Biacore T200 仪器 (Cytiva) 进行 SPR 实验,并使用 Biacore T200 系统控制软件 v. 2.01 获取数据。 生物素化 ECD-IR (Nordic BioSite) 固定在链霉亲和素传感器芯片 SA (Cytiva) 上。 HBS-P+缓冲液(Cytiva)用作运行缓冲液。 ECD-IR 固定后,引入 15 分钟的稳定时间以达到稳定的基线。 NR-1、NR-2、NR-4、NR-7、NR-15、NR-8 和 NR-8dsDNA 在运行缓冲液中以 11.4 nM 胰岛素浓度注射。 胰岛素和 INS-DNA 以 55 nM 注射,这是获得可分析结合曲线的最低浓度。 NR 注射作为阴性对照,其浓度等于胰岛素 NanoRod 注射中使用的 NanoRod 最高浓度 (NR-1 = 11.4 nM)。 或者,以 2 nM 纳米结构浓度注入 NR-4、NR-7、NR-15 和 NR-5.7(扩展数据图 XNUMX)。 4e)和NR-7聚乙二醇 还注射了 50 nM 浓度的胰岛素(扩展数据图 XNUMX)。 9c)。 每个样品的注射使用 180 秒的结合阶段和 300 秒的解离阶段进行。 解离平衡常数 (KD), 关联速率常数 (kon)和解离速率常数(k折扣)使用BIAevaluation 3.0软件测定。 这 t1/2 定义停留时间的值使用公式 ln2/ 确定k折扣。 为了比较 IR 和 IGF7R 之间 NR-1 结构的结合,根据制造商的说明,通过胺偶联反应将 ECD-IR 和 ECD-IGF1R 蛋白 (Nordic BioSite) 固定在 CM5 传感器芯片的两个不同流动池上。 通过在单循环动力学模式下在运行缓冲液 (HBS-P+) 中注射不同浓度的胰岛素(6.2、18.5、55.6、166.7 和 500.0 nM)来测试胰岛素和 INS-DNA 的结合,使用140秒和300秒的解离阶段。 通过注射单一浓度的结构(7 nM 胰岛素),使用 11.4 秒的缔合相和 180 秒的解离相来测试 NR-300 的结合。
考马斯凝胶
这里将 0.5 µg 重组 ECD-IR (Nordic BioSite) 重悬于 Laemmli 样品缓冲液 (Bio-Rad) 中。 对于还原条件,添加2-巯基乙醇至终浓度为2.5%。 样品在 80°C 下变性 10 分钟,通过十二烷基硫酸钠-聚丙烯酰胺凝胶电泳进行解析,并用 GelCode Blue 安全蛋白染色剂 (Thermo Fisher Scientific) 进行染色。
凝胶位移测定
将 7 nM 的 NanoRods(NR 和 NR-20)与 300 nM 人 IR (Nordic BioSite) 重组细胞外结构域或 PBS 在 30 °C 下孵育 4 分钟。 然后将样品在 2% 琼脂糖凝胶上电泳并用 SYBR Safe 染色。
免疫印迹
用PBS洗涤细胞,在补充有蛋白酶和磷酸酶抑制剂混合物(Thermo Fisher Scientific)的放射免疫沉淀测定缓冲液(Sigma-Aldrich)中裂解,并在冰上摇动孵育30分钟。 裂解液通过离心(20,000×g 20°C 4 分钟)并使用 Bradford 蛋白质测定(Bio-Rad)对蛋白质裂解物进行定量。 将蛋白质裂解物重悬于含有 2.5% 2-巯基乙醇的 Laemmli 样品缓冲液 (Bio-Rad) 中,在 80°C 下变性 10 分钟,通过十二烷基硫酸钠-聚丙烯酰胺凝胶电泳进行解析,并转移到聚偏二氟乙烯膜上。 将膜在封闭溶液(含有 1% Tween 0.1 (TBST) 和 20% 脱脂奶粉的 Tris 缓冲盐水)中孵育 5.0 小时,然后与针对磷酸-IR beta/IGF4R 的一抗在 1°C 下孵育过夜beta (CST 3024, 1:1,000)、磷酸-AKT-S473 (CST 4058, 1:1,000) 或 GAPDH (Invitrogen PA1-987, 1:5,000)。 用 TBST 洗涤 31460 次后,将膜与辣根过氧化物酶缀合的二抗(Invitrogen,1,5,000:1)在室温下孵育 XNUMX 小时。 辣根过氧化物酶的检测通过 ChemiDoc 成像系统 (Bio-Rad) 上的化学发光底物 Immobilon Forte 进行。 使用 ImageJ 软件进行带密度测定。
流式细胞术
如上所述制备分化的、血清饥饿的脂肪细胞。 随后用 Hanks 平衡盐溶液 (HBSS) 洗涤脂肪细胞两次,并在胶原酶 D 溶液(1.5 U ml - 1 胶原酶 D (Roche) 和 10 mM CaCl2 在 HBSS 中)20°C 37 分钟。 将细胞重悬于 HBSS 中,通过 35 µm HBSS 平衡细胞滤网 (BD Biosciences) 过滤,在 300× 下沉淀g 5 分钟并重悬于染色缓冲液(1×PBS 和 1% 牛血清白蛋白)中。 根据制造商的说明,用 LIVE/DEAD 可固定黄色死细胞染色试剂盒 (Thermo Fisher Scientific) 标记死细胞,随后将细胞悬浮液在 300× 下沉淀。g 5 分钟并重悬于染色缓冲液中。 这里,约 100,000 个细胞与最终体积 10 µl 的 647 nM ATTO-100 标记的 NanoRod 结构在 10 °C 下孵育 37 分钟。 将没有 NanoRod 结构孵育的细胞用作未处理的对照。 然后用染色缓冲液以300×离心洗涤细胞两次g 5分钟。 使用 BD FACSDIVA 软件 v. 9.0 (BD Biosciences) 在 BD FACSCANTO II 上进行流式细胞术测量。 活脂肪细胞最初通过在 FSC-A 与 AmCyan-A 上门控细胞来鉴定,然后在 FSC-A 与 FSC-H 上门控以检测单峰。 使用FlowJo 10.7.1软件(BD Biosciences)分析获得的数据。 使用未处理对照归一化后荧光强度的几何平均值来定义 NanoRods 的细胞标记程度。
RNA-seq文库制备和测序
使用 Quick-RNA Microprep Plus Kit (Zymo Research) 从分化的脂肪细胞中分离总 RNA,并根据制造商的低样品方案,使用 TruSeq RNA Library Prep Kit v500 使用 2 ng 纯化的 RNA 进行 mRNA-seq 文库制备。 根据制造商的多孔板方案,使用 QuantiFluor dsDNA 系统 (Promega) 在 Varioskan LUX 多模式酶标仪 (Thermo Fisher) 上进行文库定量。 使用 Bioanalysisr 2100 和高灵敏度 DNA 试剂盒(安捷伦)评估文库大小和质量。 使用 NextSeq 标准标准化方案 (Illumina) 对文库进行变性和稀释,并使用单端读数 (1 × 75 bp) 和 NextSeq 500/550 High Output Kit v. 2.5(75 个循环)在 NextSeq 550 平台上进行测序(照明)。
RNA-seq 定量、DEG 分析和 GSEA
测序读数被映射到参考转录组 Mus musculus 蛋白质编码转录序列(释放M29、GRCm39; https://www.gencodegenes.org/mouse/)并使用 Salmon 1.7.0 进行量化(参考文献 XNUMX)。 33)。 使用 tximport 包生成计数表34 并使用 DESeq2 软件包获得 DEG 列表(v. 1.34.0)35,其中只有经过调整的基因 P 等于或低于 0.001 的值和一个日志2倍数变化截止值±0.58被考虑用于进一步分析。 热图和 UpSet 图是使用 ComplexHeatmap (v. 2.10.0) 生成的36。 使用基因排序列表作为 clusterProfiler 的输入,对具有基因本体术语和 KEGG 路径的生物过程进行 GSEA (v. 4.2.2)37 以及错误发现率调整后的重要性 P 值分别低于 0.10 和 0.05。
斑马鱼显微注射和游离葡萄糖定量
NanoRod 和胰岛素 NanoRods 与寡聚赖氨酸-PEG (K10-聚乙二醇5K, Alamanda Polymers),K 中赖氨酸胺之间的比例为 1:110-聚乙二醇5K 以及DNA中的磷酸盐30,并在室温下孵育 30 分钟,然后将 2 nl 样品显微注射到每个斑马鱼幼虫中。 对于涂覆的 NanoRod 样品,制备的注射样品的结构终浓度为 100 nM;对于涂覆的胰岛素 NanoRod 样品,制备的胰岛素的终浓度为 100 nM(对应于 NR-100.0 的 NanoRods 14.3 和 1 nM)聚乙二醇 和NR-7聚乙二醇, 分别)。 在斑马鱼幼虫中注射 1 nl 浓度为 100 nM 的人胰岛素已被证明可诱导游离葡萄糖水平降低以及与胰岛素信号传导一致的转录变化38。 因此,我们在我们的测定中注射了 2 nl 100 nM 胰岛素浓度,以评估胰岛素介导的对游离葡萄糖水平的影响。 由于 2 dpf 斑马鱼的总血容量为 60–89 nl(参考文献 XNUMX)。 39),在我们的测定中注射胰岛素的估计浓度约为 2-3 nM。 在这些测定中,我们还限制了注射样品的量,较高的注射水平(3 和 4 nl)导致幼虫存活率较差。
斑马鱼的维持和杂交(斑马鱼)生产线是按照斯德哥尔摩 djurförsöksetiska nämnd 批准的瑞典动物福利法规进行的。 由于 β 细胞消融和游离葡萄糖测定实验仅使用 5 天以下的动物,因此根据 2010/63/EU,不需要道德许可。 使用的斑马鱼转基因品系之前已被描述过,即, Tg(插件:CFP–NTR)s892 (参考文献。 27) 以及 Tg(插件:枫)s949 (参考文献。 28).
β细胞消融是在两天龄 Tg(插件:CFP–NTR) 以及 Tg(插件:CFP–NTR);Tg(插件:枫)胚胎用 10 mM MTZ (Sigma-Aldrich) 稀释在 1% DMSO (VWR) 中的蛋水溶液 (E3) 中,并补充有 0.2 mM 1-苯基-2-硫脲(PTU,Acros Organics)处理 24 小时。 β细胞消融后,三天大 Tg(插件:CFP–NTR) 幼虫 (72 hpf) 用 0.01% 三卡因麻醉,然后将 2 nl 1× PBS、未修饰的胰岛素或包被的 NanoRod/胰岛素 NanoRods 注射到主静脉(居维叶管)中40。 将最终浓度为 0.1% 的酚红 (Sigma-Aldrich) 添加到 PBS、胰岛素或包被胰岛素 NanoRod 样品中,以帮助显微注射过程的可视化和成功注射幼虫的确定。 斑马鱼幼虫被随机分配到治疗组。 如其他地方所述测量游离葡萄糖水平41 使用基于荧光的酶试剂盒(BioVision)。 每个条件/重复使用三到六只注射幼虫的组。
共焦成像
Tg(插件:CFP–NTR);Tg(插件:枫) 消融处理后 24 小时收集消融幼虫,按照先前规定的方案进行麻醉和注射,并在通过共焦成像分析 β 细胞数量之前固定在 4% 多聚甲醛溶液中。 使用 Leica TCS SP8 显微镜和 LAS X 软件(v. 3.5.5.19976)获取共焦图像。 β细胞消融的初级胰岛 Tg(插件:CFP–NTR);Tg(插件:枫)用×40水浸物镜扫描幼虫, z 使用斐济软件(v1.53)对堆栈进行分析。 所有显示的图像都是从同一实验中获取的,并且为了可视化目的调整了它们的对比度值。 β细胞的定量是在原始未修改的图像上进行的。
统计分析
没有使用统计方法来预先确定样本量,但样本量与之前出版物中报道的相似28,38,42。 细胞培养样品和动物被随机分配到对照组和治疗组。 数据收集和分析并不是在不考虑实验条件的情况下进行的。 大多数图表都绘制了单独的数据点。 样本量(n)的实验生物重复次数和所使用的统计方法在相应的图例中指出。 对数据集进行高斯分布测试,然后进行适当的统计测试。 使用 GraphPad Prism 9.4.0 处理数据的统计分析和图形表示。 进行双尾曼-惠特尼检验来比较对照细胞和胰岛素处理细胞之间的簇特性。 对于蛋白质印迹定量,进行单向方差分析(ANOVA),然后进行 Dunnett 多重比较检验。 为了对 β 细胞进行定量,进行了 Kruskal-Wallis 检验和 Dunn 多重比较检验。 使用单向方差分析和 Tukey 多重比较检验进行游离葡萄糖值的分析。
报告摘要
有关研究设计的更多信息,请参阅 自然投资组合报告摘要 链接到这篇文章。
- :具有
- :是
- :不是
- :在哪里
- ][p
- 000
- 001
- 01
- 1
- 1:1比
- 10
- 100
- 11
- 12
- 125
- 13
- 14
- 15%
- 150
- 180
- 19
- 2%
- 20
- 200
- 2000
- 2006
- 2011
- 2012
- 2014
- 2015
- 2016
- 2017
- 2020
- 2021
- 2022
- 22
- 23
- 24
- 25
- 26
- 27
- 28
- 30
- 300
- 32
- 33
- 35%
- 36
- 39
- 40
- 400
- 41
- 50
- 500
- 58
- 60
- 7
- 70
- 72
- 75
- 8
- 80
- 87
- 9
- 90
- a
- 美国广播公司
- 以上
- 根据
- 获得
- 后天
- 获得
- 操作
- 活化
- 添加
- 添加
- 增加
- 额外
- 调整
- 后
- 驳
- 援助
- 加拿大航空
- AL
- 所有类型
- 分配
- 还
- 量
- an
- 分析
- 分析
- 锚
- 和
- 动物
- 动物
- 抗体
- 抗体
- 应用
- 适当
- 批准
- 约
- 保健
- 围绕
- 刊文
- AS
- 评估
- 评估
- 分配
- 社区
- At
- 气氛
- 附
- 可使用
- b
- 均衡
- BAND
- 基地
- 基于
- 底线
- 基本包
- BD
- BE
- 光束
- 很
- before
- 作为
- 如下。
- 好处
- 测试
- 之间
- 捆绑
- 生物技术
- 盲人
- 封锁
- 闭塞
- 血液
- 蓝色
- 博尔特
- 都
- 半身裙/裤
- BP
- 广阔
- 棕色
- 缓冲
- 但是
- by
- 计算
- 相机
- 枢机主教
- 进行
- 细胞
- 细胞
- 中心
- 链
- 链
- 更改
- 变
- 更改
- 化学
- 芯片
- 碎屑
- 点击
- 簇
- 鸡尾酒
- 相干
- 采集
- 柱
- 列
- 相当常见
- 比较器
- 比较
- 相比
- 对照
- 比较
- 补充
- 复杂
- 符合
- 组件
- 由
- 浓度
- 选矿厂
- 流程条件
- 有条件
- 条件
- 进行
- 配置
- 合流
- 考虑
- 一贯
- 常数
- 对比
- 控制
- 转换
- 铜
- 相关
- 相应
- 可以
- 克雷格
- 创建
- 路口
- 文化塑造
- 曲线
- 习俗
- 周期
- data
- 数据点
- 数据集
- 一年中的
- 死
- 减少
- 默认
- 定义
- 学位
- 交付
- 密度
- 描述
- 设计
- 检测
- 检测
- 决心
- 决心
- 开发
- 发展
- 发展的
- 设备
- 不同
- 分化
- 稀
- 稀释
- 分散
- 显示
- 瓦解
- 分配
- 的DNA
- 域
- 完成
- 干
- 动态
- e
- Ë&T
- e3
- 每
- 影响
- 发射
- 结束
- 环境中
- 酶促的
- 等于
- 平衡
- 配备
- 估计
- 估计
- 醚(ETH)
- 伦理
- 评估
- 所有的
- 过剩
- 交换
- 扩大
- 扩张
- 实验
- 试验
- 实验
- 曝光
- 特快
- 表达
- 延长
- 高效率
- 脂肪
- 部分
- 无花果
- 数字
- 过滤
- 最后
- (名字)
- 五
- 固定
- 流
- 流体
- 专注焦点
- 其次
- 以下
- 针对
- 力
- 格式
- 训练
- 公式
- 长处
- 四
- FRAME
- 自由的
- 止
- 冻结
- 功能上
- 进一步
- G2
- Gain增益
- 根
- 产生
- 基因组
- 玻璃
- 黄金
- 图表
- 格
- 团队
- 组的
- 事业发展
- 哈佛
- 哈佛大学
- 有
- 相关信息
- 高
- 高性能
- 更高
- 最高
- HTTP
- HTTPS
- 人
- i
- ICE
- 确定
- ii
- 图片
- 图片
- 同步成像
- 免疫
- 改善
- in
- 结合
- 增加
- 孵化
- 孵化
- 孵化
- 独立
- 表示
- 个人
- 感应
- 感染
- 信息
- 原来
- 输入
- 说明
- 仪器
- 文书
- 集成
- 内部
- 成
- 介绍
- 孤立
- 隔离
- KDA
- 试剂盒
- 标签
- 幼虫
- LAS
- 激光器是如何工作的
- 左
- 传奇
- 立法
- 各级
- 库
- 自学资料库
- 光
- 有限
- Line
- 线
- 友情链接
- 链接
- 液体肥产线
- 清单
- 书单
- 生活
- 爱
- 低
- 制成
- 主要
- 保养
- 地图
- 大规模
- 材料
- 意味着
- 测量
- 测量
- 测量
- 媒体
- 中等
- 默克公司
- 代谢
- 方法
- 方法
- 方法有
- 云母
- 显微镜
- 牛奶
- 分钟
- 最低限度
- 米斯拉
- 混合
- 杂
- 混合
- 搅和
- MJ
- ML
- 时尚
- 造型
- 修改
- 改性
- 模块
- 最先进的
- 老鼠
- MS
- 多
- 亦即
- 纳米技术
- 本地人
- 自然
- 负
- 全新
- NHS
- 没有
- 小说
- 数
- 数字
- 目标
- 获得
- 获得
- of
- on
- 一旦
- 仅由
- 到
- 本体论
- 光学
- 优化
- or
- 有机
- 原版的
- 我们的
- 输出
- 产量
- 超过
- 过夜
- 氧
- 包
- 涂料
- 参数
- 通过
- 途径
- 模式
- PBS
- 为
- 百分
- 演出
- 执行
- 相
- 刺穿
- 像素
- 放置
- 计划
- 塑料
- 平台
- 柏拉图
- 柏拉图数据智能
- 柏拉图数据
- 加
- pm
- 点
- 聚合物
- 贫困
- 个人档案
- 都曾预测
- 初步
- 准备
- 准备
- 以前
- 先前
- 小学
- 程序
- 过程
- 处理
- 过程
- 产品
- 生产
- 本人简介
- 促进
- 促进
- 蛋白质
- 蛋白质
- 协议
- 提供
- 提供
- 目的
- 质量
- 量化
- 量子比特
- R
- 兔
- 排名
- 率
- 比
- 原
- 达到
- 应对
- 反应
- 反应
- 读者
- 红色
- 减少
- 减少
- 参考
- 反射
- 再生
- 法规
- 松弛
- 释放
- 去掉
- 去除
- 删除
- 重复
- 报道
- 报告
- 表示
- 必须
- 研究
- 住所
- 抵制
- 解决
- 回复
- 导致
- 揭示
- 戒指
- RNA
- 罗氏
- Room
- rt
- 运行
- 运行
- s
- SA
- 安全
- 盐
- 同
- .
- 次
- 选
- 可选择的
- 灵敏度
- 序列
- 测序
- 精華
- 服务器
- XNUMX所
- 转移
- 如图
- 西格玛
- 意义
- 白银
- 类似
- 模拟
- 模拟
- 自
- 单
- 网站
- 网站
- SIX
- 尺寸
- 尺寸
- 滑
- 慢慢地
- 小
- 钠
- 软件
- 方案,
- SPR
- 纺
- 稳定
- 堆栈
- 标准
- 标准
- 说
- 统计
- 步
- 步骤
- 存储
- 链
- 结构体
- 结构
- 研究
- 提交
- 后来
- 顺利
- 抑制
- 磁化面
- 生存
- 悬挂
- 瑞典语
- 系统
- 产品
- T
- 表
- 拍摄
- 塔洛斯
- 针对
- 技术
- 专业技术
- 十
- 条款
- test
- 测试
- 文本
- 比
- 这
- 其
- 然后
- 因此
- 热
- 博曼
- Free Introduction
- 那些
- 三
- 通过
- 次
- 时
- 至
- 工具
- 工具
- 合计
- 画
- 成绩单
- 转移
- 治疗
- 海卫一
- 两次
- 二
- 超级
- 单位
- 普遍
- 大学
- 直到
- 使用
- 用过的
- 运用
- v1
- 真空
- 折扣值
- 价值观
- 与
- 通过
- 视频
- 意见
- 可视化
- 想像
- 视觉
- 体内
- 挥发物
- 体积
- W
- 是
- 洗涤
- 水
- we
- 卷筒纸
- Web服务器
- 福利
- 井
- 井
- 为
- 西式
- 这
- 中
- 也完全不需要
- 将
- wu
- X
- 黄色
- 更年轻
- 和风网