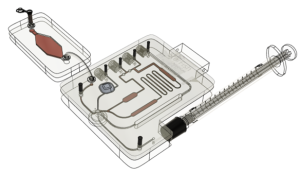
এই নিবন্ধটি মেডিকেল ডিভাইস 510(k) এবং CE চিহ্নিত নিয়ন্ত্রক পথের মধ্যে কিছু মিল এবং পার্থক্য তুলে ধরে এবং সামগ্রিক নিয়ন্ত্রক কৌশলের কিছু দিককে সামঞ্জস্য করতে সাহায্য করে।
সম্পাদকের দ্রষ্টব্য: এই নিবন্ধটি ভিনসেন্ট ক্র্যাবট্রির 2014 ব্লগ 510(k) এবং CE মার্কিং (Pt 1 এবং Pt 2)-এ আপডেট করে এবং প্রতিস্থাপন করে।
FDA-এর 510(k) পথের একটি সুস্পষ্ট সংজ্ঞা রয়েছে যা নির্মাতাদের FDA-এর প্রিমার্কেট অনুমোদন (PMA) পথের তুলনায় দ্রুত গতিতে এবং কম খরচে তাদের পণ্য বাজারে আনতে দেয়। ইউরোপীয় ইউনিয়ন সিই মার্কিং প্রক্রিয়া, যা ডিভাইসটি এফডিএ অনুমোদিত হলে সহজবোধ্য হিসাবে বিবেচিত হয়েছিল, এটি আর একটি তুচ্ছ প্রক্রিয়া নয়। EU-এর MDR (2017/745) এবং IVDR (2017/746) প্রবর্তনের ফলে বেশ কিছু নির্মাতারা তাদের নথিগুলি মেনে চলার জন্য এবং অতিরিক্ত পরীক্ষা বা ক্লিনিকাল অধ্যয়ন পরিচালনার জন্য তাদের নথি আপডেট করার জন্য প্রতিকার প্রোগ্রাম শুরু করেছে।
নির্বাহী সারসংক্ষেপ
মেডিক্যাল ডিভাইস নির্দেশিকা (MDD) EU-তে মেডিকেল ডিভাইস রেগুলেশনস (MDR) পরিবর্তনের মধ্যে রয়েছে যা চিকিৎসা ডিভাইসগুলিকে ক্লাস I, Is, Im, Ir, IIa, IIb, III এবং IIIc (কাস্টম) এ পুনরায় শ্রেণীবদ্ধ করে। ডিভাইসের শ্রেণিবিন্যাস ডিজাইন, পরীক্ষা, যাচাইকরণ, বৈধতা, ক্লিনিকাল এবং পরবর্তী বাজার নজরদারি ডিভাইসটিকে CE চিহ্নিত এবং EU মার্কেটে স্থাপন করার প্রয়োজনীয়তা নির্দেশ করে।
510(k) প্রক্রিয়া এবং CE চিহ্নিতকরণ প্রক্রিয়া এক-এক ভিত্তিতে তুলনা করা যায় না কারণ 510(k) প্রক্রিয়াটি সিই চিহ্নিতকরণ প্রক্রিয়ার প্রযোজ্যতার তুলনায় তুলনামূলকভাবে অল্প সংখ্যক পণ্যের ক্ষেত্রে প্রযোজ্য। ডিভাইসে উল্লেখযোগ্য পরিবর্তনের জন্য উভয় প্রক্রিয়ায় কিছু স্তরের নিরীক্ষণ এবং প্রতিবেদনের প্রয়োজন হয় এবং এর ফলে একটি নতুন 510(k) বা বিজ্ঞপ্তি সংস্থাগুলির দ্বারা পুনরায় পরিদর্শনের প্রয়োজন হতে পারে।
510(k) প্রক্রিয়াটি eSTAR প্রোগ্রাম এবং অগ্রগতি ট্র্যাকিং কার্যকারিতার সাথে সহজবোধ্য হতে বিকশিত হয়েছে। দ্য eSTAR প্রোগ্রাম বর্তমানে একটি যৌথ এফডিএ এবং হেলথ কানাডা পোর্টালের জন্য পাইলট করা হচ্ছে, যা নির্মাতাদের জন্য প্রক্রিয়াটিকে আরও সুবিধাজনক করে তুলবে। EUDAMED বর্তমানে নির্মাণাধীন এবং একটি পূর্ণাঙ্গ কার্যব্যবস্থা 3 সালের Q2024 এ উপলব্ধ হবে বলে আশা করা হচ্ছে।
510(k) এবং CE মার্কিং উভয় প্রক্রিয়াই গুণমান ব্যবস্থাপনা সিস্টেমের জন্য বিভিন্ন প্রবিধানের সেটের অধীনে কাজ করে, কিন্তু ISO 13485:2016 FDA এবং EU MDR ধারাগুলির অতিরিক্ত বাস্তবায়নের সাথে নিযুক্ত করা যেতে পারে। আইএসও 13485:2016 এর সাথে QSR সামঞ্জস্য করার প্রস্তাবের সাথে, একটি গুণমান ব্যবস্থাপনা সিস্টেম বাস্তবায়ন করা নির্মাতাদের জন্য সহজ হয়ে উঠবে। মূল নকশা এবং ঝুঁকি ব্যবস্থাপনা ডকুমেন্টেশন জমা দেওয়ার জন্য প্রয়োজন, এবং পরিপূরক ডকুমেন্টেশন বাজারের উপর ভিত্তি করে পরিবর্তিত হয়।
পরিভাষা, সমতা এবং প্রয়োগ
510(k) হল এফডিএ-তে একটি প্রি-মার্কেট জমা দেওয়া হল যেটি প্রদর্শন করার জন্য যে ডিভাইসটি বাজারজাত করা হবে ততটাই নিরাপদ এবং কার্যকর, অর্থাৎ যথেষ্ট পরিমাণে সমতুল্য (SE), একটি আইনত বিপণন করা ডিভাইস হিসাবে। এফডিএ আইনত বিপণন করা ডিভাইস(গুলি) সংজ্ঞায়িত করে যার সমতুল্যকে "প্রেডিকেট" হিসাবে টানা হয়। একটি ডিভাইস যথেষ্ট পরিমাণে একটি predicate এর সমতুল্য যদি বিষয় ডিভাইস:
- ভবিষ্যদ্বাণী হিসাবে একই উদ্দেশ্যযুক্ত ব্যবহার রয়েছে এবং একই প্রযুক্তিগত বৈশিষ্ট্য বা বিভিন্ন প্রযুক্তিগত বৈশিষ্ট্য রয়েছে যা সুরক্ষা এবং কার্যকারিতার বিভিন্ন প্রশ্ন উত্থাপন করে না।
- এফডিএ-তে জমা দেওয়া তথ্য প্রমাণ করে যে ডিভাইসটি বৈধভাবে বাজারজাত করা ডিভাইসের মতোই (বা তার বেশি) নিরাপদ এবং কার্যকর।
চিত্র 1 দেখুন: 510(k) জমা দেওয়ার জন্য FDA-এর অধীনে উল্লেখযোগ্য সমতা।
510(k) জমা দেওয়া ক্লাস I, II ডিভাইসের জন্য প্রযোজ্য (ছাড় না হলে) এবং ক্লাস III ডিভাইসে, যদি প্রযোজ্য হয়।
যদিও ইউরোপীয় ইউনিয়নের প্রতিটি দেশে, সাধারণত সদস্য রাষ্ট্র হিসাবে উল্লেখ করা হয়, একটি উপযুক্ত কর্তৃপক্ষ রয়েছে যা সিই মার্কিং নির্দেশাবলীর সাথে সম্পর্কিত ডিভাইসের সাথে সম্মতির জন্য দায়ী, সিই চিহ্নিতকরণের দায়িত্বটি নোটিফাইড বডিকে অর্পণ করা হয়, স্বার্থের সংঘাত রোধ করার জন্য, এবং প্রয়োজনীয়তা সামঞ্জস্যপূর্ণ।
ডিভাইসের জন্য একটি সিই মার্ক পেতে, প্রস্তুতকারককে দেখাতে হবে যে তাদের ডিভাইসটি EU MDR প্রয়োজনীয়তা মেনে চলছে। সাধারণত, ডিভাইসের জন্য সিই মার্কিং অনুমোদন করার জন্য ডিভাইস মাস্টার রেকর্ড এবং সংশ্লিষ্ট নথিগুলি পর্যালোচনা করার জন্য নোটিফাইড সংস্থাগুলিকে দায়িত্ব দেওয়া হয়। সম্মতি প্রদর্শনের একটি উপায় হল সমতুলতার মাধ্যমে। ইইউ এমডিআর-এর অধীনে সমতা দাবি করে সিই মার্কিং, সমতা প্রদর্শনের জন্য অতিরিক্ত বিবেচনার প্রয়োজন। প্রস্তুতকারকের নিম্নলিখিত বৈশিষ্ট্যগুলির জন্য সমতা দাবি করতে হবে:
- প্রযুক্তিগত - ব্যবহারের শর্ত, স্পেসিফিকেশন এবং বৈশিষ্ট্য, স্থাপনার পদ্ধতি (যেখানে প্রযোজ্য), অপারেশনের নীতি এবং সমালোচনামূলক কর্মক্ষমতা প্রয়োজনীয়তা
- জৈবিক - একই মানব টিস্যু বা শরীরের তরলগুলির সংস্পর্শে থাকা পদার্থ বা পদার্থ, একই ধরণের এবং যোগাযোগের সময়কাল এবং পদার্থের মুক্তির বৈশিষ্ট্য (অবক্ষয় পণ্য এবং লিচেবল সহ)
- ক্লিনিকাল - ক্লিনিকাল অবস্থা বা উদ্দেশ্য, রোগের তীব্রতা এবং পর্যায়, শরীরের সাইট, জনসংখ্যা, ব্যবহারকারী, একটি নির্দিষ্ট উদ্দেশ্যের জন্য প্রত্যাশিত ক্লিনিকাল প্রভাবের পরিপ্রেক্ষিতে সমালোচনামূলক কর্মক্ষমতা।
CE চিহ্নিতকরণের অধীনে সমতা প্রদর্শনের জন্য অনেক বেশি প্রচেষ্টার প্রয়োজন এবং কখনও কখনও মালিকানা সংক্রান্ত তথ্য যা একটি ভিন্ন নির্মাতার পণ্যের সাথে সমতা দাবি করার চেষ্টা করার জন্য উপলব্ধ নাও হতে পারে। EU MDR-এর অধীনে ক্লাস I-এর জন্য CE চিহ্নিতকরণের জন্য বিজ্ঞাপিত সংস্থার অনুমোদনের প্রয়োজন নেই। ক্লাস I ডিভাইসগুলি EU MDR এর অধীনে স্ব-প্রত্যয়িত। ক্লাস I ডিভাইসগুলি যেগুলি জীবাণুমুক্ত (Is), একটি পরিমাপ ফাংশন (Im) বা পুনঃব্যবহারযোগ্য অস্ত্রোপচার যন্ত্র (Ir) হিসাবে সরবরাহ করা হয় সেগুলি সিই মার্কিং সাপেক্ষে।
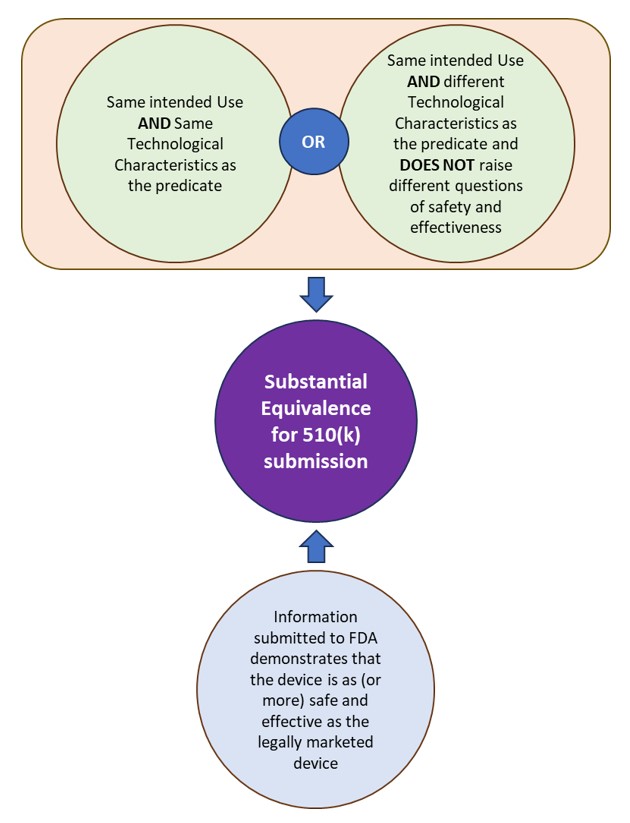
চিত্র 1: 510(k) জমা দেওয়ার জন্য FDA-এর অধীনে উল্লেখযোগ্য সমতা।
ডিভাইসে পরিবর্তন
ডিজাইন পরিবর্তনের মধ্য দিয়ে যে ডিভাইসগুলির জন্য একটি নতুন 510(k) জমা দেওয়ার প্রয়োজন হতে পারে৷ নিম্নলিখিত ক্ষেত্রে একটি নতুন 510(k) জমা দিতে হবে:
- একটি ডিভাইসের নিরাপত্তা বা কার্যকারিতা উল্লেখযোগ্যভাবে প্রভাবিত করার অভিপ্রায়ে করা পরিবর্তনগুলি।
- প্রধান লেবেলিং পরিবর্তন - দ্বন্দ্ব যোগ করা, ডিভাইসগুলিকে একক ব্যবহার থেকে পুনরায় ব্যবহারযোগ্য হিসাবে পুনরায় লেবেল করা ইত্যাদি।
- প্রধান প্রযুক্তি, প্রকৌশল, এবং কর্মক্ষমতা পরিবর্তন - নিয়ন্ত্রণ ব্যবস্থার পরিবর্তন, অপারেটিং নীতি, শক্তির ধরন পরিবর্তন ইত্যাদি।
- উপকরণ পরিবর্তন
- পরিবর্তনগুলি ডিভাইসের ঝুঁকি প্রোফাইলে উল্লেখযোগ্য পরিবর্তনের দিকে পরিচালিত করে৷
যদিও উপরের তালিকাটি সহজবোধ্য বলে মনে হচ্ছে, সেখানে বেশ কয়েকটি পরিস্থিতি রয়েছে যেখানে লাইনগুলি ঝাপসা হয়ে যায় এবং ডিভাইসটির জন্য একটি নতুন 510(k) প্রয়োজন নাও হতে পারে। এফডিএ নির্দেশিকা একটি বিদ্যমান ডিভাইসে পরিবর্তনের জন্য কখন 510(k) জমা দিতে হবে তা নির্ধারণ করা একটি নতুন 510(k) জমা দেওয়ার জন্য সিদ্ধান্ত গ্রহণে সহায়তাকারী বিস্তারিত ফ্লোচার্ট প্রদান করে। একটি পৃথক নির্দেশিকা আলোচনা যখন সফ্টওয়্যার পরিবর্তন একটি নতুন 510(k) প্রয়োজন।
EU MDR-এর অধীনে, নিম্নলিখিত এক বা একাধিক বিভাগে কোনো উল্লেখযোগ্য পরিবর্তনের মধ্য দিয়ে ডিভাইসগুলিকে ডিভাইসটিকে প্রত্যয়িত করা বিজ্ঞপ্তি সংস্থার কাছে রিপোর্ট করা উচিত।
- উদ্দিষ্ট উদ্দেশ্য
- নকশা বা কর্মক্ষমতা স্পেসিফিকেশন
- উপাদান বা উপাদান
- জীবাণুমুক্তকরণের উপর প্রভাব সহ নির্বীজন বা প্যাকেজিং নকশা
- সফটওয়্যার
উল্লেখযোগ্য পরিবর্তনের সংজ্ঞা অস্পষ্ট হতে পারে। MDCG নির্দেশিকা EU MDR এর অধীনে উল্লেখযোগ্য পরিবর্তনের উপর অতিরিক্ত তথ্য প্রদান করে। বিজ্ঞাপিত সংস্থা প্রয়োজন অনুসারে প্রস্তুতকারকের QMS বা প্রযুক্তিগত ডকুমেন্টেশন পুনরায় অডিট করার সিদ্ধান্ত নিতে পারে।
একটি ভাল নিয়ন্ত্রক কৌশল উভয়ই এফডিএ এবং ইইউ এমডিআর প্রয়োজনীয়তাগুলিকে অন্তর্ভুক্ত করবে যাতে তারা উভয়ই পূরণ হয়।
প্রক্রিয়া এবং ফি
CDRH পোর্টাল ব্যবহার করে 510(k) জমা অনলাইন করা যেতে পারে। CDRH পোর্টাল নির্মাতাদের eSTAR, একটি ইন্টারেক্টিভ পিডিএফ ফর্ম ব্যবহার করে একটি মেডিকেল ডিভাইস জমা দেওয়ার অনুমতি দেয়। CDRH পোর্টালটি একটি অগ্রগতি ট্র্যাকারও সরবরাহ করে যা জমা দেওয়ার অবস্থা প্রদর্শন করে। পোর্টালটির ফাইলের আকার এবং প্রকারের সাথে কিছু সীমাবদ্ধতা রয়েছে তবে এটি সংবাদদাতাকে সিডিআরএইচ ডকুমেন্ট কন্ট্রোল সেন্টারে (ডিসিসি) বড় আকারের নথি মেল করার অনুমতি দেয়। FDA কোয়ালিটি সিস্টেম (510 CFR 21) পরিদর্শনের জন্য অপেক্ষা করার সময় 820(k) ক্লিয়ারেন্স মঞ্জুর করা যেকোন ডিভাইস অবিলম্বে বাজারে স্থাপন করা যেতে পারে, যা ক্লিয়ারেন্সের পরে হতে পারে।
510(k) এর জন্য আবেদনের খরচ FDA ওয়েবসাইটের অধীনে প্রকাশিত হয়েছে মেডিকেল ডিভাইস ব্যবহারকারী ফি সংশোধনী (MDUFA). স্ট্যান্ডার্ড ব্যবসা এবং ছোট ব্যবসার জন্য ফি পরিবর্তিত হয়। নীচের টেবিলটি ফি কাঠামোর একটি ধারণা প্রদান করে। ফি প্রতি অর্থ বছরে আপডেট করা হয়। প্রতিটি প্রতিষ্ঠানকে বার্ষিক অর্থ প্রদান করতে হয় প্রতিষ্ঠা নিবন্ধন ফি.
সিই মার্কিং প্রক্রিয়ার জন্য CE মার্কের জন্য একটি ডিভাইসের মূল্যায়ন করার আগে নোটিফাইড বডি এবং একটি যোগ্য QMS অডিটের প্রয়োজন হয়। আপনার জন্য কাজ করে এমন ফি, ভ্রমণের ব্যবস্থা এবং দক্ষতার সঠিক সমন্বয়ের উপর ভিত্তি করে আপনার নোটিফাইড বডি বেছে নিন।
EU MDR একটি ইউরোপীয় ডাটাবেস অন মেডিক্যাল ডিভাইস (EUDAMED) ডাটাবেসের ধারণা প্রবর্তন করেছে যা "ইউরোপীয় ইউনিয়নে (ইইউ) উপলব্ধ মেডিকেল ডিভাইসগুলির জীবনচক্রের একটি জীবন্ত ছবি" প্রদানের উদ্দেশ্যে। EUDAMED এর সাথে সম্পর্কিত ছয়টি মডিউল গঠিত হবে: অভিনেতা নিবন্ধন, অনন্য ডিভাইস সনাক্তকরণ (UDI) এবং ডিভাইস নিবন্ধন, বিজ্ঞপ্তি সংস্থা এবং শংসাপত্র, ক্লিনিকাল তদন্ত এবং কর্মক্ষমতা অধ্যয়ন, সতর্কতা এবং বাজার নজরদারি। মার্চ 2024 পর্যন্ত, EUDAMED-এর তিনটি লাইভ মডিউল রয়েছে - অর্থনৈতিক অপারেটর, ডিভাইস এবং শংসাপত্র। চূড়ান্ত তিনটি মডিউল Q3 2024 এ অনলাইনে যাওয়ার জন্য নির্ধারিত হয়েছে।
সিই মার্কিং-এর জন্য জমাগুলি পরিচালনা করার জন্য একটি অনলাইন সিস্টেমের অনুপস্থিতিতে, প্রস্তুতকারককে সার্টিফিকেশনের জন্য প্রয়োজনীয় ডকুমেন্টেশন এবং প্রমাণগুলি ভাগ করার জন্য নোটিফাইড বডি দ্বারা সেট আপ করা পোর্টাল/শেয়ার ফোল্ডার/অন্যান্য পদ্ধতি ব্যবহার করতে হবে। নোটিফাইড বডি বাজারের জন্য ডিভাইসটি প্রত্যয়িত করার আগে EU MDR কোয়ালিটি ম্যানেজমেন্ট সিস্টেম প্রয়োজনীয়তা (অ্যানেক্স IX) এর বিরুদ্ধে একটি QMS অডিট পরিচালনা করে। নোটিফাইড বডি কিউএমএস অডিট এবং টেকনিক্যাল ডকুমেন্টেশন রিভিউ (বা কিছু ক্ষেত্রে স্যাম্পলিং) ছাড়া ডিভাইসগুলিকে CE চিহ্নিত করা যাবে না এবং বাজারে রাখা যাবে না, যদি না ডিভাইসটিকে ক্লাস I শ্রেণীভুক্ত করা হয়।
EU MDR বিজ্ঞপ্তি সংস্থাগুলিকে প্রতিটি কার্যকলাপের জন্য একটি ফ্ল্যাট ফি বা একটি সময়-ভিত্তিক ফি নেওয়ার অনুমতি দেয়। যাইহোক, বিজ্ঞাপিত সংস্থাগুলি চার্জের জন্য কোনও সীমাবদ্ধ নয়। নীচের সারণীটি বিজ্ঞপ্তি সংস্থা এবং তাদের ফিগুলির একটি নমুনা দেখায়৷ ভ্রমণ এবং দক্ষতার জন্য অতিরিক্ত ফি প্রযোজ্য হতে পারে।
গুনগত পরিচালনা পদ্ধতি
প্রস্তুতকারকদের তাদের যথাযথ পরিশ্রম করতে হবে এবং নিশ্চিত করতে হবে যে বাজারে তাদের ডিভাইসগুলি স্থাপন করার আগে উপযুক্ত গুণমান ব্যবস্থাপনা সিস্টেম রয়েছে।
FDA কোয়ালিটি সিস্টেম রেগুলেশনস (QSR) (21 CFR 820) এর অধীনে গুণমান ব্যবস্থাপনা সিস্টেম পরিচালনা করে, যা বাণিজ্যিকভাবে মেডিকেল ডিভাইস বিতরণ করতে ইচ্ছুক নির্মাতাদের ক্ষেত্রে প্রযোজ্য। ISO 13485:2016 মেডিকেল ডিভাইস - কোয়ালিটি ম্যানেজমেন্ট সিস্টেমগুলিকে QSR-এর মধ্যে অন্তর্ভুক্ত করার জন্য একটি নতুন নিয়ম পাস করা হয়েছে যাতে বোর্ড জুড়ে প্রয়োজনীয়তাগুলিকে সামঞ্জস্য করার প্রয়াসে। ISO 13485:2016 বিশ্বজুড়ে অন্যান্য অনেক নিয়ন্ত্রক কর্তৃপক্ষ দ্বারা গুণমান ব্যবস্থাপনা সিস্টেমের মান হিসাবে ব্যবহৃত হয়। যদিও 510(k) ক্লিয়ারেন্সের নমনীয়তা নির্মাতাদের তাদের ডিভাইস বাজারে রাখার অনুমতি দেয়, তারা যে কোনো সময় FDA দ্বারা পরিদর্শন করা হতে পারে। তাই, ডিভাইসটিকে বাজারে আনার আগে একটি কমপ্লায়েন্ট কোয়ালিটি ম্যানেজমেন্ট সিস্টেম রয়েছে তা নিশ্চিত করা নির্মাতার সর্বোত্তম স্বার্থে।
EU MDR এর সাথে, ISO 13485:2016 CE চিহ্নিতকরণের জন্য প্রয়োজনীয় নয়। কোয়ালিটি ম্যানেজমেন্ট সিস্টেমকে অবশ্যই অ্যানেক্স IX-এ উল্লিখিত প্রবিধানগুলি মেনে চলতে হবে। প্রস্তুতকারকদের অবশ্যই বিজ্ঞপ্তি সংস্থার সাথে তাদের গুণমান ব্যবস্থাপনা সিস্টেমের মূল্যায়নের জন্য একটি আবেদন সম্পূর্ণ করতে হবে। কোয়ালিটি ম্যানেজমেন্ট সিস্টেম অডিট ছাড়াও, নোটিফাইড বডি কোয়ালিটি ম্যানেজমেন্ট সিস্টেমের বিরুদ্ধে ডিভাইসগুলির জন্য প্রযুক্তিগত ডকুমেন্টেশন মূল্যায়ন করবে যাতে সার্টিফিকেশনের আগে সমস্ত প্রয়োজনীয়তা পূরণ করা হয়।
কোয়ালিটি ম্যানেজমেন্ট সিস্টেমকে সামঞ্জস্য করার জন্য, সর্বোত্তম অনুশীলন হল একটি ISO 13485:2016 এবং মেডিকেল ডিভাইস সিঙ্গেল অডিট প্রোগ্রাম (MDSAP) সম্মতিমূলক সিস্টেম বাস্তবায়ন করা যাতে FDA, EU MDR, হেলথ কানাডা বা অন্যান্য দেশ যেখানে নির্মাতা ব্যবসা করতে চায় .
ডকুমেন্টেশন
FDA এবং EU MDR ডিভাইসের জন্য একটি নিয়ন্ত্রিত নকশা প্রক্রিয়া প্রয়োজন।
510(k) জমা দেওয়ার জন্য একটি সম্পূর্ণ ডিজাইন হিস্ট্রি ফাইল (DHF) প্রয়োজন যাতে ডিভাইস সিস্টেমের প্রয়োজনীয়তা, আর্কিটেকচার, স্পেসিফিকেশন, যাচাইকরণ এবং ঝুঁকি ব্যবস্থাপনা কার্যক্রমের বৈধতা এবং ডকুমেন্টেশনের বিবরণ থাকে। 510(k) eSTAR প্রোফাইল নির্মাতাদের আবেদনের প্রতিটি বিভাগে সংশ্লিষ্ট নথি সংযুক্ত করতে দেয়। এফডিএ একটি প্রদান করে স্বীকৃতি চেকলিস্ট 510(k) প্রক্রিয়ার সাথে প্রস্তুতকারককে গাইড করতে এবং সঠিক ডকুমেন্টেশন রয়েছে তা নিশ্চিত করতে।
EU MDR-এর জন্য, একটি টেকনিক্যাল ফাইলে DHF ডকুমেন্ট থাকে এবং প্রস্তুতকারককে নিম্নলিখিত অতিরিক্ত চেকলিস্ট প্রদান করতে হয়:
- অ্যানেক্স I-এর অধীনে জেনারেল সেফটি অ্যান্ড পারফরম্যান্স রিকোয়ারমেন্ট (GSPR), পূর্বে MDD-এর অধীনে এসেনশিয়াল রিকোয়ারমেন্ট চেকলিস্ট নামে পরিচিত
- অ্যানেক্স II এর অধীনে স্ট্যান্ডার্ড টেকনিক্যাল ডকুমেন্টেশন (SteD)
- Annex III এর অধীনে পোস্ট-মার্কেট নজরদারি (PMS)
একটি উচ্চ-স্তরের প্রযুক্তিগত নথি সাধারণত বিভিন্ন DHF নথি এবং চেকলিস্ট উল্লেখ করে।
উভয় ক্ষেত্রেই, ISO 14971-এর সাথে সঙ্গতিপূর্ণ একটি সম্পূর্ণ ঝুঁকি ব্যবস্থাপনা ফাইল প্রয়োজন।
তথ্যসূত্র:
- প্রিমার্কেট বিজ্ঞপ্তি 510(k) | এফডিএ
- 510(k) প্রোগ্রাম: প্রিমার্কেট নোটিফিকেশন [510(k)] (fda.gov) এর মধ্যে উল্লেখযোগ্য সমতা মূল্যায়ন
- একটি বিদ্যমান ডিভাইসে পরিবর্তনের জন্য কখন একটি 510(k) জমা দিতে হবে তা নির্ধারণ করা – শিল্প এবং খাদ্য ও ওষুধ প্রশাসন কর্মীদের জন্য নির্দেশিকা (fda.gov)
- একটি বিদ্যমান ডিভাইসে সফ্টওয়্যার পরিবর্তনের জন্য কখন একটি 510(k) জমা দিতে হবে তা নির্ধারণ করা - শিল্প এবং খাদ্য ও ওষুধ প্রশাসন কর্মীদের জন্য খসড়া নির্দেশিকা (fda.gov)
- MDCG 2019-15, ক্লাস I মেডিকেল ডিভাইসের নির্মাতাদের জন্য নির্দেশিকা নোট
- অনলাইনে মেডিকেল ডিভাইস প্রিমার্কেট জমা পাঠান এবং ট্র্যাক করুন: CDRH পোর্টাল | এফডিএ
- EUDAMED ডাটাবেস - EUDAMED (europa.eu)
- মেডিকেল ডিভাইস ব্যবহারকারী ফি সংশোধনী (MDUFA) | এফডিএ
- MDCG 2023-2, স্ট্যান্ডার্ড ফি তালিকা
- কোয়ালিটি সিস্টেম (QS) রেগুলেশন/মেডিকেল ডিভাইস ভালো ম্যানুফ্যাকচারিং প্র্যাকটিস | এফডিএ
- 510(k)s এর জন্য গ্রহণযোগ্যতা চেকলিস্ট | এফডিএ
- eSTAR প্রোগ্রাম | এফডিএ
- এফডিএ হেলথ কানাডা eSTAR (starfishmedical.com)
চিত্র: অ্যাডোব স্টক এবং স্টার ফিশ মেডিকেল
ধ্রুবিতা কৃষ্ণ আ QA/RA বিশেষজ্ঞ স্টারফিশ মেডিকেলে বায়োমেডিকেল ইঞ্জিনিয়ারিংয়ে এমএস ডিগ্রি সহ। তিনি মেডিক্যাল ডিভাইস কোম্পানিতে উত্পাদন, নতুন পণ্য বাস্তবায়ন, সফ্টওয়্যার স্থাপনা, প্রকল্প ব্যবস্থাপনা এবং নিয়ন্ত্রক এলাকায় কাজ করেছেন। ধ্রুবিতা প্রস্তুতকারকের জন্য গুণমান, নিয়ন্ত্রক এবং ক্রমাগত প্রক্রিয়া উন্নতির জন্য নিবেদিত।
- এসইও চালিত বিষয়বস্তু এবং পিআর বিতরণ। আজই পরিবর্ধিত পান।
- PlatoData.Network উল্লম্ব জেনারেটিভ Ai. নিজেকে ক্ষমতায়িত করুন। এখানে প্রবেশ করুন.
- প্লেটোএআইস্ট্রিম। Web3 ইন্টেলিজেন্স। জ্ঞান প্রসারিত. এখানে প্রবেশ করুন.
- প্লেটোইএসজি। কার্বন, ক্লিনটেক, শক্তি, পরিবেশ সৌর, বর্জ্য ব্যবস্থাপনা. এখানে প্রবেশ করুন.
- প্লেটো হেলথ। বায়োটেক এবং ক্লিনিক্যাল ট্রায়াল ইন্টেলিজেন্স। এখানে প্রবেশ করুন.
- উত্স: https://starfishmedical.com/blog/medical-device-510k-ce-marking/
- : আছে
- : হয়
- :না
- :কোথায়
- $ ইউপি
- 1
- 12
- 2%
- 2014
- 2016
- 2024
- 21
- 300
- 32
- 4
- 400
- 420
- 500
- 8
- 820
- a
- উপরে
- দিয়ে
- ক্রিয়াকলাপ
- কার্যকলাপ
- অভিনেতা
- যোগ
- যোগ
- অতিরিক্ত
- অতিরিক্ত তথ্য
- প্রশাসন
- রৌদ্রপক্ব ইষ্টক
- প্রভাবিত
- পর
- বিরুদ্ধে
- সব
- অনুমতি
- এছাড়াও
- সংশোধনী
- an
- এবং
- আত্মসাৎ করা
- বার্ষিক
- কোন
- প্রাসঙ্গিক
- আবেদন
- প্রযোজ্য
- যথাযথ
- অনুমোদন
- অনুমোদন করা
- অনুমোদিত
- স্থাপত্য
- রয়েছি
- এলাকার
- কাছাকাছি
- আয়োজন
- প্রবন্ধ
- AS
- আ
- পরিমাপ করা
- মূল্যায়ন
- সাহায্য
- যুক্ত
- At
- সংযুক্ত
- প্রচেষ্টা
- নিরীক্ষা
- কর্তৃপক্ষ
- কর্তৃত্ব
- সহজলভ্য
- প্রতীক্ষমাণ
- ভিত্তি
- ভিত্তি
- BE
- কারণ
- পরিণত
- হয়েছে
- আগে
- হচ্ছে
- একাত্মতার
- নিচে
- সর্বোত্তম
- মধ্যে
- বায়োমেডিকেল
- ব্লগ
- দাগ
- তক্তা
- লাশ
- শরীর
- উভয়
- আবদ্ধ
- আনা
- ব্যবসায়
- ব্যবসা
- কিন্তু
- by
- CAN
- কানাডা
- না পারেন
- মামলা
- বিভাগ
- শ্রেণীকরণ
- কেন্দ্র
- সার্টিফিকেট
- সাক্ষ্যদান
- প্রত্যয়িত
- পরিবর্তন
- পরিবর্তন
- বৈশিষ্ট্য
- অভিযোগ
- চার্জ
- বেছে নিন
- দাবি
- দাবি
- শ্রেণী
- শ্রেণীবিন্যাস
- পরিষ্কার
- পরিষ্করণ
- রোগশয্যা
- এর COM
- সমাহার
- বাণিজ্যিকভাবে
- কোম্পানি
- তুলনা
- উপযুক্ত
- সম্পূর্ণ
- সম্মতি
- অনুবর্তী
- মেনে চলে
- মেনে চলতে
- স্থিরীকৃত
- ধারণা
- শর্ত
- পরিবেশ
- আবহ
- কর্মের যেসব প্রবণতা
- দ্বন্দ্ব
- বিবেচ্য বিষয়
- নির্মাণ
- যোগাযোগ
- ধারণ
- একটানা
- নিয়ন্ত্রণ
- নিয়ন্ত্রিত
- সুবিধাজনক
- মূল
- মূল্য
- খরচ
- দেশ
- দেশ
- সংকটপূর্ণ
- এখন
- প্রথা
- ডেটাবেস
- সিদ্ধান্ত নেন
- রায়
- সিদ্ধান্ত মেকিং
- নিবেদিত
- সংজ্ঞায়িত
- সংজ্ঞা
- ডিগ্রী
- অর্পণ
- প্রদর্শন
- প্রমান
- প্রদর্শক
- বিস্তৃতি
- নকশা
- নকশা প্রক্রিয়া
- বিশদ
- বিস্তারিত
- যন্ত্র
- ডিভাইস
- পার্থক্য
- বিভিন্ন
- অধ্যবসায়
- নির্দেশনা
- আলোচনা
- রোগ
- প্রদর্শন
- প্রদর্শন
- বিতরণ করা
- do
- দলিল
- ডকুমেন্টেশন
- কাগজপত্র
- সম্পন্ন
- খসড়া
- টানা
- ড্রাগ
- কারণে
- স্থিতিকাল
- e
- প্রতি
- সহজ
- EC
- অর্থনৈতিক
- প্রভাব
- কার্যকর
- কার্যকারিতা
- প্রচেষ্টা
- পারেন
- নিযুক্ত
- শক্তি
- প্রকৌশল
- নিশ্চিত করা
- সমতা
- সমতুল্য
- অপরিহার্য
- সংস্থা
- ইত্যাদি
- থার (eth)
- EU
- ইউরোপা
- ইউরোপিয়ান
- ইওরোপীয় ইউনিয়ন
- মূল্যায়ন
- মূল্যায়নের
- প্রতি
- প্রমান
- বিবর্তিত
- অব্যাহতিপ্রাপ্ত
- বিদ্যমান
- প্রত্যাশিত
- ল্যাপারোস্কোপিক পদ্ধতি
- দ্রুত
- এফডিএ
- পারিশ্রমিক
- ফি
- কয়েক
- ব্যক্তিত্ব
- ফাইল
- চূড়ান্ত
- অভিশংসক
- ফ্ল্যাট
- নমনীয়তা
- অনুসরণ
- খাদ্য
- খাদ্য এবং ঔষধ প্রশাসন
- জন্য
- ফর্ম
- বের
- থেকে
- সম্পূর্ণ
- ক্রিয়া
- কার্যকারিতা
- Go
- ভাল
- শাসন করে
- মঞ্জুর
- পথপ্রদর্শন
- কৌশল
- নির্দেশিকা
- আছে
- স্বাস্থ্য
- সাহায্য
- অত: পর
- গোপন
- উচ্চ
- উচ্চস্তর
- হাইলাইট
- ইতিহাস
- যাহোক
- HTTPS দ্বারা
- মানবীয়
- i
- ধারণা
- শনাক্ত
- if
- ii
- গ
- অবিলম্বে
- প্রভাব
- বাস্তবায়ন
- বাস্তবায়ন
- উন্নতি
- in
- সুদ্ধ
- নিগমবদ্ধ
- শিল্প
- তথ্য
- সূচনা
- যন্ত্র
- অভিপ্রেত
- অভিপ্রায়
- ইচ্ছুক
- অভিপ্রায়
- ইন্টারেক্টিভ
- স্বার্থ
- মধ্যে
- উপস্থাপিত
- ভূমিকা
- তদন্ত
- জড়িত থাকার
- আইএসও
- IT
- যৌথ
- JPG
- রকম
- পরিচিত
- লেবেল
- নেতৃত্ব
- নেতৃত্ব
- বরফ
- আইনত
- উচ্চতা
- জীবনচক্র
- সীমাবদ্ধতা
- সীমা
- লাইন
- তালিকা
- জীবিত
- আর
- অনেক
- নিম্ন
- প্রণীত
- করা
- মেকিং
- পরিচালনা করা
- ব্যবস্থাপনা
- ব্যবস্থাপনা পদ্ধতি
- উত্পাদক
- নির্মাতারা
- উত্পাদন
- অনেক
- মার্চ
- মার্চ 2024
- ছাপ
- চিহ্নিত
- বাজার
- বাজারজাত করা
- অবস্থানসূচক
- মালিক
- উপকরণ
- সর্বোচ্চ প্রস্থ
- মে..
- MDR
- পরিমাপ
- পদ্ধতি
- চিকিৎসা
- চিকিৎসার যন্ত্র
- চিকিত্সা সংক্রান্ত যন্ত্রপাতি
- সদস্য
- মিলিত
- পদ্ধতি
- মডিউল
- পর্যবেক্ষণ
- অধিক
- অবশ্যই
- প্রয়োজন
- প্রয়োজন
- নতুন
- নতুন পণ্য
- না।
- বিঃদ্রঃ
- নোট
- প্রজ্ঞাপন
- বিজ্ঞপ্তি
- সংখ্যা
- প্রাপ্ত
- of
- on
- ONE
- অনলাইন
- পরিচালনা করা
- অপারেটিং
- অপারেশন
- অপারেটরদের
- or
- মূলত
- অন্যান্য
- সামগ্রিক
- গতি
- প্যাকেজিং
- গৃহীত
- পথ
- পথ
- বেতন
- পিডিএফ
- কর্মক্ষমতা
- ছবি
- চালিত
- জায়গা
- স্থাপিত
- স্থাপন
- Plato
- প্লেটো ডেটা ইন্টেলিজেন্স
- প্লেটোডাটা
- খেলোয়াড়
- PMS
- জনসংখ্যা
- পোর্টাল
- পোস্ট
- অনুশীলন
- চর্চা
- প্রতিরোধ
- পূর্বে
- নীতি
- নীতিগুলো
- পূর্বে
- প্রক্রিয়া
- প্রসেস
- পণ্য
- পণ্য
- প্রোফাইল
- কার্যক্রম
- প্রোগ্রাম
- উন্নতি
- প্রকল্প
- প্রকল্প ব্যবস্থাপনা
- বৈশিষ্ট্য
- প্রস্তাব
- মালিকানা
- প্রদান
- প্রদত্ত
- উপলব্ধ
- প্রকাশিত
- উদ্দেশ্য
- Q3
- কোয়ালিফাইং
- গুণ
- প্রশ্ন
- বৃদ্ধি
- নথি
- রেফারেন্স
- উল্লেখ করা
- গণ্য
- নিবন্ধন
- আইন
- নিয়ন্ত্রক
- সংশ্লিষ্ট
- অপেক্ষাকৃতভাবে
- মুক্তি
- উপসম
- প্রতিবেদন
- প্রয়োজন
- প্রয়োজনীয়
- প্রয়োজন
- আবশ্যকতা
- প্রয়োজন
- দায়িত্ব
- দায়ী
- পুনর্ব্যবহারযোগ্য
- এখানে ক্লিক করুন
- পর্যালোচনা
- অধিকার
- ঝুঁকি
- ঝুকি ব্যবস্থাপনা
- নিয়ম
- s
- নিরাপদ
- নিরাপত্তা
- একই
- পরিস্থিতিতে
- তালিকাভুক্ত
- অধ্যায়
- মনে হয়
- পাঠান
- আলাদা
- সেট
- সেট
- বিভিন্ন
- নির্দয়তা
- শেয়ার
- সে
- উচিত
- শো
- গুরুত্বপূর্ণ
- উল্লেখযোগ্যভাবে
- অনুরূপ
- মিল
- সহজ
- একক
- সাইট
- ছয়
- আয়তন
- ছোট
- ছোট ব্যবসা
- সফটওয়্যার
- কিছু
- কখনও কখনও
- নির্দিষ্ট
- স্পেসিফিকেশনের
- দণ্ড
- পর্যায়
- মান
- তারামাছ
- যুক্তরাষ্ট্র
- অবস্থা
- অকপট
- কৌশল
- গঠন
- গবেষণায়
- বিষয়
- নমন
- জমা
- জমা
- পেশ
- জমা
- সারগর্ভ
- যথেষ্ট
- অস্ত্রোপচার
- নজরদারি
- পদ্ধতি
- সিস্টেম
- টেবিল
- গ্রহণ করা
- টাস্কড
- কারিগরী
- প্রযুক্তিক
- প্রযুক্তিঃ
- পরীক্ষামূলক
- যে
- সার্জারির
- বিশ্ব
- তাদের
- সেখানে।
- তারা
- এই
- তিন
- দ্বারা
- সময়
- টিস্যু
- থেকে
- পথ
- যে ব্যক্তি অনুসরণ করে
- অনুসরণকরণ
- রূপান্তর
- ভ্রমণ
- আদর্শ
- ধরনের
- সাধারণত
- অধীনে
- ভুগা
- চলমান
- মিলন
- অনন্য
- যদি না
- আপডেট
- আপডেট
- আপডেট
- ব্যবহার
- ব্যবহৃত
- ব্যবহারকারী
- ব্যবহার
- বৈধতা
- বিভিন্ন
- বিভিন্ন করা
- প্রতিপাদন
- ভিডিও
- চেক
- সতর্ক প্রহরা
- ভিনসেন্ট
- ছিল
- উপায়
- ওয়েবসাইট
- কখন
- যে
- যখন
- ইচ্ছা
- সঙ্গে
- মধ্যে
- ছাড়া
- কাজ করছে
- কাজ
- কাজ
- বিশ্ব
- বছর
- আপনি
- আপনার
- ইউটিউব
- zephyrnet