Dieser Artikel beleuchtet einige der Gemeinsamkeiten und Unterschiede zwischen den Regulierungswegen für Medizinprodukte 510(k) und der CE-Kennzeichnung und trägt dazu bei, einige Aspekte einer gesamten Regulierungsstrategie zu harmonisieren.
Anmerkung des Herausgebers: Dieser Artikel aktualisiert und ersetzt Vincent Crabtrees Blog aus dem Jahr 2014 über 510(k) und CE-Kennzeichnung (Teil 1 und Teil 2).
Die FDA hat eine klare Definition des 510(k)-Pfads, der es Herstellern ermöglicht, ihre Produkte im Vergleich zum Premarket Approval (PMA)-Pfad der FDA schneller und zu geringeren Kosten auf den Markt zu bringen. Der CE-Kennzeichnungsprozess der Europäischen Union, der ursprünglich als unkompliziert galt, wenn das Gerät von der FDA zugelassen wurde, ist kein trivialer Prozess mehr. Die Einführung der MDR (2017/745) und IVDR (2017/746) der EU hat dazu geführt, dass mehrere Hersteller Abhilfeprogramme gestartet haben, um ihre Dokumente auf Konformität zu aktualisieren und zusätzliche Tests oder klinische Studien durchzuführen.
Executive Summary
Die Medizinprodukterichtlinie (MDD) befindet sich in der Übergangsphase zur Medizinprodukteverordnung (MDR) in der EU, die Medizinprodukte in die Klassen I, Is, Im, Ir, IIa, IIb, III und IIIc (kundenspezifisch) neu klassifiziert. Die Geräteklassifizierung legt die Anforderungen an Design, Prüfung, Verifizierung, Validierung, klinische Tests und Überwachung nach dem Inverkehrbringen fest, damit das Gerät die CE-Kennzeichnung erhält und auf den EU-Markt gebracht wird.
Der 510(k)-Prozess und der CE-Kennzeichnungsprozess können nicht eins zu eins verglichen werden, da der 510(k)-Prozess im Vergleich zur Anwendbarkeit des CE-Kennzeichnungsprozesses für eine relativ kleine Anzahl von Produkten gilt. Wesentliche Änderungen an Geräten erfordern ein gewisses Maß an Überwachung und Berichterstattung in beiden Prozessen und können dazu führen, dass ein neues 510(k) oder eine erneute Inspektion durch benannte Stellen erforderlich wird.
Der 510(k)-Prozess hat sich mit dem eSTAR-Programm und der Fortschrittsverfolgungsfunktion zu einem unkomplizierten Verfahren entwickelt. Der Das eSTAR-Programm wird derzeit für ein gemeinsames Portal von FDA und Health Canada getestet, was den Prozess für Hersteller komfortabler machen wird. EUDAMED befindet sich derzeit im Aufbau und ein voll funktionsfähiges System wird voraussichtlich im dritten Quartal 3 verfügbar sein.
Sowohl 510(k)- als auch CE-Kennzeichnungsprozesse unterliegen unterschiedlichen Regelwerken für das Qualitätsmanagementsystem, aber ISO 13485:2016 kann mit zusätzlicher Implementierung von FDA- und EU-MDR-Klauseln angewendet werden. Mit dem Vorschlag, QSR mit ISO 13485:2016 zu harmonisieren, wird die Implementierung eines Qualitätsmanagementsystems für Hersteller einfacher. Für die Einreichung ist eine grundlegende Design- und Risikomanagementdokumentation erforderlich, und die ergänzende Dokumentation variiert je nach Markt.
Terminologie, Äquivalenz und Anwendung
510(k) ist eine vorab bei der FDA eingereichte Einreichung, um nachzuweisen, dass das zu vermarktende Produkt genauso sicher und wirksam, d. h. im Wesentlichen gleichwertig (SE) ist, wie ein legal vermarktetes Produkt. Als „Prädikat“ definiert die FDA das/die legal vermarktete(n) Produkt(e), zu dem/denen die Gleichwertigkeit gezogen wird. Ein Gerät entspricht im Wesentlichen einem Prädikat, wenn das betreffende Gerät:
- hat den gleichen Verwendungszweck wie das Prädikat und weist die gleichen technologischen Merkmale oder unterschiedliche technologische Merkmale auf, die keine unterschiedlichen Fragen der Sicherheit und Wirksamkeit aufwerfen.
- Die an die FDA übermittelten Informationen belegen, dass das Gerät genauso (oder mehr) sicher und wirksam ist wie das legal vermarktete Gerät.
Siehe Abbildung 1: Wesentliche Gleichwertigkeit gemäß FDA für 510(k)-Anträge.
510(k)-Einreichungen gelten für Geräte der Klassen I, II (sofern nicht ausgenommen) und Geräte der Klasse III, sofern zutreffend.
Obwohl jedes Land in der Europäischen Union, in der Regel als Mitgliedstaaten bezeichnet, über eine zuständige Behörde verfügt, die für die Einhaltung der CE-Kennzeichnungsrichtlinien des Geräts verantwortlich ist, wird die Verantwortung für die CE-Kennzeichnung an benannte Stellen delegiert, um Interessenkonflikte zu vermeiden. und Anforderungen harmonisieren.
Um eine CE-Kennzeichnung für das Gerät zu erhalten, muss der Hersteller nachweisen, dass sein Gerät den EU-MDR-Anforderungen entspricht. Typischerweise werden benannte Stellen damit beauftragt, den Gerätestammdatensatz und die zugehörigen Dokumente zu überprüfen, um die CE-Kennzeichnung für das Gerät zu genehmigen. Eine Möglichkeit, Konformität nachzuweisen, ist die Gleichwertigkeit. Die CE-Kennzeichnung erfordert durch die Behauptung der Gleichwertigkeit gemäß der EU-MDR zusätzliche Überlegungen zum Nachweis der Gleichwertigkeit. Der Hersteller ist verpflichtet, die Gleichwertigkeit für folgende Merkmale zu beanspruchen:
- Technisch – Nutzungsbedingungen, Spezifikationen und Eigenschaften, Einsatzmethoden (sofern zutreffend), Betriebsprinzipien und kritische Leistungsanforderungen
- Biologisch – Materialien oder Substanzen, die mit denselben menschlichen Geweben oder Körperflüssigkeiten in Kontakt kommen, ähnliche Art und Dauer des Kontakts und Freisetzungseigenschaften von Substanzen (einschließlich Abbauprodukten und auslaugbaren Stoffen)
- Klinisch – klinischer Zustand oder Zweck, Schweregrad und Stadium der Erkrankung, Körperstelle, Population, Benutzer, kritische Leistung im Hinblick auf die erwartete klinische Wirkung für einen bestimmten beabsichtigten Zweck.
Der Nachweis der Gleichwertigkeit im Rahmen der CE-Kennzeichnung erfordert viel mehr Aufwand und erfordert manchmal proprietäre Informationen, die für den Versuch, die Gleichwertigkeit mit Produkten eines anderen Herstellers geltend zu machen, möglicherweise nicht verfügbar sind. Die Genehmigung einer benannten Stelle für die CE-Kennzeichnung ist für Klasse I gemäß der EU-MDR nicht erforderlich. Geräte der Klasse I sind gemäß EU MDR selbstzertifiziert. Produkte der Klasse I, die steril geliefert werden (Is), eine Messfunktion haben (Im) oder ein wiederverwendbares chirurgisches Instrument sind (Ir), unterliegen der CE-Kennzeichnung.
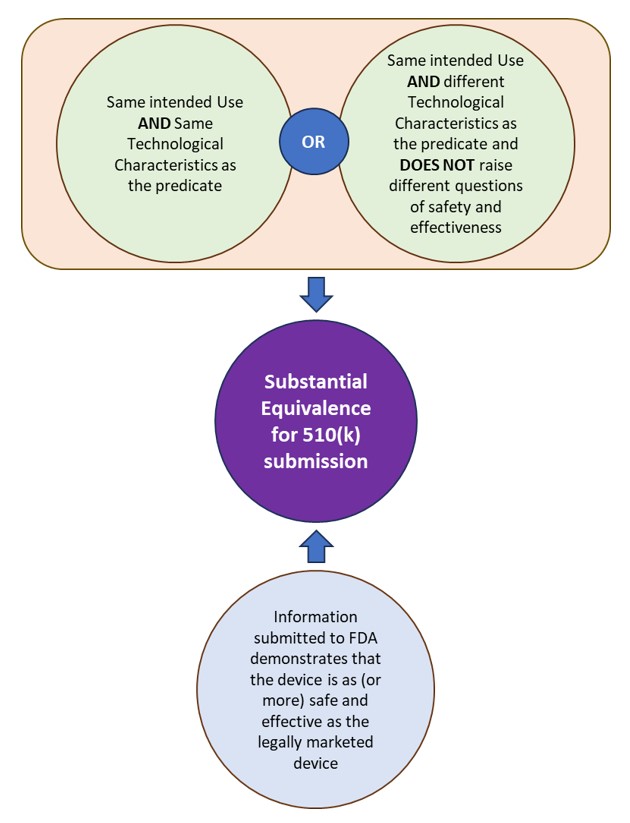
Abbildung 1: Wesentliche Gleichwertigkeit gemäß FDA für 510(k)-Anträge.
Änderungen am Gerät
Geräte, bei denen Designänderungen vorgenommen wurden, erfordern möglicherweise eine neue 510(k)-Einreichung. In den folgenden Fällen sollte ein neuer 510(k) eingereicht werden:
- Änderungen, die mit der Absicht vorgenommen werden, die Sicherheit oder Wirksamkeit eines Geräts erheblich zu beeinträchtigen.
- Wesentliche Änderungen bei der Kennzeichnung – Hinzufügung von Kontraindikationen, Neukennzeichnung von Geräten als wiederverwendbar für den einmaligen Gebrauch usw.
- Wesentliche Technologie-, Konstruktions- und Leistungsänderungen – Änderungen im Steuermechanismus, im Funktionsprinzip, Änderungen der Energieart usw.
- Materialänderungen
- Änderungen, die zu einer erheblichen Änderung des Risikoprofils des Geräts führen.
Während die obige Liste einfach erscheint, gibt es mehrere Szenarien, in denen die Grenzen verschwimmen und das Gerät möglicherweise keinen neuen 510(k) benötigt. Die FDA-Leitlinien Entscheiden, wann ein 510(k) für eine Änderung an einem vorhandenen Gerät eingereicht werden soll Bietet detaillierte Flussdiagramme, die bei der Entscheidungsfindung für die Einreichung eines neuen 510(k) helfen. In einem separaten Leitfaden wird erläutert, wann Änderungen an der Software erfordern ein neues 510(k).
Gemäß der EU-MDR müssen Geräte, bei denen wesentliche Änderungen in einer oder mehreren der folgenden Kategorien vorgenommen werden, die Änderung der benannten Stelle melden, die das Gerät zertifiziert hat.
- beabsichtigter Zweck
- Design- oder Leistungsspezifikation
- Zutat oder Material
- Sterilisation oder Verpackungsdesign mit Auswirkungen auf die Sterilisation
- Software.
Die Definition einer signifikanten Änderung kann mehrdeutig sein. MDCG-Leitfaden bietet zusätzliche Informationen zu wesentlichen Änderungen im Rahmen der EU-MDR. Die benannte Stelle kann bei Bedarf beschließen, das QMS oder die technische Dokumentation des Herstellers erneut zu auditieren.
Eine gute Regulierungsstrategie umfasst sowohl FDA- als auch EU-MDR-Anforderungen, um sicherzustellen, dass beide erfüllt werden.
Verfahren und Gebühren
510(k)-Einreichungen können online über das CDRH-Portal erfolgen. Über das CDRH-Portal können Hersteller mithilfe von eSTAR, einem interaktiven PDF-Formular, eine Einreichung für Medizinprodukte einreichen. Das CDRH-Portal bietet außerdem einen Fortschrittstracker, der den Einreichungsstatus anzeigt. Das Portal weist einige Einschränkungen hinsichtlich der Dateigröße und -typen auf, ermöglicht dem Korrespondenten jedoch, übergroße Dokumente an das CDRH Document Control Center (DCC) zu senden. Jedes Gerät, dem die 510(k)-Freigabe erteilt wurde, kann sofort auf den Markt gebracht werden, während auf die Inspektion des FDA-Qualitätssystems (21 CFR 820) gewartet wird, die möglicherweise nach der Freigabe erfolgt.
Die Antragskosten für 510(k) werden auf der FDA-Website unter veröffentlicht Änderungen der Nutzungsgebühr für medizinische Geräte (MDUFA). Die Gebühren variieren für Standardunternehmen und Kleinunternehmen. Die folgende Tabelle gibt einen Überblick über die Gebührenstruktur. Die Gebühren werden jedes Geschäftsjahr aktualisiert. Jeder Betrieb ist zur Zahlung einer Jahresgebühr verpflichtet Registrierungsgebühr für die Einrichtung.
Der CE-Kennzeichnungsprozess erfordert die Einbeziehung benannter Stellen und ein qualifiziertes QMS-Audit, bevor ein Gerät für eine CE-Kennzeichnung bewertet werden kann. Wählen Sie Ihre Benannte Stelle auf der Grundlage der für Sie geeigneten Kombination aus Gebühren, Reisearrangements und Fachwissen aus.
Mit der EU-MDR wurde das Konzept einer Europäischen Datenbank für Medizinprodukte (EUDAMED) eingeführt, die ein „lebendiges Bild des Lebenszyklus von Medizinprodukten liefern soll, die in der Europäischen Union (EU) verfügbar gemacht werden“. EUDAMED wird aus sechs Modulen bestehen, die sich auf Folgendes beziehen: Akteursregistrierung, eindeutige Geräteidentifikation (UDI) und Geräteregistrierung, benannte Stellen und Zertifikate, klinische Untersuchungen und Leistungsstudien, Vigilanz und Marktüberwachung. Seit März 2024 verfügt EUDAMED über drei Live-Module – Wirtschaftsteilnehmer, Geräte und Zertifikate. Die letzten drei Module sollen im dritten Quartal 3 online gehen.
In Ermangelung eines Online-Systems zur Verwaltung der Einreichungen zur CE-Kennzeichnung ist der Hersteller verpflichtet, von benannten Stellen eingerichtete Portale/Freigabeordner/andere Methoden zu nutzen, um die für die Zertifizierung erforderlichen Unterlagen und Nachweise weiterzugeben. Die benannte Stelle führt vor der Zertifizierung des Geräts für den Markt ein QMS-Audit anhand der Anforderungen des EU-MDR-Qualitätsmanagementsystems (Anhang IX) durch. Geräte können nicht ohne ein QMS-Audit einer benannten Stelle und eine Überprüfung der technischen Dokumentation (oder in manchen Fällen einer Probenahme) eine CE-Kennzeichnung erhalten und auf den Markt gebracht werden, es sei denn, das Gerät ist der Klasse I zugeordnet.
Mit der EU-MDR können benannte Stellen für jede Aktivität entweder eine Pauschalgebühr oder eine zeitabhängige Gebühr erheben. Allerdings sind die Benannten Stellen an keine Höchstgrenzen für die Entgelte gebunden. Die folgende Tabelle zeigt eine Auswahl benannter Stellen und deren Gebühren. Es können zusätzliche Gebühren für Reisen und Fachwissen anfallen.
Quality Management System
Hersteller müssen ihre Sorgfaltspflicht erfüllen und sicherstellen, dass das entsprechende Qualitätsmanagementsystem vorhanden ist, bevor sie ihre Geräte auf den Markt bringen.
Die FDA regelt das Qualitätsmanagementsystem gemäß den Quality System Regulations (QSR) (21 CFR 820), das für Hersteller gilt, die medizinische Geräte kommerziell vertreiben möchten. Es wurde eine neue Regel verabschiedet, um die ISO 13485:2016 Medizinprodukte – Qualitätsmanagementsysteme in das QSR zu integrieren und so die Anforderungen allgemein zu harmonisieren. ISO 13485:2016 wird von vielen anderen Regulierungsbehörden auf der ganzen Welt als Standard für Qualitätsmanagementsysteme verwendet. Während die Flexibilität der 510(k)-Zulassung es Herstellern ermöglicht, ihre Geräte auf den Markt zu bringen, können sie jederzeit von der FDA geprüft werden. Daher liegt es im besten Interesse des Herstellers, sicherzustellen, dass ein konformes Qualitätsmanagementsystem vorhanden ist, bevor das Gerät auf den Markt gebracht wird.
Gemäß der EU-MDR ist ISO 13485:2016 keine Voraussetzung für die CE-Kennzeichnung. Das vorhandene Qualitätsmanagementsystem sollte den in Anhang IX festgelegten Vorschriften entsprechen. Hersteller müssen bei der benannten Stelle einen Antrag auf Bewertung ihres Qualitätsmanagementsystems stellen. Zusätzlich zu einem Qualitätsmanagementsystem-Audit bewertet die benannte Stelle die technische Dokumentation der Geräte anhand des Qualitätsmanagementsystems, um sicherzustellen, dass alle Anforderungen vor der Zertifizierung erfüllt sind.
Um das Qualitätsmanagementsystem zu harmonisieren, besteht die beste Vorgehensweise in der Implementierung eines ISO 13485:2016- und Medical Device Single Audit Program (MDSAP)-konformen Systems mit zusätzlichen Compliance-Anforderungen für FDA, EU MDR, Health Canada oder andere Länder, in denen der Hersteller Geschäfte tätigen möchte .
Dokumentation
Die FDA und die EU-MDR erfordern einen kontrollierten Designprozess für Geräte.
Für die Einreichung gemäß 510(k) ist eine vollständige Design History File (DHF) erforderlich, in der die Systemanforderungen, die Architektur, die Spezifikationen, die Verifizierung und Validierung sowie die Dokumentation der Risikomanagementaktivitäten des Geräts detailliert aufgeführt sind. Das 510(k) eSTAR-Profil ermöglicht es Herstellern, das zugehörige Dokument jedem Abschnitt des Antrags beizufügen. Die FDA stellt eine Checkliste für die Abnahme um den Hersteller beim 510(k)-Prozess anzuleiten und sicherzustellen, dass die richtige Dokumentation vorhanden ist.
Für die EU-MDR enthält eine technische Akte die DHF-Dokumente und erfordert außerdem, dass der Hersteller die folgenden zusätzlichen Checklisten bereitstellt:
- Allgemeine Sicherheits- und Leistungsanforderungen (GSPR) gemäß Anhang I, früher bekannt als Checkliste für wesentliche Anforderungen gemäß MDD
- Technische Standarddokumentation (SteD) gemäß Anhang II
- Post-Market Surveillance (PMS) gemäß Anhang III
Ein technisches Dokument auf hoher Ebene verweist typischerweise auf die verschiedenen DHF-Dokumente und die Checklisten.
In beiden Fällen ist eine vollständige Risikomanagementdatei gemäß ISO 14971 erforderlich.
References:
- Premarket-Benachrichtigung 510(k) | FDA
- Das 510(k)-Programm: Bewertung der wesentlichen Gleichwertigkeit in Premarket-Benachrichtigungen [510(k)] (fda.gov)
- Entscheiden, wann ein 510(k) für eine Änderung an einem vorhandenen Gerät eingereicht werden soll – Leitfaden für Industrie und Mitarbeiter der Lebensmittel- und Arzneimittelbehörde (fda.gov)
- Entscheiden, wann ein 510(k) für eine Softwareänderung an einem vorhandenen Gerät eingereicht werden soll – Leitlinienentwurf für Industrie und Mitarbeiter der Lebensmittel- und Arzneimittelbehörde (fda.gov)
- MDCG 2019-15, Leitlinien für Hersteller von Medizinprodukten der Klasse I
- Senden und verfolgen Sie Einreichungen von Medizinprodukten vor der Markteinführung online: CDRH-Portal | FDA
- EUDAMED-Datenbank – EUDAMED (europa.eu)
- Änderungen der Nutzungsgebühr für medizinische Geräte (MDUFA) | FDA
- MDCG 2023-2, Liste der Standardgebühren
- Qualitätssystem (QS)-Verordnung/Gute Herstellungspraxis für Medizinprodukte | FDA
- Akzeptanz-Checklisten für 510(k)s | FDA
- eSTAR-Programm | FDA
- FDA Health Canada eSTAR (starfishmedical.com)
Bilder: Adobe Stock & StarFish Medical
Dhruvitha Krishna ist ein QA/RA-Spezialist bei StarFish Medical mit einem MS-Abschluss in Biomedizintechnik. Sie war in den Bereichen Fertigung, Implementierung neuer Produkte, Softwarebereitstellung, Projektmanagement und Regulierung in Medizingeräteunternehmen tätig. Dhruvitha widmet sich der Qualität, den Vorschriften und der kontinuierlichen Prozessverbesserung für den Hersteller.
- SEO-gestützte Content- und PR-Distribution. Holen Sie sich noch heute Verstärkung.
- PlatoData.Network Vertikale generative KI. Motiviere dich selbst. Hier zugreifen.
- PlatoAiStream. Web3-Intelligenz. Wissen verstärkt. Hier zugreifen.
- PlatoESG. Kohlenstoff, CleanTech, Energie, Umwelt, Solar, Abfallwirtschaft. Hier zugreifen.
- PlatoHealth. Informationen zu Biotechnologie und klinischen Studien. Hier zugreifen.
- Quelle: https://starfishmedical.com/blog/medical-device-510k-ce-marking/
- :hast
- :Ist
- :nicht
- :Wo
- $UP
- 1
- 12
- 2%
- 2014
- 2016
- 2024
- 21
- 300
- 32
- 4
- 400
- 420
- 500
- 8
- 820
- a
- oben
- über
- Aktivitäten
- Aktivität
- Schauspieler
- Hinzufügen
- Zusatz
- Zusätzliche
- Zusätzliche Angaben
- Verwaltung
- Adobe
- beeinflussen
- Nach der
- gegen
- Alle
- erlaubt
- ebenfalls
- Änderungen
- an
- und
- Anbau
- jährlich
- jedem
- anwendbar
- Anwendung
- gilt
- angemessen
- Genehmigung
- genehmigen
- genehmigt
- Architektur
- SIND
- Bereiche
- um
- Vereinbarungen
- Artikel
- AS
- Aspekte
- beurteilen
- Bewertung
- helfen
- damit verbundenen
- At
- anhängen
- versuchen
- Prüfung
- Verwaltung
- Autorität
- verfügbar
- erwartet
- basierend
- Grundlage
- BE
- weil
- werden
- war
- Bevor
- Sein
- gehörend
- unten
- BESTE
- zwischen
- biomedizinische
- Blog
- verwischen
- Tafel
- Körper
- Körper
- beide
- gebunden
- bringen
- Geschäft
- Unternehmen
- aber
- by
- CAN
- Kanada
- kann keine
- Fälle
- Kategorien
- kategorisiert
- Center
- Zertifikate
- Zertifizierung
- Zertifzierte
- Übernehmen
- Änderungen
- Charakteristik
- berechnen
- Gebühren
- Auswählen
- Anspruch
- behauptet
- Klasse
- Einstufung
- klar
- Spiel
- Klinische
- COM
- Kombination
- kommerziell
- Unternehmen
- verglichen
- kompetent
- abschließen
- Compliance
- konform
- entspricht
- entsprechen
- zusammengesetzt
- konzept
- Zustand
- Bedingungen
- Leitung
- dirigiert
- Konflikt
- Überlegungen
- Baugewerbe
- Kontakt
- enthält
- kontinuierlich
- Smartgeräte App
- gesteuert
- Praktische
- Kernbereich
- Kosten
- Kosten
- Ländern
- Land
- kritischem
- Zur Zeit
- Original
- Datenbase
- entscheidet
- Entscheidung
- Decision Making
- gewidmet
- Definiert
- Definition
- Grad
- delegiert
- zeigen
- zeigt
- demonstrieren
- Einsatz
- Design
- Designprozess
- detailliert
- Detaillierung
- Gerät
- Geräte
- Unterschiede
- anders
- Fleiß
- Richtlinien
- diskutiert
- Krankheit
- Display
- Displays
- verteilen
- do
- Dokument
- Dokumentation
- Unterlagen
- erledigt
- Lüftung
- gezogen
- Medikament
- zwei
- Dauer
- e
- jeder
- einfacher
- EC
- Wirtschaftlich
- bewirken
- Effektiv
- Wirksamkeit
- Anstrengung
- entweder
- beschäftigt
- Energie
- Entwicklung
- gewährleisten
- Gleichwertigkeit
- Äquivalent
- essential
- Gründung
- etc
- Äther (ETH)
- EU
- Europa
- Europäische
- Europäische Union
- Bewerten
- Auswerten
- Jedes
- Beweis
- entwickelt
- befreit
- vorhandenen
- erwartet
- Expertise
- beschleunigt
- FDA
- Gebühr
- Honorare
- wenige
- Abbildung
- Reichen Sie das
- Finale
- Fiscal
- Wohnung
- Flexibilität
- Folgende
- Nahrung,
- Food and Drug Administration
- Aussichten für
- unten stehende Formular
- weiter
- für
- voller
- Funktion
- Funktionalität
- Go
- gut
- regiert
- erteilt
- die Vermittlung von Kompetenzen,
- Guide
- Anleitungen
- Haben
- Gesundheit
- hilft
- daher
- versteckt
- GUTE
- High-Level
- Highlights
- Geschichte
- aber
- HTTPS
- human
- i
- Idee
- Login
- if
- ii
- iii
- sofort
- Impact der HXNUMXO Observatorien
- Implementierung
- Umsetzung
- Verbesserung
- in
- Einschließlich
- integrieren
- Energiegewinnung
- Information
- Einleiten
- Instrument
- beabsichtigt
- Beabsichtigen
- beabsichtigt
- Absicht
- interaktive
- Interesse
- in
- eingeführt
- Einleitung
- Untersuchungen
- Beteiligung
- ISO
- IT
- dank
- jpg
- Art
- bekannt
- Beschriftung
- führen
- führenden
- geführt
- rechtlich
- Niveau
- Lebenszyklus
- Einschränkungen
- Grenzen
- Linien
- Liste
- leben
- länger
- Los
- senken
- gemacht
- um
- Making
- verwalten
- Management
- Management System
- Hersteller
- Hersteller
- Herstellung
- viele
- März
- März 2024
- Kennzeichen
- markiert
- Markt
- vermarktet
- Markierung
- Master
- Materialien
- max-width
- Kann..
- MDR
- Messen
- Mechanismus
- sowie medizinische
- medizinisches Gerät
- Medizinprodukte
- Mitglied
- versiegelte
- Methoden
- Module
- Überwachung
- mehr
- sollen
- Need
- erforderlich
- Neu
- neue Produkt
- nicht
- beachten
- Notizen
- Benachrichtigung
- Benachrichtigungen
- Anzahl
- erhalten
- of
- on
- EINEM
- Online
- betreiben
- die
- Betrieb
- Betreiber
- or
- ursprünglich
- Andere
- Gesamt-
- Frieden
- Verpackung
- Bestanden
- Weg
- Wegen
- AUFMERKSAMKEIT
- Leistung
- ein Bild
- pilotiert
- Ort
- platziert
- Platzierung
- Plato
- Datenintelligenz von Plato
- PlatoData
- Spieler
- PMS
- Bevölkerung
- Portal
- Post
- Praxis
- Praktiken
- verhindern
- vorher
- Prinzip
- Grundsätze
- Vor
- Prozessdefinierung
- anpassen
- Produkt
- Produkte
- Profil
- Programm
- Programme
- Fortschritt
- Projekt
- Projektmanagement
- immobilien
- Angebot
- Eigentums-
- die
- vorausgesetzt
- bietet
- veröffentlicht
- Zweck
- Q3
- Qualifikations-
- Qualität
- Fragen
- erhöhen
- Rekord
- Referenzen
- bezeichnet
- angesehen
- Registrierung:
- Vorschriften
- Regulierungsbehörden
- bezogene
- verhältnismäßig
- Release
- Sanierung
- Reporting
- erfordern
- falls angefordert
- Anforderung
- Voraussetzungen:
- erfordert
- Verantwortung
- für ihren Verlust verantwortlich.
- wiederverwendbar
- Überprüfen
- Überprüfung
- Recht
- Risiko
- Risikomanagement
- Regel
- s
- Safe
- Sicherheit
- gleich
- Szenarien
- vorgesehen
- Abschnitt
- scheint
- senden
- getrennte
- kompensieren
- Sets
- mehrere
- Schwere
- Teilen
- sie
- sollte
- Konzerte
- signifikant
- bedeutend
- ähnlich
- Ähnlichkeiten
- Einfacher
- Single
- am Standort
- SIX
- Größe
- klein
- Kleine und mittlere Unternehmen
- Software
- einige
- manchmal
- spezifisch
- Spezifikationen
- Unser Team
- Stufe
- Standard
- Seestern
- Staaten
- Status
- einfach
- Strategie
- Struktur
- Es wurden Studien
- Fach
- Einreichung
- Einsendungen
- abschicken
- eingereicht
- einreichen
- wesentlich
- im Wesentlichen
- chirurgisch
- Überwachung
- System
- Systeme und Techniken
- Tabelle
- Nehmen
- beauftragt
- Technische
- technologische
- Technologie
- Testen
- zur Verbesserung der Gesundheitsgerechtigkeit
- Das
- die Welt
- ihr
- Dort.
- vom Nutzer definierten
- fehlen uns die Worte.
- nach drei
- Durch
- Zeit
- Gewebe
- zu
- verfolgen sind
- tracker
- Tracking
- Übergang
- reisen
- tippe
- Typen
- typisch
- für
- unterziehen
- unterziehen
- Gewerkschaft
- einzigartiges
- es sei denn
- Aktualisierung
- aktualisiert
- Updates
- -
- benutzt
- Mitglied
- Verwendung von
- Bestätigung
- verschiedene
- variieren
- Verification
- Video
- Anzeigen
- Wachsamkeit
- vincent
- wurde
- Wege
- Webseite
- wann
- welche
- während
- werden wir
- mit
- .
- ohne
- gearbeitet
- arbeiten,
- Werk
- weltweit wie ausgehandelt und gekauft ausgeführt wird.
- Jahr
- U
- Ihr
- Youtube
- Zephyrnet