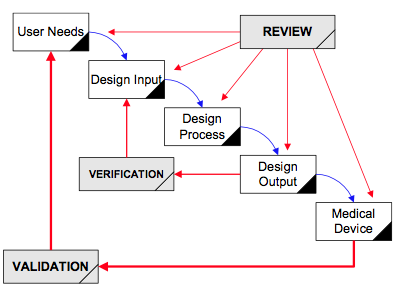
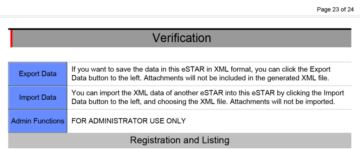
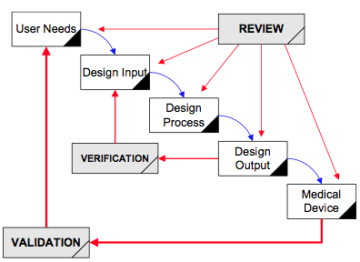
Das Wasserfalldiagramm wurde von der FDA von Health Canada und ISO 9001:1994 kopiert, aber tatsächlich verwendet jeder einen iterativen Designprozess.
[Eingebetteten Inhalt]
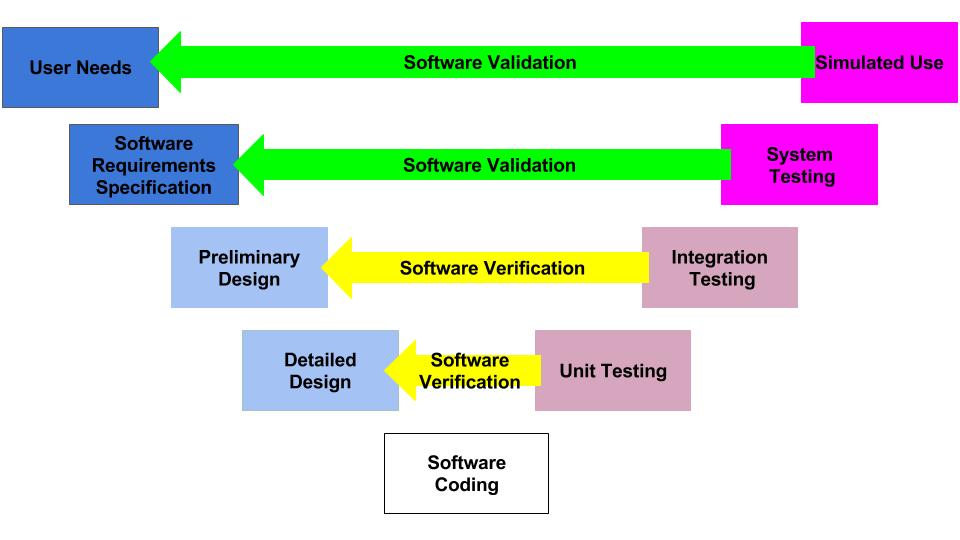
Die FDA forderte erstmals 1996 die Einführung von Designkontrollen für Hersteller medizinischer Geräte auf. Leider wurde der Designprozess 1996 als linearer Prozess beschrieben. Tatsächlich umfasst die Entwicklung fast aller Produkte, insbesondere medizinischer Geräte, einen iterativen Designprozess. Das V-Diagramm von IEC 62304 ist näher am tatsächlichen Entwurfskontrollprozess, aber selbst dieser Prozess ist zu stark vereinfacht.
Was ist der Designkontrollprozess?
Der Design-Kontrollprozess ist die Sammlung von Methoden, die von einem Team aus Personen und Unternehmen verwendet werden, um sicherzustellen, dass ein neues medizinisches Gerät den Anforderungen von Kunden, Aufsichtsbehörden, anerkannten Standards und Interessengruppen entspricht. Bei so vielen erforderlichen Eingaben ist es höchst unwahrscheinlich, dass jemals ein neues medizinisches Gerät in einem linearen Prozess entwickelt werden könnte. Der Designkontrollprozess muss auch das Risikomanagement und die Disziplinen menschlicher Faktoren integrieren. ISO 14971:2019, der internationale Risikomanagementstandard, erfordert die Durchführung einer optionalen Kontrollanalyse. Die Optionskontrollanalyse erfordert die Bewertung mehrerer Risikokontrolloptionen und die Auswahl der besten Kombination von Risikokontrollen für die Implementierung. Der Human-Factors-Prozess beinhaltet formative Tests, bei denen Sie verschiedene Lösungen für Benutzeroberflächen, Gebrauchsanweisungen und Schulungen bewerten. Dies erfordert immer mehrere Überarbeitungen, bevor die Benutzerspezifikationen für die Validierung in summativen Usability-Tests bereit sind. Der Prozesserfolg wird durch die Durchführung von Verifizierungs- und Validierungstests überprüft. Der Prozess endet, wenn das Team zustimmt, dass alle Aktivitäten zur Designübertragung abgeschlossen sind und Ihre behördliche Genehmigung eingegangen ist.
Woher kommen Designkontrollen?
Das obige Diagramm heißt „Anwendung von Designkontrollen auf den Wasserfall-Designprozess.“ Die FDA hat dieses Diagramm 1997 eingeführt Leitfaden für Designkontrollen. Die ursprüngliche Quelle des Diagramms war jedoch Health Canada.
Dieses Diagramm ist eine der ersten Folien, die ich für jeden Designkontrollkurs verwende, den ich unterrichte, da das Diagramm den Designkontrollprozess visuell darstellt. Der von Health Canada und der US-amerikanischen FDA definierte Designkontrollprozess entspricht dem Design- und Entwicklungsabschnitt in ISO 13485 und ISO 9001 (d. h. – Abschnitt 7.3). Sieben Unterabschnitte umfassen die Anforderungen dieser ISO-Normen:
- 7.3.1 – Designplanung
- 7.3.2 – Designeingaben
- 7.3.3 – Design-Ausgaben
- 7.3.4 – Designbewertungen
- 7.3.5 – Designverifizierung
- 7.3.6 – Designvalidierung
- 7.3.7 – Designänderungen
Zusätzlich zu den sieben Unterabschnitten dieser ISO-Standards enthält die FDA Quality System Regulation (QSR) auch zusätzliche Anforderungen in den folgenden Unterabschnitten von 21 CFR 820.30: a) Allgemein, h) Designübertragung und J) Konstruktionsverlaufsdatei (DHF).
Kostenloser Download – Überblick über den Design- und Entwicklungsprozess
Was sind die Phasen des Design-Kontrollprozesses?
Normalerweise schließen wir den Designkontrollprozess ab, indem wir Ihr Gerät in den USA auf den Markt bringen, da Sie zu diesem Zeitpunkt Ihre Design History File (DHF) schließen sollten. Wenn Sie jedoch in andere Märkte expandieren möchten, empfehlen wir eine bestimmte Reihenfolge. Wir empfehlen zunächst den US-Markt, da keine Zertifizierung des Qualitätssystems erforderlich ist und der FDA 510(k)-Prozess aufgrund der Implementierung einfacher ist als der CE-Kennzeichnungsprozess MDR und für IVDR. Der kanadische Markt ist der zweite Markt, den wir empfehlen, da der Kanadischer Gerätelizenzantrag Der Prozess für Health Canada ist sogar einfacher als der 510(k)-Prozess für Geräte der Klasse II. Der kanadische Markt wird aufgrund der Anforderungen von Health Canada nicht als erstes Land für die Markteinführung empfohlen MDSAP-Zertifizierung für Ihr Qualitätssystem, und der kanadische Markt macht 10 % der US-Marktgröße aus. Der europäische Markt sollte aufgrund der hohen Kosten und des langen Zeitrahmens für die Erlangung der CE-Kennzeichnung wahrscheinlich Ihr letzter Markt sein. Jede der Design- und Entwicklungsphasen wird in der ersten Spalte unseres kostenlosen Downloads „Überblick über regulatorische Prozesse, Entwicklung medizinischer Geräte und Qualitätssystemplanung für Start-ups“ beschrieben.
Welche behördlichen Einreichungen sind in jeder Design- und Entwicklungsphase erforderlich?
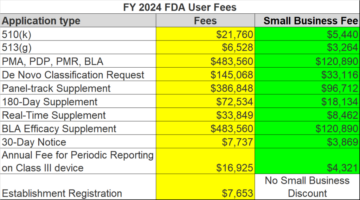
In der zweiten Spalte unseres kostenlosen Downloads sind die von der FDA für jede Phase erforderlichen Zulassungsanträge aufgeführt. Im Allgemeinen warten Unternehmen zu lange auf ihr erstes Treffen vor der Einreichung mit der FDA oder lassen das Treffen vor der Einreichung ganz aus. Das ist ein strategischer Fehler. Es steht Ihnen frei, Vorabbesprechungen bei der FDA einzureichen. Der Zweck der Besprechung besteht darin, Ihre Fragen zu beantworten. Selbst wenn Sie den regulatorischen Weg zu 100 % kennen, genau wissen, welches Prädikat Sie verwenden möchten und welche Verifizierungstests Sie durchführen müssen, haben Sie immer noch intelligente Fragen, die Sie der FDA stellen können. Kritische Fragen lassen sich in drei Kategorien einteilen: 1) Auswahl Ihrer Testartikel, 2) Begründung der Stichprobengröße und 3) Akzeptanzkriterien. Auch wenn Sie kein vollständiges Testprotokoll für die Prüfung durch die FDA vorbereitet haben, können Sie eine Begründung für Ihren Testartikel vorschlagen (z. B. die kleinste Größe in Ihrer Produktfamilie). Sie können auch einen Absatz bereitstellen, in dem die statistische Begründung Ihrer Stichprobengröße erläutert wird. Sie können auch einen Absatz vorlegen, in dem die Datenanalysemethode erläutert wird, die Sie verwenden möchten.
Das folgende Beispiel zeigt, wie Sie durch die Besprechung der Einzelheiten Ihres Testplans mit der FDA Anfragen nach zusätzlichen Informationen und erneute Tests vermeiden können. Viele der Hersteller von chirurgischen Masken, die während der Covid-19-Pandemie Geräte eingereicht hatten, stellten fest, dass die FDA die Anforderungen an die Probengröße geändert hatte und nun drei nicht aufeinanderfolgende Chargen mit einer Berechnung der Probengröße von 4 % AQL verlangte. Wenn das Unternehmen eine Charge von 50,000 Masken herstellen würde, wäre es gezwungen, eine große Anzahl von Masken zu bemustern, während eine Losgröße von 250 Masken es dem Unternehmen ermöglichte, die Mindestprobengröße von 32 Masken zu bemustern.
Wenn der regulatorische Weg für Ihr Gerät unklar ist, können Sie in der ersten Design- und Entwicklungsphase mit der Einreichung einer 513(g)-Einreichung beginnen. Nachdem Sie von der FDA eine schriftliche Bestätigung des korrekten Zulassungswegs erhalten haben, können Sie bei der FDA einen Antrag auf ein Treffen vor der Einreichung einreichen. Wenn es sich bei dem Weg für Ihr Gerät um einen De-Novo-Klassifizierungsantrag handelt, führen Sie möglicherweise ein vorläufiges Treffen vor der Einreichung durch, um eine Einigung mit der FDA darüber zu erzielen, welche anerkannten Standards als Sonderkontrollen für Ihr Gerät angewendet werden sollten. Während Sie mehr als 70 Tage auf Ihr Vorgespräch mit der FDA warten, können Sie Angebote von Testlabors einholen und Entwürfe von Testprotokollen erstellen. Nach dem Treffen vor der Einreichung können Sie eine Ergänzung zur Einreichung vor der Einreichung einreichen, die detaillierte Testprotokolle enthält – einschließlich Ihrer Begründung für die Auswahl der Testartikel, der Begründung der Stichprobengröße und der Akzeptanzkriterien.
Welche Qualitätssicherungsdokumentation ist in jeder Phase erforderlich?
Neben Prüfberichten für Ihre Verifizierungs- und Validierungsprüfungen finden Sie hier auch viele weitere unterstützende Dokumente, die Sie ebenfalls vorbereiten müssen. Wir bezeichnen diese unterstützenden Dokumente allgemein als „Qualitätssicherungsdokumentation“, da die Dokumente bestätigen, dass Sie bestimmte Kunden- und Regulierungsanforderungen erfüllen. Die Dokumente sollten jedoch von der Person oder den Personen erstellt werden, die für diesen Teil Ihres Designprojekts verantwortlich sind. Beispielsweise benötigt jedes Gerät eine Bedienungsanleitung und einen Etikettierungsentwurf. Auch wenn Sie jemanden aus der Qualitätsabteilung benötigen, der eine regulatorische Checkliste ausfüllt, um sicherzustellen, dass alle Anforderungen erfüllt sind erforderliche Symbole und allgemeine Etiketteninhalte enthalten sind, benötigen Sie außerdem einen Elektrotechniker, der Abschnitte des Handbuchs mit EMV-Kennzeichnungsanforderungen aus dem vorbereitet EMV-Leitfaden der FDA. Im Abschnitt „Nichtklinische Leistungstests“ Ihrer Einreichung müssen Sie Folgendes angeben Dokumentation menschlicher Faktoren zusätzlich zu Ihrem summativen Usability-Testbericht. Sie benötigen beispielsweise eine Verwendungsspezifikation, Ergebnisse Ihrer systematischen Suche nach unerwünschten Ereignissen für Anwendungsfehler, eine Aufgabenanalyse und eine nutzungsbezogene Risikoanalyse (URRA). Die Software- und Cybersicherheitsdokumentation umfasst neben den Testberichten auch mehrere Dokumente.
Welche Verfahren müssen Sie in jeder Entwicklungsphase implementieren?
In der letzten Spalte unseres kostenlosen Downloads sind die Verfahren aufgeführt, die wir in jeder Phase des Designprozesses empfehlen. In Kanada und Europa müssen Sie die Implementierung Ihres gesamten Qualitätssystems abschließen, bevor Sie einen kanadischen Lizenzantrag oder einen CE-Kennzeichnungsantrag einreichen. In den USA können Sie die Implementierung Ihres Qualitätssystems jedoch während der FDA-Prüfung Ihres 510k-Antrags oder sogar nach Erhalt der 510k-Freigabe abschließen. Die Anforderung an das Qualitätssystem besteht darin, dass Ihr Qualitätssystem vollständig implementiert ist, wenn Sie Ihr Unternehmen bei der FDA registrieren und mit dem Vertrieb beginnen.
Veröffentlicht in: Designkontrolle
- SEO-gestützte Content- und PR-Distribution. Holen Sie sich noch heute Verstärkung.
- PlatoData.Network Vertikale generative KI. Motiviere dich selbst. Hier zugreifen.
- PlatoAiStream. Web3-Intelligenz. Wissen verstärkt. Hier zugreifen.
- PlatoESG. Automobil / Elektrofahrzeuge, Kohlenstoff, CleanTech, Energie, Umwelt, Solar, Abfallwirtschaft. Hier zugreifen.
- BlockOffsets. Modernisierung des Eigentums an Umweltkompensationen. Hier zugreifen.
- Quelle: https://medicaldeviceacademy.com/iterative-design/
- :Ist
- :nicht
- :Wo
- 000
- 1
- 14
- 16
- 1994
- 1996
- 250
- 30
- 32
- 50
- 7
- a
- oben
- Akzeptanz
- Aktivitäten
- berührt das Schneidwerkzeug
- Zusatz
- Zusätzliche
- Zusätzliche Angaben
- Neben
- Nach der
- Zustimmung
- Alle
- erlaubt
- ebenfalls
- insgesamt
- immer
- an
- Analyse
- und
- beantworten
- Anwendung
- angewandt
- Genehmigung
- SIND
- Artikel
- Artikel
- AS
- Versicherung
- Autor
- vermeiden
- BE
- weil
- Bevor
- beginnen
- BESTE
- Beyond
- aber
- by
- namens
- CAN
- Kanada
- kanadischen
- Kategorien
- Zertifizierung
- geändert
- Klasse
- Einstufung
- Menu
- näher
- Sammlung
- Kolonne
- Kombination
- wie die
- Unternehmen
- Unternehmen
- abschließen
- Abgeschlossene Verkäufe
- Leitung
- zuversichtlich
- Bestätigung
- Inhalt
- Smartgeräte App
- Steuerung
- und beseitigen Muskelschwäche
- Kosten
- könnte
- Land
- Kurs
- COVID-19
- COVID-19-Pandemie
- Kriterien
- kritischem
- Kunde
- Kunden
- Internet-Sicherheit
- technische Daten
- Datenanalyse
- Datum
- Tage
- de
- definiert
- beschrieben
- Design
- Designprozess
- detailliert
- Details
- entwickelt
- Entwicklung
- Gerät
- Geräte
- DID
- anders
- Disziplinen
- diskutieren
- Displays
- Verteilung
- do
- Dokumentation
- Unterlagen
- Nicht
- herunterladen
- Lüftung
- zwei
- im
- e
- jeder
- einfacher
- eingebettet
- Ende
- endet
- Ingenieur
- gewährleisten
- Ganz
- Äquivalent
- Fehler
- insbesondere
- Gründung
- Äther (ETH)
- Europa
- Europäische
- bewerten
- Auswerten
- Sogar
- Veranstaltungen
- ÜBERHAUPT
- Jedes
- jedermann
- Beispiel
- Erweitern Sie die Funktionalität der
- Erläuterung
- Faktoren
- Fallen
- Familie
- FDA
- Reichen Sie das
- Einreichungen
- Finden Sie
- Fertig
- Vorname
- Folgende
- Aussichten für
- gezwungen
- gefunden
- Frei
- für
- voll
- Allgemeines
- allgemein
- bekommen
- gehen
- die Vermittlung von Kompetenzen,
- hätten
- Haben
- Gesundheit
- Hilfe
- GUTE
- hoch
- Geschichte
- Ultraschall
- aber
- http
- HTTPS
- human
- menschliche Faktoren
- i
- if
- ii
- zeigt
- implementieren
- Implementierung
- umgesetzt
- Umsetzung
- in
- das
- inklusive
- Dazu gehören
- Information
- Eingänge
- integrieren
- Intelligent
- Schnittstellen
- International
- in
- eingeführt
- beinhaltet
- ISO
- ISO 9001
- IT
- jpg
- Wissen
- Label
- Beschriftung
- Labs
- grosse
- Nachname
- starten
- Start
- Lizenz
- Listen
- Lang
- Los
- gemacht
- Management
- manuell
- Hersteller
- viele
- Markt
- Märkte
- Markierung
- Maske"
- Masken
- max-width
- sowie medizinische
- medizinisches Gerät
- Medizinprodukte
- Triff
- Treffen
- Tagungen
- Metadaten
- Methode
- Methoden
- könnte
- Minimum
- Fehler
- mehrere
- sollen
- Need
- Neu
- nicht
- Neu
- jetzt an
- Anzahl
- erhalten
- beschaffen
- of
- on
- EINEM
- Option
- Optionen
- or
- Auftrag
- Original
- Andere
- UNSERE
- skizzierte
- Überblick
- Pandemie
- Weg
- Personen
- Leistung
- person
- Phase
- Plan
- Planung
- Plato
- Datenintelligenz von Plato
- PlatoData
- Spieler
- gepostet
- BLOG-POSTS
- genau
- Danach
- bereit
- Gegenwart
- wahrscheinlich
- Verfahren
- Prozessdefinierung
- Produkt
- Projekt
- bietet
- Protokoll
- Protokolle
- die
- Zweck
- Qualität
- Fragen
- Zitate
- bereit
- echt
- Realität
- Received
- anerkannt
- empfehlen
- empfohlen
- in Bezug auf
- Registrieren
- Rechtliches
- Regulators
- Regulierungsbehörden
- behördliche Genehmigung
- berichten
- Meldungen
- Anforderung
- Zugriffe
- falls angefordert
- Anforderung
- Voraussetzungen:
- erfordert
- für ihren Verlust verantwortlich.
- Die Ergebnisse
- Überprüfen
- Revisionen
- Risiko
- Risikomanagement
- rauben
- Suche
- Zweite
- Abschnitt
- Abschnitte
- sehen
- Auswahl
- Auswahl
- sieben
- mehrere
- sollte
- Größe
- Slides
- kleinste
- So
- Software
- Lösungen
- Jemand,
- Quelle
- besondere
- spezifisch
- Spezifikation
- Spezifikationen
- Stakeholder
- Standard
- Normen
- Anfang
- Start-ups
- statistisch
- Immer noch
- Strategisch
- Einreichung
- abschicken
- eingereicht
- Erfolg
- ergänzen
- Unterstützung
- chirurgisch
- System
- Aufgabe
- Team
- Test
- Testen
- Tests
- als
- zur Verbesserung der Gesundheitsgerechtigkeit
- Das
- ihr
- Dort.
- Diese
- vom Nutzer definierten
- fehlen uns die Worte.
- obwohl?
- nach drei
- Timeline
- zu
- auch
- Ausbildung
- privaten Transfer
- Unglücklicherweise
- unwahrscheinlich
- aktualisiert
- us
- USA
- Nutzbarkeit
- Usability-Tests
- -
- benutzt
- Mitglied
- verwendet
- validiert
- Bestätigung
- Verification
- verified
- überprüfen
- Video
- Warten
- wurde
- we
- GUT
- waren
- wann
- welche
- während
- werden wir
- mit
- würde
- WPEngine
- geschrieben
- U
- Ihr
- Youtube
- Zephyrnet