Coltura cellulare
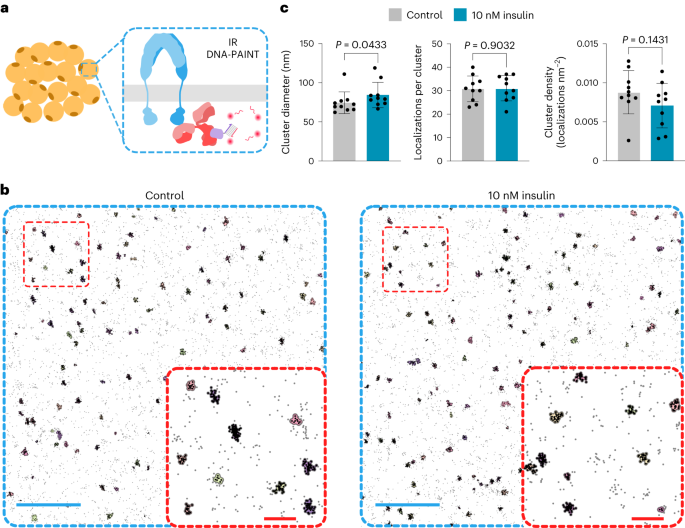
Gli adipociti bruni sono stati differenziati da una linea cellulare di topo preadipociti marroni immortalata gentilmente fornita da B. Spiegelman (Università di Harvard) come precedentemente descritto19. I preadipociti sono stati mantenuti ed espansi a bassa confluenza (<50%) in un mezzo di crescita (terreno di Eagle modificato di Dulbecco, alto glucosio (Gibco), integrato con siero bovino fetale al 20% (Sigma-Aldrich), HEPES 20 mM (Sigma-Aldrich) e 100 Uml-1 penicillina-streptomicina (Gibco)). Per la differenziazione, i preadipociti sono stati lavati due volte con soluzione tamponata con fosfato (PBS) (Gibco, pH 7.4, 1×), dissociati con TrypLE Express e seminati ad una densità di circa 23,000 cellule cm-2 nel mezzo di crescita. Il terreno è stato cambiato dopo 24 ore con un terreno di differenziazione (terreno di Eagle modificato da Dulbecco, ad alto contenuto di glucosio, integrato con siero bovino fetale al 10%, insulina 20 nM, triiodotironina 1 nM e 100 U ml-1 penicillina-streptomicina) e le cellule sono state coltivate per 2 giorni. La differenziazione cellulare è stata quindi indotta mediante l'aggiunta di un mezzo di induzione (mezzo di differenziazione integrato con indometacina 0.125 mM, desametasone 0.5 μM e isobutilmetilxantina 0.5 mM) per 2 giorni, dopo di che il mezzo è stato cambiato con il mezzo di differenziazione per altri due giorni. Gli adipociti differenziati sono stati lavati una volta con un mezzo di denutrizione (terreno di Eagle modificato da Dulbecco, a basso contenuto di glucosio (Gibco), integrato con glucosio fino a una concentrazione finale di 8 mM, 0.5% di albumina sierica bovina (Sigma-Aldrich) e 100 U ml-1 penicillina-streptomicina) e incubati per 2 ore nel mezzo di fame prima del trattamento con insulina NanoRods o NanoRods diluiti nel mezzo di fame per i tempi indicati nel testo principale. Dopo il trattamento, le cellule sono state lavate una volta in PBS e raccolte per l'isolamento delle proteine per gli immunoblot o dell'RNA per l'espressione genica. Per l'analisi IR mediante DNA-PAINT, i preadipociti sono stati differenziati come descritto sopra con le seguenti modifiche. Dopo il trattamento con il mezzo di induzione, le cellule sono state dissociate con TrypLE Express e seminate nel mezzo di differenziazione in pozzetti μ-Slide 18 Well Glass Bottom (ibidi). Dopo 2 giorni, le cellule sono state incubate con il mezzo di fame per 2 ore, seguite da trattamento con insulina 10 nM nel mezzo di fame per 10 minuti. Negli esperimenti di controllo l’aggiunta di insulina è stata omessa. Prima del trattamento, gli adipociti differenziati sono stati analizzati visivamente per valutare la densità della superficie cellulare e per valutare la differenziazione delle cellule, e quindi assegnati in modo casuale ai gruppi di trattamento e di controllo.
Le cellule sono state mantenute, espanse e differenziate in un'atmosfera umidificata contenente il 5% di CO2 a 37 °C.
DNA-PAINT di IR
Gli adipociti differenziati sono stati fissati per 12 minuti a temperatura ambiente (RT) con paraformaldeide al 4% preriscaldata in PBS, lavati tre volte con PBS, bloccati per 90 minuti a temperatura ambiente con una soluzione bloccante (3.0% siero bovino fetale/0.1% Triton X -100 in PBS) e incubati con anticorpo anti-IR β di coniglio (segnalazione cellulare (4B8); diluizione 1:300 nella soluzione bloccante) per 2 giorni a 4 °C. Le cellule sono state quindi lavate tre volte con PBS e incubate con il nanobody FluoTag-XM-QC anti-coniglio IgG (Massive Photonics) diluito 1:200 in un tampone bloccante (Massive Photonics) per 1 ora a temperatura ambiente. Dopo tre lavaggi con PBS, le cellule sono state incubate con nanoparticelle d'oro da 80 nm (Sigma-Aldrich; diluizione 1:5 nel tampone bloccante) per 10 minuti. Le cellule sono state lavate una volta con PBS e incubate con filamenti marcati con Cy5b da 3 nM (Massive Photonics) diluiti in un buffer di immagine (Massive Photonics).
L'imaging è stato effettuato su un microscopio Nikon ECLIPSE Ti-E con un sistema Perfect Focus (strumenti Nikon), applicando una configurazione di fluorescenza a riflessione interna totale di tipo obiettivo utilizzando un modulo circolare di fluorescenza a riflessione interna totale iLAS2 (sistemi Gataca) con un'immersione in olio Obiettivo CFI Plan Apo con apertura numerica per fluorescenza a riflessione interna totale × 1.49 (strumenti Nikon) dotato di ingrandimento Optovar ausiliario × 100 corrispondente a una dimensione finale dei pixel di 1.5 nm. Il laser utilizzato era un OBIS 87 nm LS 561 mW (coerente) con ottica di espansione del raggio di ingresso iLas personalizzata (Cairn) ottimizzata per l'imaging a super risoluzione a campo ridotto. Il fascio di luce fluorescente è stato fatto passare prima attraverso un cubo filtro (150, Chroma Technology) contenente un filtro di eccitazione quadband, un filtro dicroico quadband e un filtro di emissione quadband (ZET89901/405/488/561x, ZET640/405/488/561bs e ZET640 /405/488/561m, Tecnologia Chroma). La luce di fluorescenza è stata quindi filtrata spettralmente con un filtro di emissione (ET640/595m, Chroma Technology) e ripresa su una fotocamera con dispositivo ad accoppiamento di carica iXon Ultra 50 con moltiplicazione di elettroni (Andor). Il software Micro-Manager v. 888 è stato utilizzato per acquisire 1.4 fotogrammi con frame di lettura da 12,000 MHz, esposizione di 10 ms e nessun guadagno di moltiplicazione degli elettroni. In ciascuna condizione sono state fotografate un totale di dieci cellule provenienti da tre esperimenti indipendenti (Nota integrativa e la figura supplementare. 1).
Produzione e purificazione dell'INS-DNA
Insulina (Merck, 1 mg ml-1) è stato fatto reagire con dibenzocicloottin-solfo-N-idrossisuccinimidil estere (DBCO-sulfo-NHS, Click Chemistry Tools; 690 µM) in 100 mM Na2CO3 tampone (pH 11.5) per 20 minuti a temperatura ambiente. La reazione è stata quindi spenta per 5 minuti mediante l'aggiunta di Tris base (Sigma-Aldrich, 100 mM). La soluzione è stata lavata tre volte con 400 µl di Na 100 mM2CO3 utilizzando unità filtranti centrifughe Amicon Ultra da 0.5 ml con membrana cut-off da 3 kDa (Merck). Ad ogni fase di lavaggio, le colonne sono state centrifugate per 10 minuti a 14,000×g. Dopo la fase di lavaggio finale, l'insulina-DBCO (690 µM) è stata miscelata con DNA modificato con azide (Biomers, 35 µM; Tabella Supplementare 3) in 100 mM Na2CO3 e lasciato reagire per 3 ore a temperatura ambiente. La reazione è stata bloccata aggiungendo NaN3 (Sigma-Aldrich, 6.9 mM). I campioni sono stati analizzati su un gel di poliacrilammide nativo (6% di poliacrilammide 19:1 in 1× TAE, 20 min, 200 V, tampone di corsa TAE) e colorati con SYBR Gold (Thermo Fisher) secondo le istruzioni del produttore, per confermare l'INS- Formazione del DNA. L'imaging è stato eseguito utilizzando un imager gel ImageQuant LAS 4000. Il protocollo di coniugazione insulina-DBCO-sulfo-NHS è stato ottimizzato per promuovere il legame dell'oligo ssDNA alla lisina-29 della catena B (lisina B29) rispetto ai gruppi amminici al livello N terminale delle catene A e B dell’insulina. Il valore pKa dell'ammina B29 è superiore a quello delle ammine delle due N termini (11.2 contro 8.6 e 6.8). A pH elevato, si prevede che il gruppo NHS del reticolante reagisca preferenzialmente con il gruppo amminico più basico, ovvero l'ammina lisina B2932. Pertanto, le condizioni di reazione del pH sono state ottimizzate per promuovere un singolo prodotto INS-DNA.
Le miscele di reazione INS-DNA sono state purificate mediante cromatografia liquida ad alte prestazioni a fase inversa C18 colonna (Agilent Poroshell 120 EC-C18) su un Amersham Pharmacia Biotech ÄKTA Ettan LC. Il tampone A (50 mM di trietilammina acetato) e il tampone B (90% acetonitrile e 10% tampone A) sono stati utilizzati in un profilo di gradiente, in cui la percentuale di tampone B è stata aumentata dal 30% al 50% in 20 minuti. Le frazioni sono state raccolte e centrifugate su un concentratore sotto vuoto (Thermo Scientific SpeedVac Savant DNA 120) per 30 minuti a calore elevato per rimuovere i componenti volatili dei tamponi per cromatografia liquida ad alte prestazioni. I picchi selezionati sono stati scambiati con tampone in PBS utilizzando unità filtranti centrifughe Amicon Ultra da 0.5 ml con una membrana cut-off da 3 kDa (Merck), mediante centrifugazione tre volte per 10 minuti a 14,000×g e lavando ogni volta con 400 µl di PBS. Campioni di frazioni purificate sono stati eseguiti su un gel di poliacrilammide nativo e colorati con SYBR Gold (Thermo Fisher) per visualizzare l'INS-DNA purificato. La purezza finale dei coniugati è stata analizzata per ogni preparazione tramite tre metodi: confronto delle intensità delle bande di colorazione con argento (Pierce Silver Stain Kit) su elettroforesi su gel di sodio dodecil solfato-poliacrilammide (Invitrogen, 4–12% Bolt gel) rispetto agli standard di insulina (Merck) , confronto dell'intensità della banda SYBR Gold sull'elettroforesi su gel di poliacrilammide nativo rispetto agli standard del DNA (tecnologie integrate del DNA) e tramite il kit di analisi Qubit ssDNA (fluorimetro Qubit 4, Invitrogen). Le concentrazioni finali di INS-DNA sono state calcolate sulla base delle misurazioni Qubit ssDNA. Il DNA INS purificato è stato congelato e conservato a -20 °C fino a ulteriore utilizzo.
Produzione di NanoRod e NanoRod di insulina
Le strutture di origami sono state preparate mescolando il DNA plasmidico dell'impalcatura (p7560, Tilibit, 10 nM) con i filamenti di fiocco appropriati (Tecnologie del DNA integrate, 100 nM) (Tabelle Supplementari 4-9) in un buffer di ripiegamento (Tris 5.0 mM a pH 8.5 (Sigma-Aldrich), EDTA 1.0 mM (Panreac AppliChem) e MgCl 12.5 mM2 (Sigma-Aldrich)). La miscela è stata quindi posizionata in un termociclatore (ciclatore termico a gradiente PTC-225 di MJ Research) e ricotta riscaldando a 80.0 °C per 5 minuti, raffreddando a 60.0 °C a 1.0 °C al minuto per 20 minuti e quindi raffreddando lentamente a 20.0 °C a 0.5 °C al minuto. I punti metallici in eccesso sono stati rimossi utilizzando unità filtranti centrifughe Amicon Ultra da 0.5 ml con una membrana cut-off da 100 kDa (Merck) mediante centrifugazione cinque volte per 2 minuti a 14,000×g e lavare ogni volta con 400 µl del tampone di ripiegamento. La concentrazione della struttura purificata è stata determinata misurando l'assorbanza del DNA a 260 nm (Thermo Scientific NanoDrop 2000). L'INS-DNA purificato è stato quindi aggiunto in eccesso stechiometrico 3 volte ai siti estesi di legame del filamento disponibili sulla struttura NanoRod e ricotto in un termociclatore riscaldando a 37.0 °C per 1 ora, raffreddando a 22.0 °C a 0.1 °C al minuto, incubazione a 22.0 °C per 14 ore e raffreddamento a 4.0 °C a 0.1 °C al minuto. L'INS-DNA non legato è stato rimosso utilizzando unità filtranti centrifughe Amicon Ultra da 0.5 ml con una membrana cut-off da 100 kDa (Merck), centrifugando cinque volte per 2 minuti a 14,000×g e lavando ogni volta con 400 µl di PBS + MgCl 10 mM2. I NanoRod di insulina sono stati conservati a 4 °C fino al successivo utilizzo.
Elettroforesi su gel di agarosio
Le strutture NanoRod sono state analizzate eseguendo campioni su gel di agarosio su ghiaccio per 4 ore a 70 V. I gel erano composti da agarosio al 2% (Thermo Scientific TopVision Agarose) in tampone TBE 0.5 × (Panreac AppliChem) più MgCl 10 mM2 (Sigma-Aldrich) e colorazione 1× SYBR Safe DNA (Invitrogen). L'imaging è stato eseguito utilizzando un imager gel ImageQuant LAS 4000.
Dispersione della luce dinamica
I campioni NanoRod e NanoRod di insulina sono stati preparati in PBS + 10 mM MgCl2, siringa filtrata utilizzando membrane da 0.1 µm (Merck) e analizzata su uno strumento Zetasizer Ultra (Malvern Panalytical). Sono state effettuate tre misurazioni a 25 °C in una cella a basso volume (ZSU1002) e quindi è stata calcolata la media.
Simulazione oxDNA del NanoRod
Le strutture NR, NR-1, NR-2, NR-4, NR-7 e NR-15 sono state analizzate utilizzando la modellazione a grana grossa di oxDNA (https://oxdna.org/). Strutture NanoRod con filamenti dsDNA che si estendono dai siti di incorporazione dell'insulina sono state create utilizzando vHelix e convertite nel formato oxDNA utilizzando il sito web tacoxDNA (http://tacoxdna.sissa.it/). Le strutture sono state sottoposte al oxDNA.org server web per simulazione a 37 °C, con 1 come concentrazione salina, 1 × 108 passaggi temporali con l'annunciot valore di 0.0001 e una fase di rilassamento preliminare con i parametri predefiniti. Sono state visualizzate le simulazioni e realizzati i video utilizzando lo strumento oxView (https://oxdna.org/).
TEM a colorazione negativa
I NanoRod purificati (10 nM) sono stati dispensati su una griglia TEM in rame supportata da carbonio scaricata a bagliore (TEM-CF200CU50, Thermo Fisher Scientific) e incubati per 60 secondi prima di rimuovere la soluzione. Le griglie sono state quindi colorate per 10 secondi con 5 µl di formiato di uranile al 2% p/v, che è stato successivamente rimosso. La procedura di colorazione è stata ripetuta sette volte e le griglie TEM sono state asciugate all'aria per 30 minuti prima dell'imaging. L'imaging è stato eseguito su un Talos 120C G2 (120 kV, rilevatore Ceta-D) a ×92,000 per visualizzazioni in campo vicino. Le immagini grezze sono state elaborate utilizzando il software ImageJ (v1.53).
AFM
Le strutture NanoRod sono state esposte su un disco di mica fissato con adesivo epossidico al centro di un vetrino da microscopio e racchiuso da un anello di plastica fissato al vetrino utilizzando Reprorubber. Le nanostrutture sono state diluite a 1 nM in tampone TE-Mg (5 mM Tris base, 1 mM EDTA, 10 mM MgCl2, pH 8.0) e 10 µl sono stati pipettati sulla mica appena scissa. Dopo 30 s, 4 ml di NiSO 5 mM4 è stato aggiunto e incubato per altri 4.5 minuti. La superficie è stata quindi risciacquata con 1.0 ml di tampone TE-Mg filtrato da 0.1 µm, dopo di che 1.5 ml di tampone TE-Mg filtrato sono stati aggiunti al disco di mica per l'imaging. L'imaging è stato eseguito in liquido utilizzando un microscopio a forza atomica NanoWizard 3 Ultra JPK Instruments con un cantilever Bruker AC40 in modalità AC.
DNA-PAINT di nanostrutture di insulina NanoRod
I pozzetti con fondo in vetro da 18 pozzetti µ-Slide (ibidi) sono stati puliti con isopropanolo e asciugati con N2. I pozzetti sono stati incubati con 1 mg ml-1 Albumina di siero bovino con biotina (Thermo Fisher) in tampone A (Tris-HCl 10 mM, NaCl 100 mM e Tween 0.05 allo 20% (v/v) a pH 8.0) per 5 minuti a temperatura ambiente, lavato tre volte con tampone A e incubato con 0.5mg ml-1 neutravidina (Thermo Fisher) nel tampone A per 5 minuti a temperatura ambiente. I pozzetti sono stati quindi lavati tre volte con tampone A seguiti da tre lavaggi con tampone B (5 mM Tris-HCl, 10 mM MgCl2, EDTA 1 mM e Tween 0.05 allo 20% (v/v) a pH 8.0). Quindi, NanoRod da 500 pM che incorporano quattro filamenti di DNA marcati con biotina (Dati estesi Fig. 2a), con INS-DNA contenente una sequenza di aggancio PAINT a 9 nucleotidi (DS1; Tabella supplementare 3), è stato aggiunto a ciascun pozzetto per 5 minuti. I pozzetti sono stati lavati tre volte con tampone B. Quindi, 1 nM del filamento imager Atto-647N (IS1; Tabella supplementare 10) nel tampone B integrato con scavenger di ossigeno (acido protocatecuico (Sigma), protocatechuato 3,4-diossigenasi (Sigma) e Trolox (Sigma)) è stato aggiunto a ciascun pozzetto. Per PAINT a doppio scambio, tre sequenze di docking (DS2; Tabella supplementare 10) sono stati aggiunti su entrambe le estremità dei NanoRod. I campioni sono stati preparati come descritto in precedenza, lavando i pozzetti dieci volte con il tampone B tra ciascuna acquisizione di immagini. Ciascuna acquisizione di immagini è stata eseguita con un diverso filamento di imager Atto-647N (IS1 e IS2; Tabella supplementare 10). Il software Micro-Manager è stato utilizzato per acquisire 9,000 fotogrammi con frame di lettura da 10 MHz, esposizione di 200 ms e nessun guadagno di moltiplicazione degli elettroni (Nota integrativa e fig. supplementari 2 ed 3).
SPR
Per eseguire gli esperimenti SPR è stato utilizzato uno strumento Biacore T200 (Cytiva) e i dati sono stati acquisiti utilizzando il software di controllo del sistema Biacore T200 v. 2.01. L'ECD-IR biotinilato (Nordic BioSite) è stato immobilizzato su un chip sensore streptavidina SA (Cytiva). Il tampone HBS-P+ (Cytiva) è stato utilizzato come tampone di corsa. Dopo l'immobilizzazione dell'ECD-IR, è stato introdotto un tempo di stabilizzazione di 15 minuti per raggiungere una linea di base stabile. NR-1, NR-2, NR-4, NR-7, NR-15, NR-8 e NR-8dsDNA sono stati iniettati a una concentrazione di insulina di 11.4 nM nel buffer di corsa. L'insulina e l'INS-DNA sono stati iniettati a 55 nM, la concentrazione minima per ottenere una curva di legame che potesse essere analizzata. NR è stato iniettato come controllo negativo a una concentrazione pari alla concentrazione più alta di NanoRod utilizzata nelle iniezioni di insulina NanoRod (NR-1 = 11.4 nM). In alternativa, NR-2, NR-4, NR-7 e NR-15 sono stati iniettati ad una concentrazione di nanostruttura di 5.7 nM (Dati estesi Fig. 4e) e NR-7K-PEG è stata anche iniettata una concentrazione di insulina di 50 nM (Dati estesi Fig. 9c). L'iniezione di ciascun campione è stata eseguita utilizzando una fase di associazione di 180 s e una fase di dissociazione di 300 s. La costante di equilibrio di dissociazione (KD), costante del tasso di associazione (kon) e costante del tasso di dissociazione (kMENO) sono stati determinati utilizzando il software BIAevaluation 3.0. IL t1/2 i valori, che definiscono il tempo di permanenza, sono stati determinati utilizzando la formula ln2/kMENO. Per confrontare il legame delle strutture NR-7 tra IR e IGF1R, le proteine ECD-IR e ECD-IGF1R (Nordic BioSite) sono state immobilizzate su due diverse celle a flusso di un chip sensore CM5 tramite reazioni di accoppiamento amminico, secondo le istruzioni del produttore. Il legame dell'insulina e dell'INS-DNA è stato testato iniettando diverse concentrazioni di insulina (6.2, 18.5, 55.6, 166.7 e 500.0 nM) nel tampone di corsa (HBS-P+) in modalità cinetica a ciclo singolo, utilizzando una fase di associazione di 140 s e una fase di dissociazione di 300 s. Il legame di NR-7 è stato testato iniettando una singola concentrazione di struttura (11.4 nM di insulina) utilizzando una fase di associazione di 180 s e una fase di dissociazione di 300 s.
Gel Coomassie
Qui 0.5 µg di ECD-IR ricombinante (Nordic BioSite) sono stati risospesi nel tampone campione Laemmli (Bio-Rad). Per le condizioni riducenti, è stato aggiunto 2-mercaptoetanolo a una concentrazione finale del 2.5%. I campioni sono stati denaturati a 80 °C per 10 minuti, risolti mediante elettroforesi su gel di sodio dodecil solfato-poliacrilammide e colorati con il colorante proteico sicuro GelCode Blue (Thermo Fisher Scientific).
Saggio di spostamento del gel
I NanoRod (NR e NR-7) a 20 nM sono stati incubati con un dominio extracellulare ricombinante da 300 nM di IR umano (Nordic BioSite) o con PBS per 30 minuti a 4 °C. I campioni sono stati quindi analizzati su gel di agarosio al 2% e colorati con SYBR Safe.
immunoblotting
Le cellule sono state lavate con PBS, lisate in tampone di analisi di radioimmunoprecipitazione (Sigma-Aldrich) integrato con un cocktail di inibitori di proteasi e fosfatasi (Thermo Fisher Scientific) e incubate su ghiaccio con agitazione per 30 minuti. Il lisato è stato eliminato mediante centrifugazione (20,000×g per 20 minuti a 4 °C) e i lisati proteici sono stati quantificati utilizzando il dosaggio proteico Bradford (Bio-Rad). I lisati proteici sono stati risospesi nel tampone campione Laemmli (Bio-Rad) contenente il 2.5% di 2-mercaptoetanolo, denaturato a 80 °C per 10 minuti, risolti mediante elettroforesi su gel di sodio dodecil solfato-poliacrilammide e trasferiti su membrane di polivinilidene fluoruro. Le membrane sono state incubate per 1 ora in una soluzione bloccante (soluzione salina tamponata con Tris con 0.1% Tween 20 (TBST) e 5.0% latte in polvere senza grassi), seguita da incubazione notturna a 4 °C con anticorpi primari contro fosfo-IR beta/IGF1R beta (CST 3024, 1:1,000), fosfo-AKT-S473 (CST 4058, 1:1,000) o GAPDH (Invitrogen PA1-987, 1:5,000). Dopo tre lavaggi con TBST, le membrane sono state incubate con anticorpi secondari coniugati con perossidasi di rafano (Invitrogen, 31460, 1:5,000) per 1 ora a temperatura ambiente. Il rilevamento della perossidasi di rafano è stato eseguito mediante il substrato chemiluminescente Immobilon Forte su un sistema di imaging ChemiDoc (Bio-Rad). La densiometria a banda è stata eseguita utilizzando il software ImageJ.
Citometria a flusso
Gli adipociti differenziati e privati di siero sono stati preparati come descritto sopra. Gli adipociti sono stati successivamente lavati due volte con soluzione salina bilanciata di Hanks (HBSS) e dissociati in soluzione di collagenasi D (1.5 U ml-1 collagenasi D (Roche) e CaCl 10 mM2 in HBSS) per 20 minuti a 37 °C. Le cellule sono state risospese in HBSS, filtrate attraverso un filtro cellulare bilanciato con HBSS da 35 µm (BD Biosciences), pellettizzate a 300×g per 5 minuti e risospesi in un tampone di colorazione (1× PBS e 1% di albumina di siero bovino). Le cellule morte sono state etichettate con il kit LIVE/DEAD Fixable Yellow Dead Cell Stain Kit (Thermo Fisher Scientific) secondo le istruzioni del produttore e, successivamente, la sospensione cellulare è stata pellettizzata a 300×g per 5 minuti e risospesi nel tampone di colorazione. Qui circa 100,000 cellule sono state incubate con strutture NanoRod marcate con ATTO-10 da 647 nM in un volume finale di 100 µl per 10 minuti a 37 °C. Le cellule incubate senza le strutture NanoRod sono state utilizzate come controllo non trattato. Le cellule sono state poi lavate due volte con il tampone di colorazione mediante centrifugazione a 300×g per 5 minuti Le misurazioni della citometria a flusso sono state eseguite su un BD FACSCANTO II con il software BD FACSDIVA v. 9.0 (BD Biosciences). Le cellule di adipociti vivi sono state inizialmente identificate mediante gating su FSC-A rispetto a AmCyan-A, seguito da gating su FSC-A rispetto a FSC-H per rilevare singoletti. I dati acquisiti sono stati analizzati utilizzando il software FlowJo 10.7.1 (BD Biosciences). La media geometrica dell'intensità della fluorescenza dopo la normalizzazione rispetto al controllo non trattato è stata utilizzata per definire il grado di etichettatura cellulare da parte dei NanoRod.
Preparazione e sequenziamento della libreria RNA-seq
L'RNA totale è stato isolato dagli adipociti differenziati utilizzando il kit Quick-RNA Microprep Plus (Zymo Research) e 500 ng di RNA purificato sono stati utilizzati per la preparazione della libreria mRNA-seq utilizzando TruSeq RNA Library Prep Kit v2 secondo il protocollo a basso campione del produttore. La quantificazione della libreria è stata eseguita utilizzando il sistema QuantiFluor dsDNA (Promega) secondo il protocollo della piastra multipozzetto del produttore su un lettore di micropiastre multimodale Varioskan LUX (Thermo Fisher). Le dimensioni e la qualità della libreria sono state valutate utilizzando Bioanalyser 2100 e High Sensitivity DNA Kit (Agilent). Le librerie sono state denaturate e diluite utilizzando il protocollo di normalizzazione standard NextSeq (Illumina) e il sequenziamento è stato eseguito utilizzando letture single-end (1 × 75 bp) con NextSeq 500/550 High Output Kit v. 2.5 (75 cicli) su una piattaforma NextSeq 550 ( Illumina).
Quantificazione dell'RNA-seq, analisi DEG e GSEA
Le letture del sequenziamento sono state mappate rispetto a un trascrittoma di riferimento di Mus musculus sequenze di trascrizione codificanti proteine (rilascio M29, GRCm39; https://www.gencodegenes.org/mouse/) e quantificato utilizzando Salmon 1.7.0 (rif. 33). Le tabelle di conteggio sono state generate utilizzando il pacchetto tximport34 e gli elenchi di DEG sono stati ottenuti utilizzando il pacchetto DESeq2 (v. 1.34.0)35, dove solo i geni sono modificati P valori uguali o inferiori a 0.001 e un log2Per ulteriori analisi è stato considerato il cut-off di modifica della piega a ±0.58. Le mappe di calore e i grafici UpSet sono stati generati utilizzando ComplexHeatmap (v. 2.10.0)36. Il GSEA per i processi biologici con termini di Gene Ontology e percorsi KEGG è stato eseguito utilizzando un elenco classificato di geni come input per clusterProfiler (v. 4.2.2)37 e un significato aggiustato per il tasso di false scoperte P valori inferiori a 0.10 e 0.05, rispettivamente.
Microiniezioni di pesce zebra e quantificazione del glucosio libero
NanoRod e NanoRod di insulina sono stati miscelati con oligolisina-PEG (K10-PEG5K, Alamanda Polymers) in rapporto 1:1 tra le ammine della lisina in K10-PEG5K e i fosfati nel DNA30e incubato a temperatura ambiente per 30 minuti prima di una microiniezione di 2 nl del campione in ciascuna larva di pesce zebra. I campioni per l'iniezione sono stati preparati ad una concentrazione finale di 100 nM di strutture per i campioni NanoRod rivestiti e ad una concentrazione finale di 100 nM di insulina per i campioni NanoRod rivestiti di insulina (corrispondenti a 100.0 e 14.3 nM di NanoRod per NR-1K-PEG e NR-7K-PEG, rispettivamente). È stato dimostrato che l'iniezione di 1 nl di insulina umana a una concentrazione di 100 nM nelle larve di pesce zebra induce una diminuzione dei livelli di glucosio libero e cambiamenti trascrizionali coerenti con la segnalazione dell'insulina38. Pertanto, nei nostri test abbiamo iniettato 2 nl di concentrazione di insulina 100 nM per valutare gli effetti mediati dall'insulina sui livelli di glucosio libero. Poiché il volume totale del sangue per un pesce zebra da 2 dpf è 60–89 nl (rif. 39), la concentrazione stimata dell'insulina iniettata nei nostri test sarebbe di circa 2–3 nM. In questi test, eravamo limitati anche nella quantità di campione iniettato, con livelli di iniezione più elevati (3 e 4 nl) con conseguente scarsa sopravvivenza delle larve.
Il mantenimento e l'incrocio del pesce zebra (D.rerio) le linee sono state realizzate in conformità alla legislazione svedese sul benessere degli animali approvata dallo Stockholms djurförsöksetiska nämnd. Poiché per gli esperimenti di ablazione delle cellule β e di analisi del glucosio libero sono stati utilizzati solo animali di età inferiore a 5 giorni, non è stato richiesto alcun permesso etico secondo 2010/63/UE. Le linee transgeniche di pesce zebra utilizzate sono state precedentemente descritte, vale a dire: Tg(ins:CFP-NTR)s892 (Rif. 27) e Tg(ins:Kaede)s949 (Rif. 28).
L'ablazione delle cellule β è stata eseguita in bambini di due giorni Tg(ins:CFP-NTR) e Tg(ins:CFP-NTR);Tg(ins:Kaede) embrioni mediante trattamento con 10 mM MTZ (Sigma-Aldrich) diluito in 1% DMSO (VWR) in una soluzione di acqua di uovo (E3) integrata con 0.2 mM 1-fenil-2-tiourea (PTU, Acros Organics) per 24 ore. Dopo l'ablazione delle cellule β, a tre giorni Tg(ins:CFP-NTR) le larve (72 hpf) sono state anestetizzate in tricaina allo 0.01% e iniettate con 2 nl di 1× PBS, insulina non modificata o NanoRod/insulina NanoRod rivestiti nella vena cardinale comune (dotto di Cuvier)40. Rosso fenolo (Sigma-Aldrich) a una concentrazione finale dello 0.1% è stato aggiunto ai campioni NanoRod di PBS, insulina o insulina rivestita per facilitare la visualizzazione del processo di microiniezione e la determinazione delle larve iniettate con successo. Le larve di pesce zebra sono state assegnate in modo casuale ai gruppi di trattamento. I livelli di glucosio libero sono stati misurati come descritto altrove41 utilizzando un kit enzimatico a base di fluorescenza (BioVision). Sono stati utilizzati gruppi da tre a sei larve iniettate per condizione/replica.
Imaging confocale
Tg(ins:CFP-NTR);Tg(ins:Kaede)-ablate le larve sono state raccolte 24 ore dopo il trattamento di ablazione, anestetizzate e iniettate seguendo il protocollo precedentemente indicato e fissate in una soluzione di paraformaldeide al 4% prima di analizzare i numeri di cellule β mediante imaging confocale. Le immagini confocali sono state acquisite con un microscopio Leica TCS SP8 e il software LAS X (v. 3.5.5.19976). Le isole pancreatiche primarie delle cellule β sono ablate Tg(ins:CFP-NTR);Tg(ins:Kaede) le larve sono state scansionate con un obiettivo a immersione in acqua ×40 e il z gli stack sono stati analizzati utilizzando il software Fiji (v1.53). Tutte le immagini visualizzate sono state acquisite dallo stesso esperimento e i loro valori di contrasto sono stati regolati a scopo di visualizzazione. La quantificazione delle cellule β è stata eseguita su immagini originali non modificate.
analisi statistica
Non sono stati utilizzati metodi statistici per predeterminare le dimensioni del campione, ma le dimensioni del campione erano simili a quelle riportate nelle pubblicazioni precedenti28,38,42. Campioni di colture cellulari e animali sono stati assegnati in modo casuale ai gruppi di controllo e di trattamento. La raccolta e l'analisi dei dati non sono state eseguite in modo cieco rispetto alle condizioni degli esperimenti. I singoli punti dati vengono tracciati per la maggior parte dei grafici. Misura di prova (n) del numero di ripetizioni biologiche sperimentali e i metodi statistici utilizzati sono indicati nelle legende delle figure corrispondenti. I set di dati sono stati testati per la distribuzione gaussiana seguita dal test statistico appropriato. L'analisi statistica e la rappresentazione grafica dei dati sono state elaborate con GraphPad Prism 9.4.0. È stato eseguito il test di Mann-Whitney a due code per confrontare le proprietà del cluster tra le cellule di controllo e quelle trattate con insulina. Per le quantificazioni Western Blot è stata effettuata l'analisi della varianza unidirezionale (ANOVA) seguita dal test di confronti multipli di Dunnett. Per la quantificazione delle cellule β è stato effettuato il test di Kruskal-Wallis seguito dal test di confronti multipli di Dunn. L'analisi dei valori di glucosio libero è stata eseguita utilizzando ANOVA unidirezionale con il test di confronti multipli di Tukey.
Reporting summary
Ulteriori informazioni sulla progettazione della ricerca sono disponibili nel Riepilogo dei rapporti sul portafoglio naturalistico collegato a questo articolo.
- Distribuzione di contenuti basati su SEO e PR. Ricevi amplificazione oggi.
- PlatoData.Network Generativo verticale Ai. Potenzia te stesso. Accedi qui.
- PlatoAiStream. Intelligenza Web3. Conoscenza amplificata. Accedi qui.
- PlatoneESG. Carbonio, Tecnologia pulita, Energia, Ambiente, Solare, Gestione dei rifiuti. Accedi qui.
- Platone Salute. Intelligence sulle biotecnologie e sulle sperimentazioni cliniche. Accedi qui.
- Fonte: https://www.nature.com/articles/s41565-023-01507-y
- :ha
- :È
- :non
- :Dove
- ][P
- 000
- 001
- 01
- 1
- 1: Rapporto 1
- 10
- 100
- 11
- 12
- 125
- 13
- 14
- 15%
- 150
- 180
- 19
- 2%
- 20
- 200
- 2000
- 2006
- 2011
- 2012
- 2014
- 2015
- 2016
- 2017
- 2020
- 2021
- 2022
- 22
- 23
- 24
- 25
- 26
- 27
- 28
- 30
- 300
- 32
- 33
- 35%
- 36
- 39
- 40
- 400
- 41
- 50
- 500
- 58
- 60
- 7
- 70
- 72
- 75
- 8
- 80
- 87
- 9
- 90
- a
- ABC
- sopra
- Secondo
- acquisire
- acquisito
- acquisizione
- Action
- Attivazione
- aggiunto
- l'aggiunta di
- aggiunta
- aggiuntivo
- Rettificato
- Dopo shavasana, sedersi in silenzio; saluti;
- contro
- aiuto
- ARIA
- AL
- Tutti
- allocato
- anche
- quantità
- an
- analisi
- .
- Presentatrice
- ed
- animali
- animali
- Anticorpi
- anticorpo
- AMMISSIONE
- opportuno
- approvato
- circa
- SONO
- in giro
- articolo
- AS
- valutare
- valutato
- addetto
- Associazione
- At
- Atmosfera
- allegato
- disponibile
- b
- balanced
- BAND
- base
- basato
- Linea di base
- basic
- BD
- BE
- Larghezza
- stato
- prima
- essendo
- sotto
- vantaggi
- beta
- fra
- rilegatura
- biotech
- cieco
- bloccato
- blocco
- sangue
- Blu
- Bolt
- entrambi
- Parte inferiore
- BP
- ampio
- pelle
- bufferizzare
- ma
- by
- calcolato
- stanza
- Cardinale
- svolta
- cella
- Celle
- centro
- catena
- Catene
- il cambiamento
- cambiato
- Modifiche
- chimica
- patata fritta
- Chips
- clicca
- Cluster
- cocktail
- COERENTE
- collezione
- Colonna
- colonne
- Uncommon
- COMP
- confrontare
- rispetto
- confronto
- confronto
- complementare
- complesso
- conformità
- componenti
- composto
- concentrazione
- concentratore
- condizione
- condizionale
- condizioni
- condotto
- Configurazione
- confluenza
- considerato
- coerente
- costante
- contrasto
- di controllo
- convertito
- Rame
- correlazioni
- Corrispondente
- potuto
- Craig
- creato
- incrocio
- Cultura
- curva
- costume
- cicli
- dati
- punti dati
- dataset
- Giorni
- morto
- diminuire
- Predefinito
- definire
- Laurea
- consegna
- densità
- descritta
- Design
- individuare
- rivelazione
- determinazione
- determinato
- Dev
- in via di sviluppo
- sviluppo
- dispositivo
- diverso
- diversificato
- diluito
- diluizione
- Dispersione
- visualizzati
- Rottura
- distribuzione
- dna
- dominio
- fatto
- asciugare
- dinamico
- e
- E&T
- e3
- ogni
- effetti
- emissione
- finisce
- ambienti
- enzimatica
- pari
- equilibrio
- attrezzato
- stimato
- stime
- Etere (ETH)
- etico
- valutare
- Ogni
- eccesso
- scambiati
- ampliato
- espansione
- esperimento
- sperimentale
- esperimenti
- Esposizione
- esprimere
- espressione
- estendendo
- FAST
- Grasso
- campo
- Fico
- figura
- filtro
- finale
- Nome
- cinque
- fisso
- flusso
- fluido
- Focus
- seguito
- i seguenti
- Nel
- forza
- formato
- formazione
- formula
- Forte
- quattro
- TELAIO
- Gratis
- da
- congelati
- funzionalmente
- ulteriormente
- G2
- Guadagno
- Gen
- generato
- genoma
- vetro.
- Oro
- grafici
- Griglia
- Gruppo
- Gruppo
- Crescita
- harvard
- Università di Harvard
- Avere
- qui
- Alta
- Alte prestazioni
- superiore
- massimo
- http
- HTTPS
- umano
- i
- ICE
- identificato
- ii
- Immagine
- immagini
- Imaging
- immune
- competenze
- in
- incorporando
- è aumentato
- incubato
- Incubando
- INCUBAZIONE
- studente indipendente
- indicato
- individuale
- induzione
- infezione
- informazioni
- inizialmente
- ingresso
- istruzioni
- strumento
- strumenti
- integrato
- interno
- ai miglioramenti
- introdotto
- isolato
- da solo
- KDA
- kit
- etichettatura
- Larva
- LAS
- laser
- a sinistra
- Legends
- Legislazione
- livelli
- biblioteche
- Biblioteca
- leggera
- Limitato
- linea
- Linee
- LINK
- connesso
- Liquido
- Lista
- elenchi
- vivere
- amore
- Basso
- fatto
- Principale
- manutenzione
- Maps
- massiccio
- materiale
- significare
- misurato
- misurazioni
- di misura
- Media
- medie
- Merck
- metabolica
- metodo
- metodi
- metodi erano
- Mica
- Microscopio
- latte
- verbale
- ordine
- Mishra
- scelta
- misto
- mescola
- Miscelazione
- MJ
- ML
- Moda
- modellismo
- modifiche
- modificato
- modulo
- maggior parte
- mouse
- MS
- multiplo
- cioè
- nanotecnologia
- nativo
- Natura
- negativo.
- New
- NHS
- no
- romanzo
- numero
- numeri
- obiettivo
- ottenere
- ottenuto
- of
- on
- una volta
- esclusivamente
- su
- ontologia
- ottica
- ottimizzati
- or
- biologico
- i
- nostro
- su
- produzione
- ancora
- per una notte
- Oxygen
- pacchetto
- dipingere
- parametri
- Passato
- percorsi
- modelli
- PBS
- per
- per cento
- perfetta
- eseguire
- eseguita
- fase
- forare
- pixel
- posto
- piano
- plastica
- piattaforma
- Platone
- Platone Data Intelligence
- PlatoneDati
- più
- pm
- punti
- Polimeri
- povero
- lavori
- previsto
- preliminare
- preparazione
- preparato
- precedente
- in precedenza
- primario
- procedura
- processi
- elaborati
- i processi
- Prodotto
- Produzione
- Profilo
- promuoverlo
- promuove
- proprietà
- Proteine
- Proteine
- protocollo
- purché
- fornisce
- fini
- qualità
- quantificazione
- qubit
- R
- Coniglio
- classificato
- tasso
- rapporto
- Crudo
- raggiungere
- Reagire
- reazione
- reazioni
- Lettore
- Rosso
- Ridotto
- riducendo
- riferimento
- riflessione
- rigenerazione
- normativa
- relax
- rilasciare
- rimuovere
- rimosso
- rimozione
- ripetuto
- Segnalati
- Reportistica
- rappresentazione
- necessario
- riparazioni
- Residenza
- resistenza all'usura
- risoluto
- risposte
- risultante
- rivelare
- Anello
- RNA
- roccia
- Prenotazione sale
- rt
- Correre
- running
- s
- SA
- sicura
- sale
- stesso
- scientifico
- secondario
- selezionato
- selettivo
- Sensibilità
- Sequenza
- sequenziamento
- Siero
- server
- Sette
- spostamento
- mostrato
- Sigma
- significato
- Argento
- simile
- simulazione
- simulazioni
- da
- singolo
- site
- Siti
- SIX
- Taglia
- Dimensioni
- scivolo
- Lentamente
- piccole
- sodio
- Software
- soluzione
- sp
- spun
- stabile
- Stacks
- Standard
- standard
- ha dichiarato
- statistiche
- step
- Passi
- memorizzati
- Strands
- La struttura
- strutture
- studi
- presentata
- Successivamente
- Con successo
- repressione
- superficie
- sopravvivenza
- sospensione
- svedese
- sistema
- SISTEMI DI TRATTAMENTO
- T
- tavolo
- preso
- Talos
- mirata
- Tecnologie
- Tecnologia
- carnagione
- condizioni
- test
- testato
- testo
- di
- che
- I
- loro
- poi
- perciò
- termico
- Strumenti Bowman per analizzare le seguenti finiture:
- questo
- quelli
- tre
- Attraverso
- tempo
- volte
- a
- strumenti
- Totale
- Tracer
- Trascrizione
- trasferito
- trattamento
- tritone
- Due volte
- seconda
- Ultra
- unità
- universale
- Università
- fino a quando
- uso
- utilizzato
- utilizzando
- v1
- Vuoto
- APPREZZIAMO
- Valori
- contro
- via
- Video
- visualizzazioni
- visualizzazione
- visualizzare
- visivamente
- vivo
- volatile
- volume
- W
- Prima
- lavaggio
- Water
- we
- sito web
- web server
- Benessere
- WELL
- Wells
- sono stati
- Occidentale
- quale
- con
- entro
- senza
- sarebbe
- wu
- X
- giallo
- Minore
- zefiro