L'8 dicembre il National Institute of Standards and Technology (NIST) degli Stati Uniti ha pubblicato delle linee guida che invitano a commentare l'uso della marcia nei diritti. Lo stagista di SpicyIP Jyotpreet Kaur scrive su questi diritti, sui cambiamenti proposti nelle linee guida e sulla posizione dell'India su accordi simili. Questo post è stato scritto con il contributo di Swaraj. Jyotpreet è uno studente di giurisprudenza del terzo anno della National Law University di Delhi, interessato ai diritti di proprietà intellettuale e al diritto della concorrenza e cerca di studiare la loro interazione reciproca. È possibile accedere ai suoi post precedenti qui.

La revisione dei diritti di marcia da parte degli Stati Uniti e alcune domande su una controparte indiana
Di Jyotpreet Kaur
Come molti lettori sapranno, il governo degli Stati Uniti, soprattutto attraverso l’ufficio del rappresentante commerciale statunitense, ha perseguitato l’India per anni dopo la concessione di un’unica licenza obbligatoria, sottoposta a un attento controllo giudiziario. È stato solo durante il COVID-19 questa pressione ha smesso di essere applicata in modo così sfacciato (con uno spostamento invece verso i “segreti commerciali”). Con una svolta molto interessante degli eventi, sembra che gli Stati Uniti stiano ora spingendo verso linee guida che ampliano il modo in cui gli Stati Uniti possono applicare la propria versione di licenze obbligatorie, ovvero i diritti di “march-in”, a livello nazionale! Sembra che la pressione interna derivante dai costi sanitari in costante aumento abbia raggiunto un punto tale da consentire finalmente un riesame del modo in cui il loro sistema di brevetti influisce sui costi. L’8 dicembre, il National Institute of Standards and Technology (NIST) ha pubblicato la bozza linee guida invitando commenti sull’uso dei diritti di “March-In” a sostegno dell’obiettivo dell’amministrazione Biden di abbassare i prezzi dei farmaci. Secondo il NIST, il governo degli Stati Uniti investe circa 115 miliardi di dollari in ricerca e sviluppo attraverso varie università, organizzazioni no-profit e imprese. I diritti di marzo sono disposizioni che consentono al governo di richiedere una licenza per le invenzioni derivanti da questo investimento, previo adempimento di determinate condizioni. In particolare, sebbene la “minaccia” dei diritti March-In sia stata menzionata in precedenza, essi non sono stati effettivamente esercitati nei 44 anni trascorsi dall’entrata in vigore della legge governativa. L'obiettivo di questo progetto di linee guida sembra essere l'ampliamento dei criteri in base ai quali è possibile esercitare i diritti di marcia. Il Segretario americano alla sanità e ai servizi umani salutato questo come “potente strumento per garantire che il contribuente americano ottenga un giusto ritorno sul proprio investimento”,
Bilanciare innovazione e interesse pubblico: gli obiettivi del Bayh-Dole Act rispetto ai diritti di March-in
La legge Bayh-Dole, promulgata nel 1980, ha messo in primo piano, tra le altre cose, i diritti di “march-in” del governo federale. Come accennato in precedenza, i diritti di March-in sono simili a misure intrinseche a disposizione del governo nel caso in cui coloro che sviluppano i diritti di proprietà intellettuale a partire dalla ricerca finanziata dal governo non abbiano adeguatamente commercializzato la proprietà intellettuale. Nell’esercitare questo potere, i governi possono intervenire e dirigere l’uso dei diritti di proprietà intellettuale o concederli in licenza a terzi. La proprietà del brevetto rimane all'istituto: è solo un diritto di licenza a terzi che matura a favore dello Stato se sceglie di esercitare questo diritto. Lo scopo di questo diritto è consentire al governo di realizzare appieno il potenziale dei diritti di proprietà intellettuale in questione finanziati con fondi pubblici nel caso in cui siano sottoutilizzati dall'istituto inventore.
L'esercizio dei diritti di March-in ai sensi del Bayh-Dole Act è previsto dall'articolo 35 U.S.C. § 203, che richiede il rispetto di 4 criteri statutari. Questi sono (i) non riuscire a realizzare efficacemente l'innovazione in oggetto; (ii) la necessità di alleviare le esigenze di salute o sicurezza non soddisfatte; (iii) mancato rispetto dei requisiti di pubblica fruizione dell'invenzione; e (iv) inadempimento degli obblighi contrattuali, in particolare ai sensi dell'art. 204., che richiede che i prodotti brevettati siano fabbricati in modo significativo negli Stati Uniti fino a quando ciò non sarà commercialmente fattibile.
Ad oggi, il governo degli Stati Uniti non ha esercitato il diritto di marcia, nonostante le petizioni che chiedevano lo stesso. È stata la prima volta che è stata presentata una petizione per l'esercizio dei diritti di March-in riferendosi a CellPro dove il governo ha rifiutato di esercitare questo diritto. Questa tendenza continua fino ad oggi, come si può vedere dal otto petizioni che sono stati depositati davanti al NIH e sono stati eliminati.
Rinnovare i diritti di marcia: una ricetta per il disastro o una formula per il successo?
Uno dei cambiamenti introdotti attraverso le linee guida è stato quello di chiarire il processo di consultazione informale dell'agenzia con l'appaltatore prima dell'esercizio dei diritti di entrata e di aumentare il periodo di tempo consentito a disposizione di un'agenzia per rispondere all'appaltatore in seguito alla consultazione informale da 60 a 120 anni. giorni a XNUMX giorni.
Oltre a questo, le nuove linee guida introducono un metodo in tre fasi che sembra chiarire il processo per invocare il diritto di marcia (vedi immagine). Innanzitutto bisogna vedere se alle invenzioni in questione si applica la legge Bayh-Dole: qui si verifica se le invenzioni sono "invenzioni-oggetto" e se sono finanziate dal governo. In secondo luogo, se uno qualsiasi dei quattro criteri statutari, come menzionato sopra, sia applicabile al caso in questione e, infine, se l’esercizio dei diritti di marcia sia conforme allo spirito generale della legislazione Bayh-Dole e ai suoi obiettivi.
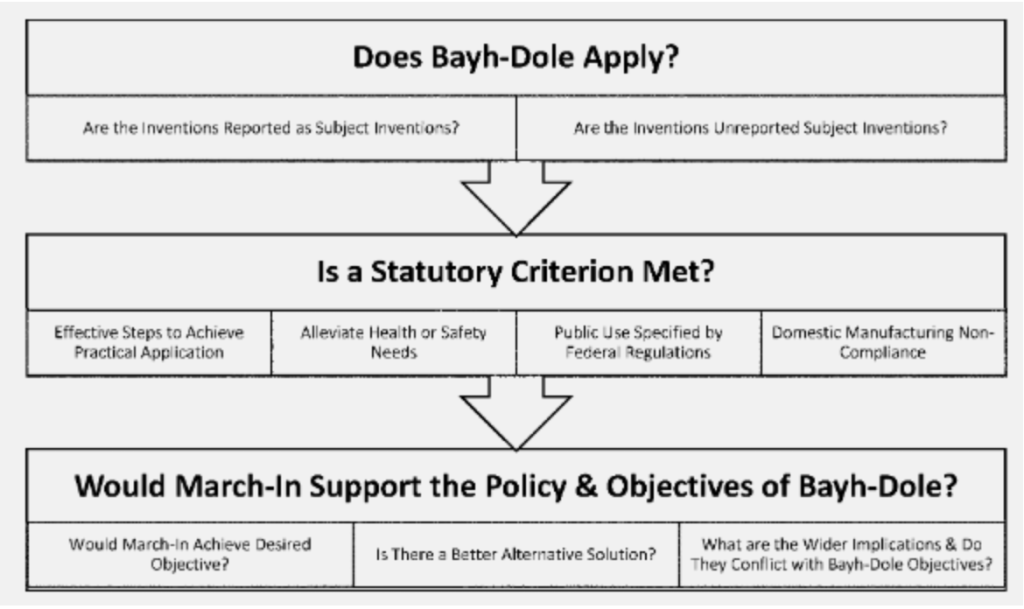
Forse il cambiamento più importante si vede nella seconda fase in cui si invoca il primo criterio statutario, vale a dire quando il titolare del brevetto non è riuscito o non riuscirà a intraprendere misure efficaci per la realizzazione dell '"innovazione in oggetto" nel suo campo di utilizzo. Le linee guida hanno aggiunto una considerazione di fattori che potrebbero "limitare irragionevolmente la disponibilità dell'invenzione al pubblico". In questo caso, le linee guida hanno introdotto un requisito di prezzi ragionevoli che in precedenza non era riconosciuto come criterio per l'esercizio dei diritti di “March-in”. Le linee guida comportano la questione se “l’appaltatore o il licenziatario abbiano reso il prodotto disponibile solo a un gruppo ristretto di consumatori o clienti a causa dei prezzi elevati”.
Ciò è in contrasto con la precedente posizione del governo, che può essere evidenziata dalle sue precedenti interazioni con i prezzi elevati come motivo per esercitare la marcia in avanti. Nel 2004, il firmatario ha spinto l'NIH a ricorrere a questa misura a causa del prezzo elevato di un farmaco per il trattamento dell'HIV chiamato Norvir e un farmaco per il trattamento del glaucoma intitolato Xalatan. Nel 2012, la preoccupazione per il prezzo elevato di Norvir è stato nuovamente sollevato davanti al NIH. Anche in questo caso, nel 2016, i firmatari hanno espresso preoccupazione riguardo al prezzo elevato del Xtandi farmaco che costa circa 98 dollari a pillola rispetto ad altri paesi ad alto reddito. Tuttavia, in tutti questi casi, gli NIH si sono rifiutati di esercitare i propri diritti di ingresso semplicemente sulla base dei prezzi, adducendo altre ragioni per rifiutarsi di farlo.
Laddove le linee guida parlano di prezzi ragionevoli, non specificano quale possa essere un prezzo “ragionevole”, lasciandolo alla discrezione del governo federale.
I sostenitori acclamano queste linee guida come misure progressiste per rendere i farmaci esorbitanti più accessibili al grande pubblico americano e per restituire al pubblico ciò che è “di diritto” suo poiché la ricerca finanziata a livello federale è essenzialmente coperta utilizzando il denaro dei contribuenti.
D’altro canto, coloro che si oppongono alle linee guida sostengono che queste sono antitetiche agli obiettivi della legge Bayh-Dole poiché la fissazione dei prezzi non è mai stata considerata come motivo per esercitare i diritti di “March-in”. La Camera di Commercio degli Stati Uniti ha definito queste linee guida una forma di “confisca governativa”. Altri sostengono che una clausola del genere ostacolerebbe l’innovazione e la concorrenza, che sono gli obiettivi primari della legge. Alcuni hanno sostenuto che l’obiettivo della legge era quello di incoraggiare la collaborazione tra il settore pubblico e quello privato allo scopo di introdurre nuove idee nel mercato, a differenza di ciò che le presenti linee guida cercano di ottenere: alleviare i problemi di accesso ai farmaci e le inefficienze del mercato. Joseph Allen ha anche sostenuto che queste linee guida sono una "pillola avvelenata" poiché, sebbene siano mirate a prendere di mira le "grandi aziende farmaceutiche", finiranno per danneggiare i piccoli inventori che sono effettivamente coperti dalla legge Bayh-Dole perché la maggior parte delle "Big-Pharma" la ricerca non è finanziata dal governo. Allo stesso tempo, sostiene che queste linee guida sono state formulate tenendo presente (solo) gli alti prezzi dei farmaci, e ignorando che il Bayh-Dole copre anche altri settori come l’energia, l’agricoltura e la protezione dell’ambiente che saranno ora colpiti dalla crisi. avversità di queste linee guida.
Cosa sta succedendo sul fronte indiano?
Ora che questo dibattito viene preso più seriamente negli Stati Uniti, ciò avrà degli effetti di ricaduta in India? Sebbene le flessibilità cartacee dell’India in materia di brevetti siano piuttosto solide e alcune, come la Sezione 3(d), abbiano fatto sentire la loro presenza, dobbiamo ancora vedere la traduzione o la pratica di molte altre disposizioni in effetti nel mondo reale. Ad esempio, nonostante si sia discusso di licenze obbligatorie per un paio di altri farmaci, da queste discussioni non è venuto fuori nulla. Non è chiaro quanto di ciò sia dovuto a pressioni esterne, ad esempio, vari accordi di libero scambio e, naturalmente, l’USTR; e quanto di questo è probabilmente dovuto ad altri motivi. Ad esempio, sebbene l’India sia stata tra quelli in prima linea nel chiedere deroghe sulla proprietà intellettuale durante la pandemia di Covid-19, ironicamente, a livello interno, sebbene il governo avesse un numero di opzioni che avrebbe potuto prendere, non è stata intrapresa molta azione. Ad esempio, il governo non ha provveduto chiarezza sulla titolarità dei diritti di proprietà intellettuale (Covaxin) e il suo atto di “concedere l’approvazione” all’Istituto Haffkine erano qualcosa che avrebbe dovuto essere minato dall’interesse pubblico per il “diritto alla salute”, come è stato sostenuto qui ed qui. Allo stesso modo, il governo indiano si era rifiutato di divulgare i dati della sperimentazione clinica tramite RTI citando la Sezione 8(1)(d) ed (e) che prevede i diritti di proprietà intellettuale come motivo per esentare la divulgazione. Lo Stato ha invocato la tutela dei diritti di proprietà intellettuale rifiutando la pubblicazione dei dati senza impegnarsi nell'atto di bilanciamento di tale tutela rispetto all'interesse pubblico in gioco (che è stato previsto anche nella S. 39(3) del TRIPS). Pertanto, lo Stato non è riuscito a esercitare la propria proprietà intellettuale in modo aperto, in contrasto con la sua posizione internazionale.
Indipendentemente da ciò, la discussione interna degli Stati Uniti su qualcosa contro cui fino ad oggi hanno assunto forti posizioni internazionali, è uno sviluppo interessante da seguire. A livello nazionale, il Dipartimento di Biotecnologia ha recentemente pubblicato una propria serie di linee guida sulla proprietà intellettuale per le invenzioni derivanti dai finanziamenti DBT. Come va e questo segna l’inizio di un altro tentativo di resuscitare la fallita “Protezione e utilizzo della legge sulla proprietà intellettuale finanziata con fondi pubblici”? Allo stesso tempo, il governo ha deciso di adottare una decisione Politica nazionale in materia di ricerca, sviluppo e innovazione nel settore farmaceutico-medtech (vedi il progetto di politica qui) nel settembre 2023 per “trasformare” il settore farmaceutico indiano e “catalizzare” la ricerca e lo sviluppo in questi settori in un duplice modo: rafforzando le infrastrutture di ricerca e promuovendo la ricerca nel settore farmaceutico. In particolare, questa politica non affronta affatto le questioni relative alla proprietà intellettuale. Forse queste sono tutte domande su cui vale la pena riflettere e su cui proveremo a mettere insieme un post separato!
- Distribuzione di contenuti basati su SEO e PR. Ricevi amplificazione oggi.
- PlatoData.Network Generativo verticale Ai. Potenzia te stesso. Accedi qui.
- PlatoAiStream. Intelligenza Web3. Conoscenza amplificata. Accedi qui.
- PlatoneESG. Carbonio, Tecnologia pulita, Energia, Ambiente, Solare, Gestione dei rifiuti. Accedi qui.
- Platone Salute. Intelligence sulle biotecnologie e sulle sperimentazioni cliniche. Accedi qui.
- Fonte: https://spicyip.com/2024/01/the-us-review-of-march-in-rights-and-some-questions-on-an-indian-counterpart.html
- :ha
- :È
- :non
- :Dove
- $ SU
- 1
- 120
- 1st
- 20
- 2012
- 2016
- 2023
- 203
- 35%
- 41
- 60
- 8
- 8°
- a
- WRI
- sopra
- accesso
- accessibile
- accessibile
- Secondo
- Raggiungere
- Legge
- Action
- effettivamente
- aggiunto
- indirizzo
- adeguatamente
- che interessano
- Dopo shavasana, sedersi in silenzio; saluti;
- ancora
- contro
- agenzia
- agricoltura
- Mirato
- Tutti
- alleviare
- consentire
- anche
- Sebbene il
- americano
- tra
- tra
- an
- ed
- Un altro
- in qualsiasi
- appare
- applicabile
- applicato
- si applica
- APPLICA
- circa
- SONO
- discutere
- sostenuto
- sostiene
- in giro
- accordi
- AS
- chiedendo
- At
- tentativo
- Authored
- disponibilità
- disponibile
- precedente
- bilanciamento
- BE
- perché
- stato
- prima
- Inizio
- essendo
- fra
- Biden
- Miliardo
- portato
- aziende
- by
- detto
- è venuto
- Materiale
- Custodie
- casi
- certo
- Telecamera climatica
- il cambiamento
- Modifiche
- controllato
- condizioni
- citando
- Info su
- collaborazione
- Venire
- Commenti
- Commercio
- commercialmente
- rispetto
- concorrenza
- Problemi della Pelle
- preoccupazioni
- condizioni
- considerazione
- consultazione
- Consumatori
- continua
- Contraente
- contrattuale
- contrasto
- Costo
- Costi
- Controparte
- paesi
- Coppia
- corso
- coperto
- copre
- COVID-19
- Pandemia di COVID-19
- criteri
- Clienti
- dati
- Data
- Giorni
- dibattito
- Dicembre
- Delhi
- Shirts Department
- Nonostante
- in via di sviluppo
- Mercato
- dirette
- disastro
- Rilevare
- Rivelazione
- discrezione
- discussione
- discussioni
- do
- effettua
- Domestico
- bozza
- progetto di linee guida
- droga
- farmaci
- dovuto
- durante
- durante COVID-19
- e
- ogni
- In precedenza
- Efficace
- in maniera efficace
- effetti
- enable
- incoraggiare
- fine
- energia
- impegnandosi
- garantire
- Ambiente
- particolarmente
- essenzialmente
- Etere (ETH)
- eventi
- sempre crescente
- evidenziato
- esempio
- Esercitare
- Espandere
- espansione
- esterno
- Fattori
- FAIL
- fallito
- in mancanza di
- Fallimento
- fiera
- Federale
- Governo federale
- federalmente
- errore
- campo
- depositata
- Infine
- Nome
- prima volta
- in primo luogo
- seguire
- i seguenti
- Nel
- prua, testa
- prima linea
- modulo
- formula
- Avanti
- quattro
- TELAIO
- da
- anteriore
- completamente
- finanziati
- finanziamento
- Generale
- ottenere
- Dare
- scopo
- governo
- Enti Pubblici
- I governi
- Govt
- concesso
- Terra
- motivo
- linee guida
- ha avuto
- cura
- Happening
- nuocere
- Avere
- he
- Salute e benessere
- assistenza sanitaria
- suo
- qui
- qui
- Alta
- HIV
- Casa
- Come
- Tuttavia
- HTML
- HTTPS
- umano
- i
- idee
- if
- ii
- iii
- Immagine
- impattato
- importante
- in
- Aumento
- India
- indiano
- governo indiano
- industrie
- inefficienze
- informale
- Infrastruttura
- inerente
- Innovazione
- Ingressi
- esempio
- invece
- Istituto
- intellettuale
- proprietà intellettuale
- interazione
- interazioni
- interesse
- interessato
- interessante
- interno
- Internazionale
- intervenire
- ai miglioramenti
- introdurre
- introdotto
- l'introduzione di
- Invenzione
- invenzioni
- Inventori
- investimento
- investe
- invitante
- invocato
- IP
- ironicamente
- problema
- sicurezza
- IT
- SUO
- giudiziario
- conservazione
- Sapere
- Legge
- partenza
- Legislazione
- Livello
- licenza
- licenze
- Licenza
- piace
- LIMITE
- SEMBRA
- abbassamento
- fatto
- make
- modo
- manufatto
- molti
- Marzo
- marchio
- Rappresentanza
- max-width
- Maggio..
- misurare
- analisi
- Soddisfare
- menzionato
- metodo
- mente
- soldi
- Scopri di più
- maggior parte
- mosso
- molti
- stretto
- il
- Bisogno
- esigenze
- mai
- New
- NIH
- nista
- Non profit
- segnatamente
- Niente
- romanzo
- adesso
- obiettivo
- Obiettivi d'Esame
- obblighi
- of
- Office
- on
- quelli
- esclusivamente
- aprire
- opporsi
- Opzioni
- or
- Altro
- Altri
- su
- ancora
- complessivo
- proprio
- proprietà
- pandemia
- parti
- partito
- brevetto
- brevettato
- per
- Forse
- Pharma
- Pharmaceutical
- Platone
- Platone Data Intelligence
- PlatoneDati
- punto
- politica
- posizione
- posizioni
- forse
- Post
- Post
- potenziale
- energia
- pratica
- presenza
- presenti
- pressione
- precedente
- prezzo
- Prezzi
- prezzi
- primario
- Precedente
- un bagno
- processi
- Prodotto
- Prodotti
- progressivo
- promuovere
- proprietà
- Diritti di proprietà
- proposto
- protezione
- fornire
- purché
- la percezione
- Pubblicazione
- scopo
- spingendo
- metti
- domanda
- Domande
- abbastanza
- R&D
- sollevato
- a raggiunto
- lettori
- mondo reale
- ragionevole
- motivi
- recentemente
- ricetta
- ricetta per il disastro
- riconosciuto
- rifiutando
- rilasciato
- resti
- richiedere
- requisito
- Requisiti
- richiede
- riparazioni
- ricerca e sviluppo
- Rispondere
- risultante
- ritorno
- recensioni
- destra
- diritti
- robusto
- RTI
- s
- Sicurezza
- Suddetto
- stesso
- scrutinio
- Secondo
- segretario
- Sezione
- settore
- Settori
- vedere
- Cercare
- cerca
- sembra
- visto
- separato
- Settembre
- sul serio
- Servizi
- set
- spostamento
- dovrebbero
- significativamente
- simile
- Allo stesso modo
- semplicemente
- da
- singolo
- piccole
- So
- alcuni
- qualcosa
- parlare
- spillover
- spirito
- palo
- posizione
- standard
- Regione / Stato
- step
- Passi
- fermato
- potenziamento
- forte
- studente
- Studio
- soggetto
- il successo
- tale
- supporto
- Circostante
- sistema
- Fai
- preso
- mira
- Contribuente
- Tecnologia
- che
- Il
- Lo Stato
- loro
- Là.
- Strumenti Bowman per analizzare le seguenti finiture:
- di
- cose
- Terza
- terzi
- questo
- quelli
- anche se?
- tre fasi
- Attraverso
- così
- tempo
- a
- insieme
- verso
- commercio
- Traduzione
- trattamento
- Trend
- prova
- prova
- TURNO
- duplice
- noi
- non chiaro
- per
- Università
- Università
- a differenza di
- fino a quando
- su
- us
- noi governo
- Impiego
- uso
- utilizzando
- utilizzo
- vario
- versione
- molto
- Prima
- we
- pesatura
- Che
- Che cosa è l'
- quando
- se
- quale
- while
- OMS
- volere
- con
- senza
- valore
- sarebbe
- anni
- ancora
- zefiro





![Workshop su "L'opposizione ai brevetti nel settore farmaceutico" [Kochi, 24-28 aprile]](https://platoaistream.net/wp-content/uploads/2023/03/workshop-on-patent-opposition-in-the-pharmaceutical-field-kochi-april-24-28.png)
![[Sponsorizzato] PatSeer Connect 2023: il ruolo dell'intelligenza artificiale nel plasmare il futuro della proprietà intellettuale](https://platoaistream.net/wp-content/uploads/2023/09/sponsored-patseer-connect-2023-ais-role-in-shaping-the-future-of-intellectual-property-360x210.png)


