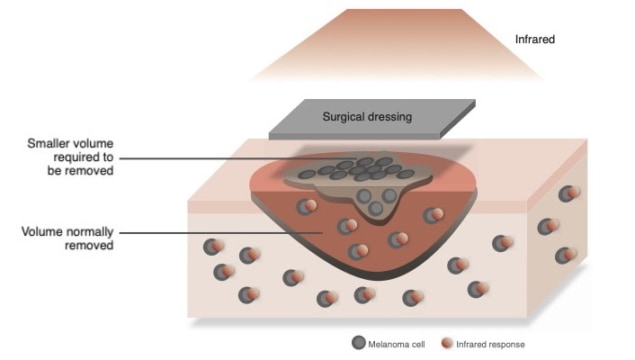
חבישה כירורגית יעילה ביותר המיועדת לחולי סרטן העור יכולה להאיץ את תהליך הריפוי לאחר הניתוח. החבישה, שפותחה על ידי חוקרים בבריטניה ובסין, מנצלת גם השפעות פוטותרמיות כדי למנוע מגידולים להופיע מחדש.
טיפול פוטותרמי (PTT) התגלה כטכניקה מבטיחה לטיפול בסרטן העור. זה כרוך בהזרקת גידולים עם ננו-חומרים מוליכים הממירים אור לחום, ולאחר מכן להאיר אותם באורכי גל ספציפיים כדי להרוג תאים סרטניים. עבור גידולים גדולים, טיפול זה חייב להתבצע בשילוב עם ניתוח, ומותירים פצעים שיש לטפל בהם בחבישות ניתוחיות למניעת זיהום.
לאחרונה הוצעו שיטות טיפול מתקדמות יותר בהן PTT משולבת ישירות בחבישות הניתוחיות. התקווה היא שחומרים אלו יוכלו לקדם ריפוי בעור, תוך מניעת התעוררות מחודשת של גידולים לאחר הטיפול. העיצובים התיאורטיים של חבישות אלו מבוססות על החומר הפוטותרמי המופחת תחמוצת גרפן (rGO). ניתן לסנתז חומר זה על ידי הצמדת קבוצות המכילות חמצן ליריעות גרפן חד-שכבות, ולאחר מכן הכפפתן לתהליך שמפחית את תכולת החמצן שלהן.
נכון לעכשיו, טכניקה זו עומדת בפני מחסום דרכים גדול: rGO רעיל לתאים חיים, כלומר לא ניתן להשתמש בו ישירות בחבישות כירורגיות. לפני תהליך ההפחתה, ניתן להפוך את תחמוצת הגרפן לתואמת יותר ביולוגית על ידי שילובו עם ביומולקולות כמו פפטידים וחלבונים. עם זאת, על מנת לשפר את התגובה הפוטותרמית שלו, החומר חייב לאחר מכן לסבול תהליך הפחתה קשה: מבוצע בכור אטום בטמפרטורות העולות על 180 מעלות צלזיוס, בסביבה של אתנול טהור. תוך הפחתת תחמוצת הגרפן של החומר, הדבר גם הורס את המבנים הביו-מולקולריים העדינים יותר המחוברים אליו.
הצוות, בראשות יואנהאו וו באוניברסיטת נוטינגהם, פיתחה כעת טכניקה חדשה המאפשרת לתהליך ההפחתה להתרחש בטמפרטורות נמוכות יותר. זה כולל מכלול של פתיתי גרפן אוקסיד, עטופים בביופולימר חלבוני בשם "רקומבינאמר דמוי אלסטין" (ELR), הידוע ביכולתו לקדם תיקון עור ולרפא פצעים. על ידי שליטה באינטראקציות המולקולריות בין המבנים הללו, הצוות ייצר ליבת תחמוצת גרפן רב-שכבתית, מוקפת במעטפת ELR.
לאחר מכן, החוקרים חשפו את המבנה הזה לחומר חיטוי המכיל 70% אתנול. בדרך כלל, הנוזל הזה חודר ישר דרך חיידקים וקליפות החלבון של וירוסים. במקרה זה, הוא עבר ישר דרך מעטפת ה-ELR כדי ליצור אינטראקציה עם תחמוצת הגרפן הטהורה שבתוכה. זה אפשר לצוות להפעיל את תהליך ההפחתה בטמפרטורות נמוכות בהרבה של 85 מעלות צלזיוס, תוך השארת מבנה ה-ELR שלם.
בסך הכל, המבנה הסופי שילב את יעילות ה-PTT הגבוהה של rGO עם היכולת לקדם התחדשות רקמות. כבונוס נוסף, החומר עבר עיקור באמצעות טיפול באתנול.

טיפול פוטותרמי בעל שלושה שיניים מבטל גידולים בעכברים
החוקרים אימתו את הגישה שלהם באמצעות in vivo ניסויים בעכברים, הוכיחו שהחבישות יכולות למנוע הישנות הגידול ולקדם ריפוי פצעים לאחר כריתת הגידול. החומר היה זקוק רק לחשיפה של 15 שניות לאור קרוב לאינפרא אדום כל 48 שעות כדי להיות יעיל.
הצוות של וו מקווה שהחבישות הייחודיות יוכלו להוביל לטיפולים מעשיים לאחר ניתוח שחולים עם סרטן העור יוכלו לספק בביתם: הן לזרז את הריפוי של פצעי הניתוח שלהם, והן מניעת גידולים להופיע מחדש עם התחדשות העור שלהם.
המחקר מתואר ב חומרים פונקציונליים מתקדמים.