을 참조 추가 정보 자세한 사항.
GO합성
s-GO와 us-GO의 수성 분산액은 이전 연구에서 설명한대로 준비되었습니다.6,45 초음파 처리와 결합된 수정된 Hummers의 방법으로. 우리는 내독소가 없는 조건에서 처리된 발열원 제거된 유리 제품을 사용했습니다. 흑연 분말을 질산나트륨 및 황산과 저온에서 격렬히 교반하여 혼합한 후, 과망간산칼륨을 첨가하고 주사용수를 적가하였다. 혼합물을 30℃에서 98분 동안 교반한 후 과산화수소로 반응을 중단시켰다. pH를 중화하고, 불순물을 제거하고, 흑연 잔류물로부터 GO를 분리하기 위해 주사용수를 사용했습니다. GO는 볼텍싱으로 각질을 제거하고 주황색 젤 층에서 주사를 위해 따뜻한 물로 용해시켰습니다. 분산액에 여전히 존재하는 흑연 잔류물은 반응 24시간 후 추가 원심분리 단계를 통해 제거되었습니다. 소형 및 초소형 플레이크로의 크기 감소는 각각 5분 및 4시간 동안 초음파 처리를 통해 수행되었습니다.
GO 나노시트의 특성화
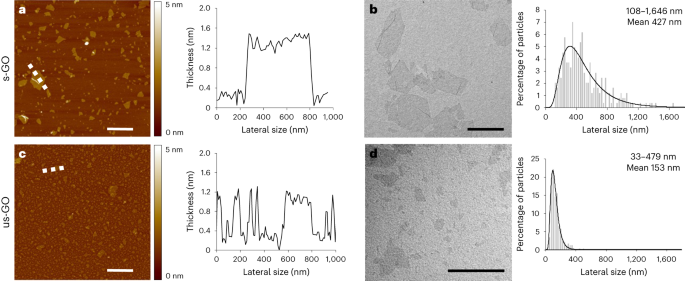
GO는 원자간력 현미경, 투과전자현미경, 유체역학적 직경 및 표면 전하(제타 전위) 측정, UV-가시광선 분광학, 형광 분광학, 라만 분광학, 푸리에 변환 적외선 분광학, 열중량 분석 및 X선 광전자 분광학으로 종합적으로 특성화되었습니다(참조: 그만큼 추가 정보 자세한 내용은).
나노입자 노출 및 특성화
나노입자 노출은 에든버러 왕립의료원(Royal Infirmary of Edinburgh) 외부에 위치한 이동 노출 실험실에서 수행되었습니다(보충 그림 2). 2), 숙련된 노출 기술자의 감독하에. GO의 스톡 현탁액(2 mg ml- 1 s-GO의 경우; 1.3mg ml- 1 for us-GO)는 박테리아 오염이 없는 멸균 증류수로 만들어졌으며 이전에 발표된 방법을 사용하여 확인되었습니다.10. s-GO를 1.3mg/ml로 희석했습니다.- 1 무균 조건의 멸균 식염수에 넣어 분취하고 사용할 때까지 4°C에서 보관합니다.
GO를 5ml 주사기로 옮기고 주사기 펌프에 놓고 Schlick 압축 공기 분무기(모델 970/S Untersiemau, Dusen-Schlick)를 사용하여 HPLC 등급 물로 인라인 희석하여 에어로졸화했습니다. Schlick 분무기의 압축된 예열(60°C) 공기 흐름은 12lm이었습니다.- 1. 에어로졸을 가열된 혼합 유리관에서 건조시킨 후 HEPA로 필터링된 실내 공기로 원하는 농도로 희석하고 초음파 분무기(Omron Ultrasonic Nebulizer NE-U50)를 사용하여 상대습도 60~12%로 가습했습니다. 에어로졸을 200ℓ 혼합 챔버에 공급하고 일정한 온도 및 상대 습도(50%) 하에서 입과 코 위에 노출 마스크를 씌워 지원자에게 전달했습니다. GO는 100~300 μgm- 사이의 노출 농도로 전달되었습니다.- 3, 목표 평균 농도는 200 μg m- 3. 이 복용량 범위는 부작용 없이 다양한 심혈관 매개 변수의 손상과 관련된 희석 디젤 배기가스에 대한 이전의 제어된 노출 연구를 기반으로 선택되었습니다.19,30 심혈관 매개변수를 변경하지 않는 탄소 및 금 나노입자를 사용합니다.29,46. 농도는 노출 기술자가 모니터링하고 유지하는 테이퍼형 요소 진동 마이크로저울(모델 1400A, Thermo Scientific) 판독값을 기반으로 현탁액을 전달하는 주사기 펌프의 속도를 변경하여 조정할 수 있습니다.
에어로졸의 입자 농도는 스테인레스 스틸 튜브를 사용하여 200 l 혼합 챔버 중앙에서 측정되었습니다. 측정된 입자 특성은 다음과 같습니다: 입자 질량(테이퍼 요소 진동 마이크로저울 및 중량 필터 기반 분석), 입자 수(응축 입자 계수기, 모델 3022 A CPC, TSI Inc.) 및 입자 크기 분포(PALAS 차동 전기 이동성 분류기) (U-DEMC 모델 2200) 및 광학 입자 크기 측정기(모델 3330, TSI Inc.)). 입자 질량은 또한 자원 노출 마스크에 가까운 금속 튜브에서 채취한 미리 무게를 잰 텔폰 필터의 누적 질량을 계산하여 노출 후 결정되었습니다.
윤리 강령
이 연구는 경험이 풍부한 임상의와 간호 지원에 의해 진행되는 절차와 부작용이 발생할 경우 필요한 응급 시설을 갖춘 주요 병원에서 수행되는 엄격한 윤리적 검토를 통해 설계되었습니다. 이 연구는 헬싱키 선언, 에든버러 대학교, NHS 학술 및 임상 중앙 연구 개발 사무국(ACCORD), 연구 윤리 위원회(18-HV-084)의 호의적인 윤리적 의견에 따라 서면 동의를 받아 수행되었습니다. 모든 참가자로부터. 해당 연구는 참조 번호로 Clinicaltrials.gov에 등록되었습니다. NCT03659864.
참가자 및 자격 기준
지역 윤리 검토의 승인을 받아 병원과 대학 캠퍼스에서 포스터와 이메일을 통해 연구 광고를 통해 14명의 건강한 지원자를 모집했습니다. 한 명의 참가자가 연구 기간 내에 노출 방문을 완료할 수 없었기 때문에 15명의 참가자의 데이터가 포함되었습니다. 비교를 위한 2D 재료에 대한 다른 제어된 노출 연구의 부족으로 인해 디젤 배기 노출로 인한 혈액 내 혈관 반응성 및 염증성 사이토카인의 변화를 기반으로 한 대기 오염 물질에 대한 이전의 제어된 노출 연구에 따라 1명의 목표가 선택되었습니다. 희석된 디젤 배기가스에 32시간 노출되면 팔뚝 혈류가 1nmol/min로 ~XNUMX% 감소했습니다.- 1 브래디키닌(디젤 배기가스 대 여과된 공기 제어에 대해 각각 분당 16ml 조직당 ~2 ± 19 대 ~2.5 ± 100ml(±sd))19. 희석된 디젤 배기가스에 2시간 노출되면 혈장 TNF-α가 12.5% 증가했습니다(0.99 ±, 0.07 대 0.88 ± 0.007 pg ml )- 1 (±sd) 디젤 배기가스 대 여과된 공기의 경우 각각25. 이 수치를 바탕으로 이러한 변화를 감지하려면 각각 12명과 10명의 자원 봉사자가 필요합니다. P 0.05% 검정력에서 < 80. 다른 연구에서는 흡입된 2D 재료의 효과를 테스트하지 않았기 때문에 추가적인 예방 조치로 이 초기 연구에서는 그룹 크기를 15명 이상으로 늘리지 않기로 결정했습니다.
관심 있는 참가자에게는 연구 참여에 동의하기 전 최소 24시간 동안 읽고 고려하도록 요청받은 참가자 정보 시트가 제공되었습니다. 연구 방문의 경우 참가자는 연구 방문 전 최소 24시간 동안 12시간 동안 알코올을 금하고 음식과 카페인 함유 음료를 금했습니다. 참가자는 포함 기준을 충족하는지 확인하기 위해 초기 심사 방문에 초대되었습니다 (보충 표 2). 참가자들은 미립자에 대한 명백한 노출을 배제하기 위해 선별 검사 방문 시 직업에 대해 질문을 받았습니다. 낮은 준수율로 인해 참가자들 사이에 추가적인 변동 요인이 추가되었기 때문에 연구 방문 외에는 참가자들에게 안면 마스크를 착용하도록 요청하지 않았습니다(이 연구는 영국에서 마스크 착용이 일반화되기 전인 코로나바이러스 대유행 이전에 진행되었습니다). 심지어 직업용 안면 마스크도 활동 모드에 따라 흡입된 입자를 제거하는 데 큰 차이가 있는 것으로 나타났습니다.47. 중요한 것은 각 지원자가 자신의 대조군 역할을 하고 무작위 순서로 각 노출을 받아 내재적 생물학 및 생활 방식 요인의 변화를 최소화했다는 것입니다.
연구 설계
그림을 참조하십시오. 2. 심사 방문을 통해 참가자의 자격 기준을 확인한 후 서면 동의를 받고 참가자 코드를 할당했습니다. 신장, 체중, 심박수, 혈압 및 폐 기능을 측정하고 전체 혈액 세포 수를 측정하기 위해 혈액 샘플 3ml를 채취했습니다. 매개 변수가 젊고 건강한 개인의 정상 범위 내에 있는 경우 참가자는 전체 연구 기간으로 이동되었습니다. 또한 참가자들은 분당 25리터의 환기 속도를 생성하는 데 필요한 작업량을 결정하기 위해 자전거 인체공학계로 등급별 심폐 운동 스트레스 테스트를 받았습니다.- 1 m- 2.
GO의 두 가지 측면 차원(다른 모든 물리화학적 특성을 거의 동일하게 유지)이 연구를 위해 선택되었습니다: s-GO 및 us-GO. 두 가지 유형의 나노시트 모두 이전 전임상(설치류) 연구에서 급성 또는 종단적 부작용이 없는 것으로 나타났습니다.6, 안전 예방 조치로 이 작업에서 제외된 '대형' GO 시트와는 대조적입니다. 연구 방문에는 이중 맹검 무작위 교차 연구 설계가 사용되었으며, 이에 따라 노출 순서(여과된 공기, s-GO, us-GO)가 무작위로 지정되었습니다. 모든 연구 방문은 다양한 노출 사이에 휴약 기간을 허용하기 위해 최소 2주 간격으로 구성되었습니다. 연구를 수행하는 자원봉사자와 임상의는 노출 그룹의 신원을 알지 못했습니다. 원시 데이터를 대조하고 분석하는 데 참여한 모든 연구자는 노출 그룹에 대해 눈이 멀었으며, 눈가림 해제는 노출별로 그룹화할 준비가 된 경우에만 발생했습니다.
노출 전(시간 t = 0시간), 심박수, 혈압 및 폐 기능을 측정하고 혈액을 채취했습니다. 참가자들에게 방광을 비우도록 요청한 다음 연구 방문 기간 동안 소변을 수집할 수 있는 소변 용기를 제공했습니다. 참가자들은 연구 기간 동안 에든버러 왕립의료원(Royal Infirmary of Edinburgh)에 위치한 노출 실험실로 이동되었습니다. 숙련된 연구 임상의와 노출 기술자가 노출 전반에 걸쳐 참여했으며 프로토콜의 나머지 부분에도 동일한 연구원과 간호 지원이 제공되었습니다.
노출 실험실에서 참가자들은 흡입을 통해 나노입자를 전달할 수 있는 안면 마스크를 착용했습니다. 자원봉사자들은 호흡률을 분당 25μl로 높이는 데 필요한 작업량으로 자전거를 타도록 요청받았습니다.- 1 m- 2 (스크리닝 방문 시 운동 테스트를 통해 미리 결정됨) 15시간 노출 동안 2분 동안 교대로 휴식을 취합니다. 노출 후, 대상은 생물학적 변수 평가를 위해 임상 연구 시설로 돌아왔습니다.
활력 징후, 폐 기능 및 노출 전 채혈(t = 0 h)에서 반복되었습니다. t = 2.25, 4, 6시간(즉, 노출 후 15분, 2시간, 4시간). 읽기 쉽도록 2.25시간 시점을 다음과 같이 지칭합니다. t = 전체 2시간). 심부 동맥 손상의 생체외 모델은 노출 후 1~1.5시간에 수행되었으며, 팔뚝 혈량측정은 노출 후 2~4시간에 수행되었습니다(아래 참조). 모든 자원봉사자와 모든 연구 방문에 대해 동일한 가벼운 점심이 제공되었습니다. 추가적인 안전 조치로서 각 그룹의 첫 번째 노출에 대해 단축된 프로토콜(체외 혈전증 분석, 팔뚝 혈량측정 또는 4시간 측정 없음)을 수행했습니다. 전체 프로토콜에 따라 후속 지원자를 위한 연구 방문은 부작용이 없고 혈액 바이오마커에 뚜렷한 변화가 없음이 확인된 후에만 예약되었습니다. 자원봉사자들은 윤리위원회의 승인을 받아 시간과 여행 비용에 대한 보상을 받았습니다.
폐 기능 및 활력 징후
참가자들은 활력 징후와 폐 기능을 측정하기 전에 15분 동안 앉은 자세로 휴식을 취하도록 요청 받았습니다. 폐 기능은 폐활량 측정법(Vitalograph Alpha III)으로 측정되었으며 스크리닝 방문 시 최적의 호흡 기술이 입증되었습니다. FEV1 그런 다음 FVC를 측정하고 밀접하게 일치하는 두 번의 연속 실행의 평균을 사용했습니다. 참가자들은 혈압계로 혈압과 심박수를 측정하기 전에 추가로 5분간 휴식을 취했습니다.
혈관 기능
임상 프로토콜은 정맥 폐쇄 혈량측정법을 통해 혈관 확장제에 반응하는 혈관 기능을 측정하는 것을 포함하도록 설계되었습니다.19 사이에 t = 4시간 및 t = 6시간 그러나 기술적, 인력적 어려움으로 인해 충분한 자원봉사자로부터 의미 있는 결론을 내릴 수 있는 신뢰할 수 있는 데이터를 얻을 수 없었기 때문에 해당 데이터는 생략되었습니다. 해당 기술에 대한 자세한 내용은 다음에서 확인할 수 있습니다. 추가 정보.
혈액 바이오마커
나노입자 노출 전에 혈액을 채취했습니다(t = 0시간) 및 2, 4, 6시간. 17게이지 캐뉼라를 양쪽 팔의 큰 전주정맥에 삽입하고 멸균 식염수로 씻어냈습니다. 먼저 혈액 1ml를 버리고 약 27ml를 채취하여 분석하였다. EDTA 처리 혈액은 혈액 세포 감별 측정에 사용되었고, 구연산염 처리 혈액은 응고 마커(활성화된 부분 트롬보플라스틴 시간, 프로트롬빈 시간, 피브리노겐)에 사용되었으며, 응고된 혈액은 C 반응성 단백질(CRP) 및 혈청 수집에 사용되었습니다. 사이토카인(IL-6, TNF-α). 혈액 측정은 표준 방법론에 따라 에딘버러의 NHS 왕립 의무실의 임상 생화학 부서에서 수행되었습니다. 사이토카인은 효소 결합 면역흡착 분석(ELISA)(R&D Systems)을 사용하여 측정되었으며 검출 한계는 0.022 pg ml 입니다.- 1 TNF-α 및 0.031 pg ml- 1 IL-6의 경우. 바이오뱅킹을 위해 혈액과 소변의 하위 샘플을 -80°C에서 동결했습니다.
생체 외 혈전증
혈액의 응고성은 심부 동맥 손상에 대한 혈전증 모델을 사용하여 생체외에서 측정되었습니다(그림 1). 6). 우리는 지원자들이 디젤 배기가스에 노출된 후의 임상 연구에서 이 기술을 광범위하게 사용했습니다.30,48 그리고 항혈전제 검사49,50. 10 ml min 의 유속으로 설정된 펌프를 통해 전주정맥에서 혈액을 채취했습니다.- 1. 캐뉼라를 비응고 튜브(Masterflex Tygon, Cole Parmer)를 사용하여 수조에서 5°C로 유지되는 37개의 순차적 원통형 관류 챔버에 연결하기 전에 처음 212ml의 혈액을 버렸습니다. 돼지 대동맥 스트립(Pel-freez)은 혈전 형성 기질로 작용하는 내막과 얇은 배지층을 조심스럽게 제거하여 준비하고 혈류의 생리학적 방향에 따라 챔버에 장착했습니다. 첫 번째 챔버의 유변학적 조건은 개방성 관상동맥의 조건을 시뮬레이션했습니다(낮은 전단 속도, ~XNUMX초).- 1), 두 번째 및 세 번째 챔버의 챔버는 약간 협착된 관상 동맥(고전단 속도, ~1,690초)을 시뮬레이션합니다.- 1). 따라서 모델은 심부 관상동맥 손상 중 하나로 작용합니다. 각 챔버 실행은 5분 동안 지속되었으며, 그 후 식염수를 스트립 위에 관류하여 비부착 혈액을 제거했습니다. 혈전이 부착된 돼지 스트립을 제거하고 4% 파라포름알데히드에 고정했습니다. 스트립을 3개의 단면으로 절단하고, 왁스를 포매하고, 조직학적으로 단면화하고, 내인성 과산화수소 활성을 1% 과산화수소 용액으로 차단했습니다. 절편을 실온에서 1.2시간 동안 다클론 토끼 항-인간 피브린(원) 항체(XNUMX μg ml )와 함께 배양했습니다.- 1; 고양이. No. A0080, Dako) 및 단클론 마우스 항 인간 CD61 항체 (1.28 μg ml- 1; 고양이. 번호 M0753, 다코). Bond Polymer 정제 검출 키트(Leica Microsystems GmbH)를 사용하고 3,3'-디아미노벤지딘 기질 발색체(66mM, Dako)로 처리하여 항원 시각화를 수행했습니다. 마지막으로, 섹션을 헤마톡실린으로 대비염색한 다음 다이렉트 레드 80(0.1% 시리우스 레드)으로 대조염색했습니다. 반자동 슬라이드 스캐너(Axioscan Z1, Zeiss) 및 이미지 분석 소프트웨어(QuPath 0.2.3)51 맹검 연구자가 혈전 면적을 정량화하기 위해 사용했습니다. 전체 혈전 면적을 감지하기 위해 색상을 기반으로 한 고해상도 분류기가 확립되었습니다.
혈장 샘플의 고충실도 나노프로테오믹스 분석
리포솜 나노입자 제조 및 혈장 단백질 농축
수소화된 대두 포스파티딜콜린(HSPC): 콜레스테롤(Chol):- 1,2-디스테아로일-sn-글리세로-3-포스포에탄올아민-폴리에틸렌 글리콜2000(DSPE-PEG2000)은 이전에 설명한 대로 얇은 지질막 수화 후 압출을 통해 제조되었습니다.52. 지질을 1:1 부피비의 클로로포름:메탄올에 용해시키고 진공 하에서 증발시켰습니다. 지질막을 황산암모늄으로 수화시켜 대형 다중층 리포솜을 생성했습니다. 소형 단층 리포솜은 미니 압출기(Avanti Polar Lipids)를 사용하여 폴리카보네이트 및 압출 필터(Whatman)를 통한 압출에 의해 생성되었습니다.
리포솜과 인간 혈장을 궤도 진탕기에서 배양하고 단백질 코팅 리포솜을 이전에 설명한 방법에 따라 과잉 혈장 단백질로부터 분리했습니다.53 크기 배제 크로마토그래피와 막 한외여과를 포함하는 5단계 정제 프로토콜을 사용합니다. 결합된 단백질을 3% SDS 트리에틸암모늄 중탄산염을 함유한 S-트랩 용해 완충액과 혼합하여 단백질을 용해시켰습니다. 샘플을 디티오트레이톨로 환원시키고, 요오도아세트아미드 및 디티오트레이톨로 알킬화시켰습니다. 단백질 용해물을 인산 및 S-트랩 결합 완충액과 혼합하여 컬럼에 단백질을 트랩한 다음 트립신으로 분해했습니다. 펩타이드 샘플을 추출한 다음 올리고 R3000 비드를 사용하여 탈염했습니다. Q Exactive Hybrid Quadrupole-Orbitrap 질량 분석기(Thermo Fisher Scientific)에 결합된 UltiMate XNUMX Rapid Separation 지질 크로마토그래피 플랫폼(Dionex Corporation)을 사용하여 액체 크로마토그래피 질량 분석법/질량 분석법으로 샘플을 분석했습니다. 펩타이드 샘플의 데이터 분석은 다음과 같습니다. 추가 정보.
에이코사노이드 및 관련 생리활성 지질 매개체
프로스타글란딘(PGD)을 포함하는 50개 이상의 에이코사노이드 패널을 사용하여 표적화된 지질 분석을 수행했습니다.2, PGE2, PGF2α, 13,14-디하이드로-15-케토-PGD2, 13,14-디하이드로-15-케토-PGE2, 11-베타-PGF2α, 6-케토-PGF1α, 15-데옥시-Δ12,14-PGD2, 15-데옥시-Δ12,14-PGJ2); 트롬복산(TxB2, 11-디하이드로-TxB2); 하이드록시-에이코사테트라엔산(5-HETE, 8-HETE, 9-HETE, 11-HETE, 12-HETE, 15-HETE, 20-HETE); 류코트리엔(LTB4, 20-카르복시-LTB4); 에폭시-에이코사트리엔산(5,6-EET, 8,9-EET, 11,12-EET, 14,15-EET; 5-OxoETE, 15-OxoETE); 디하이드록시-에이코사트리엔산(5,6-DHET, 8,9-DHET, 11,12-DHET, 14,15-DHET), 하이드록시-에이코사펜타엔산(5-HEPE, 15-HEPE), 옥타데카디엔산(9-HODE , 13-HODE, 9-Oxo-ODE, 13-Oxo-ODE), 에폭시옥타데카모노엔산(9,10-EpOME, 12,13-EpOME), 프로분해 매개체(리폭신 A4 – LXA4 및 레졸빈, RvD1, RvD2); 이소프로스탄(8-iso-PGF2α) 및 지방산(아라키돈산, 에이코사펜타엔산(EPA), 도코사헥사엔산(DHA) 및 그 대사산물, 7-HDHA; 14-HDHA; 17-HDHA; 10,17-DiHDHA).
혈장은 EDTA 처리된 혈액으로부터 제조되었습니다. 다음과 같은 내부 표준이 사용되었습니다: PGE2-d4, 15-HETE-d8, LTB4-d4, 14,15-EET-d11, 14,15-dHET-d11, 9,10-EpOME-d4, 9,10-DiHOME-d4, RvD2-d5, EPA-d5 및 8-iso-PGF2α-d4 (케이먼 케미칼). 참조 추가 정보 샘플 처리에 대한 자세한 내용은 Eicosanoids는 Shimadzu Nexera-X18 초고성능 액체 크로마토그래피 시스템을 사용하여 Hypersil GOLD C2 컬럼(Thermo)에서 분리되었습니다. 유출물은 다중 반응 모니터링을 사용하여 음이온 모드에서 작동되는 Sciex QTRAP 6500 질량 분석기의 IonTurbo 소스로 보내졌습니다. 아이코사노이드는 특징적인 전구체/생성 이온 쌍 전이 및 실제 표준과 일치하는 유지 시간을 기반으로 식별되었습니다. Sciex Analyst를 사용하여 데이터를 수집하고 분석했습니다.54 소프트웨어 v1.6. 에이코사노이드의 농도는 각 화합물에 대해 병렬로 실행되는 검량선과 비교하여 결정되었으며 적절한 내부 표준의 양을 참조하여 회수율을 조정했습니다.
일반 데이터 및 통계 분석
데이터는 Excel 2010을 사용하여 분석되었습니다.55, R 3.2.2 (참조. 56) 및 Prism 9.3 (참조. 57). 테이블의 데이터 1 및 확장 데이터 테이블 1-6 달리 명시하지 않는 한 평균 ± SD로 표시됩니다. 연속 데이터는 평균 및 SD로 표시됩니다. 그룹 내 및 그룹 간의 통계적 유의성은 Tukey의 정직 유의차 사후 테스트를 통해 양방향 분산 분석을 사용하여 테스트되었습니다. 위의 통계 패키지를 사용하여 모수적 가정(정규 분포 및 등분산)을 확인했습니다. 데이터가 정규 분포되지 않은 경우 비모수적 대안(예: Kruskal-Wallis 테스트)이 사용되었습니다.
보고 요약
연구 설계에 대한 추가 정보는 Nature 포트폴리오 보고 요약 이 기사에 링크되어 있습니다.
- SEO 기반 콘텐츠 및 PR 배포. 오늘 증폭하십시오.
- PlatoData.Network 수직 생성 Ai. 자신에게 권한을 부여하십시오. 여기에서 액세스하십시오.
- PlatoAiStream. 웹3 인텔리전스. 지식 증폭. 여기에서 액세스하십시오.
- 플라톤ESG. 탄소, 클린테크, 에너지, 환경, 태양광, 폐기물 관리. 여기에서 액세스하십시오.
- PlatoHealth. 생명 공학 및 임상 시험 인텔리전스. 여기에서 액세스하십시오.
- 출처: https://www.nature.com/articles/s41565-023-01572-3
- :있다
- :이다
- :아니
- :어디
- ][피
- 05
- 07
- 1
- 1.3
- 10
- 100
- 11
- 12
- 13
- 14
- 15%
- 19
- 2%
- 200
- 2005
- 2008
- 2010
- 2011
- 2015
- 2016
- 2017
- 2018
- 2019
- 2020
- 2021
- 24
- 25
- 27
- 28
- 29
- 2D
- 30
- 300
- 3000
- 32
- 34
- 4
- 40
- 45
- 46
- 48
- 49
- 5
- 50
- 51
- 52
- 54
- 55
- 6
- 60
- 66
- 75
- 8
- 80
- 9
- 98
- a
- 소개
- 위의
- 학술
- 협정
- 일치
- 에 따르면
- 모으다
- 누적 된
- 획득한
- 가로질러
- 행동
- 활성화
- 활동
- 행위
- 심각한
- 추가
- 또한
- 추가
- 조정
- 불리한
- 광고
- 후
- 반대
- 동의하다
- AIR
- 대기 오염
- AL
- 알코올
- All
- 수
- 수
- 거의
- 알파
- 또한
- 대안
- am
- 금액
- an
- 복수
- 분석하는
- 분석
- 분석자
- 닻
- 및
- 항독소
- 항원
- 어떤
- 분리
- 적당한
- 인가 된
- 대략
- 있군요
- 지역
- 무기
- 약
- 기사
- AS
- 문의
- 질문
- 평가
- 할당
- 관련
- 가정
- At
- 붙여진
- 진정한
- 가능
- 벤티
- 평균
- 기반으로
- 기초
- BE
- 되었다
- 된
- 전에
- 베이징
- 존재
- 이하
- 사이에
- 음료수
- 그 너머
- 제본
- 생물학
- 바이오 마커
- 바이오 마커
- 차단
- 피
- 고혈압
- 청사진
- 증서
- 두
- 묶인
- 호흡
- 버퍼
- by
- 카페인
- 계산하는
- 교정
- CAN
- 탄소
- 심혈관
- 한
- 면밀히
- 운반 된
- CAT
- 원인
- 카이만
- 세포
- 중심적인
- 방
- 변경
- 특성
- 특성
- 특징
- 요금
- 화학
- 선택
- 순환
- 분류기
- 클릭
- 객관적인
- 임상 적으로
- 임상
- 닫기
- 면밀히
- 암호
- 수집
- 모은
- 단
- 열
- 결합 된
- 위원회
- 공통의
- 비교
- 비교
- 보상을받은
- 완전한
- compliance
- 화합물
- 컴퓨팅
- 집중
- 결론
- 조건
- 확인하기
- 확인 됨
- 연결
- 연속적인
- 동의
- 고려
- 상수
- 컨테이너
- 끊임없는
- 반대로
- 제어
- 통제
- 핵심
- 코로나
- 코로나 바이러스
- 코로나 바이러스 전염병
- 법인
- 수
- 계산
- 계수기
- 결합
- 코스
- 기준
- 곡선
- 절단
- 주기
- 사이토 카인
- 데이터
- 데이터 분석
- 일
- 결정
- 선언
- 깊은
- 전달
- 배달
- 시연
- 기술 된
- 디자인
- 설계
- 원하는
- 세부설명
- 검색
- Detection System
- 결정
- 결정된
- 개발
- DID
- 디젤 엔진
- 차이
- 다른
- 어려움
- 디지털
- 희석 된
- 치수
- 곧장
- 감독 된
- 방향
- 버려진
- 발견
- 질병
- 분산
- 분산
- 분포
- 선량
- 약물
- 두
- 지속
- ...동안
- 장애
- E & T
- 마다
- 완화
- 에든버러
- 유효성
- 효과
- 여덟
- 요소
- 적임
- 비상 사태
- 빈
- 엔진
- 농축
- 확인
- 환경
- EPA
- 같은
- 확립 된
- 에테르 (ETH)
- 윤리적인
- 윤리학
- EUR
- 조차
- 이벤트
- 이벤트
- 예
- 뛰어나다
- 초과
- 제외
- 운동
- 경비
- 경험
- 노출 시간
- 표현
- extended
- 널리
- 페이스메이크업
- 안면 마스크
- 얼굴 마스크
- 시설
- 포함내용
- 인자
- 요인
- 연방 준비 은행
- 무화과
- 그림
- 도
- Film
- 영화
- 필터링
- 필터
- 최종적으로
- 먼저,
- 고정
- 흐름
- 플러시
- 다음에
- 수행원
- 식품
- 럭셔리
- 힘
- 형성
- 발견
- Foundation
- 푸리에
- FRAME
- 무료
- 에
- 겨울 왕국
- 가득 찬
- 기능
- 추가
- 생성
- 주어진
- 유리
- GMBH
- Go
- 덴탈
- 등급이 매겨진
- 그래 핀
- 매우
- 그룹
- 여러 떼
- 가이드 라인
- 처리
- 있다
- 건강은 물론, 경제성까지!
- 심장
- 신장
- 헬싱키
- 높은
- 높은 해상도
- 정직한
- 병원
- 그러나
- HTTPS
- 사람의
- 인간
- 잡종
- 수화
- 수소
- 같은
- 확인
- 통합 인증
- if
- III
- 영상
- 이미지 분석
- 손상
- 중요하게
- in
- 주식 회사
- 포함
- 포함
- 포함
- 증가
- 증가
- 배양
- 표시된
- 개인
- 유도하다
- 염증을 일으키는
- 정보
- 정보
- 처음에는
- 주사
- 해
- 내부의
- 으로
- 본래 갖추어 진
- 초대
- 참여
- IT
- 그
- 왕국
- 키트
- 실험실
- 결핍
- 언어
- 넓은
- 층
- 가장 작은
- 라이프 스타일
- 빛
- 제한
- LINK
- 연결
- 리퀴드
- 지방의
- 낮은
- 점심
- 만든
- 유지
- 유지
- 주요한
- 확인
- 사람
- 두드러진
- 마스크
- 마스크
- 질량
- 어울리는
- 자료
- 재료
- 평균
- 의미있는
- 방법
- 측정
- 측정
- 측량
- 측정 시간 상관관계
- 미디어
- 남성 컬렉션
- 만나
- 금속
- 메타놀
- 방법
- 방법론
- 현미경 사용
- Microsoft
- Microsoft Excel에서
- 중간
- 제분업자
- 제 분소
- 분
- 최소화
- 혼합 된
- 혼성
- 혼합물
- ML
- 모바일
- 유동성
- 모드
- 모델
- 모드
- 수정
- 모니터링
- 모니터링
- 단클론
- 마우스
- 입
- 무 케르
- 여러
- 나노
- 나노 기술
- 자연
- 필요한
- 필요
- NHS
- 아니
- 표준
- 일반적으로
- 코
- 번호
- 간호
- 획득
- 분명한
- 직업
- 직업
- 발생
- 발생하는
- of
- Office
- on
- ONE
- 만
- 열 수
- 오픈 소스
- 운영
- 의견
- 광
- 최적의
- or
- 주황색
- 주문
- 최
- 기타
- 그렇지 않으면
- 우리의
- 아웃
- 설명
- 외부
- 위에
- 자신의
- 패키지
- 쌍
- 세계적 유행병
- 패널
- 평행
- 매개 변수
- 일부의
- 참가자
- 참가자
- 입자
- 특허
- 병리학
- 용
- 성능
- 수행
- 실행할 수 있는
- 기간
- 미문
- 위치
- 혈장
- 플랫폼
- 플라톤
- 플라톤 데이터 인텔리전스
- 플라토데이터
- 포인트 적립
- 정반대의
- 오염
- 중합체
- 유가 증권
- 위치
- 위치하는
- 게시하다
- 포스터
- 가능성
- 힘
- 주의
- 준비
- 제시
- 제시
- 압박
- 예방
- 너무 이른
- 이전에
- 절차
- 처리
- 생산
- 생산
- 생산
- 보호
- 단백질
- 단백질
- 프로토콜
- 제공
- 출판
- 펌프
- R
- R&D
- R3
- 토끼
- 닥치는대로의
- 무작위
- 범위
- 빠른
- 율
- 비율
- 살갗이 벗어 진
- 원시 데이터
- 반응
- 읽기
- 읽기
- 준비
- 접수
- 리시버
- 회복
- 빨간색
- 감소
- 축소
- 참고
- 참조
- 수정하다
- 등록된
- 관련
- 상대적인
- 신뢰할 수있는
- 제거
- 제거
- 제거됨
- 제거
- 반복
- 통계 보고서
- 필수
- 연구
- 연구 및 개발
- 연구원
- 연구원
- 주민
- 호흡의
- 응답
- 응답
- REST
- 보유
- 리뷰
- 엄밀한
- 방
- 왕의
- 통치
- 달리기
- 실행
- s
- 안전
- 같은
- 견본
- 예약
- SCI
- 과학적인
- 전형
- 둘째
- 섹션
- 섹션
- 참조
- 선택된
- 별도의
- 세럼
- 세트
- 시트
- 시트
- 단축
- 영상을
- 표시
- 의미
- 상당한
- 안전표시
- 시뮬레이션하다
- 대지
- 사이트
- 좌석
- 크기
- 크기
- 슬라이드
- 작은
- 나트륨
- 소프트웨어
- 해결책
- 출처
- 지우면 좋을거같음 . SM
- 분광학
- 속도
- 직원
- 스테인리스 강
- 표준
- 기준
- 통계적인
- 스틸
- 단계
- 아직도
- 활발한
- 재고
- 정지
- 저장
- 스트레스
- 조각
- 연구
- 교육과정
- 제목
- 후속의
- 기판
- 충분한
- 감독
- SUPPORT
- 표면
- 현탁
- 정학
- 합성
- 체계
- 시스템은
- 테이블
- 촬영
- 복용
- 목표
- 팀
- 테크니컬
- 기술자
- 기술
- 기법
- test
- 테스트
- 지원
- 그
- XNUMXD덴탈의
- 영국
- 그들의
- 그때
- 그곳에.
- Bowman의
- 그들
- 얇은
- 제삼
- 이
- 그
- 세
- 을 통하여
- 도처에
- 그러므로
- 시간
- 조직
- 에
- 오늘
- 했다
- 금액
- 전송
- 변환
- 전환
- 전달
- 트랩
- 여행
- 치료
- 두
- 유형
- 궁극의
- 울트라
- 초음파
- 할 수 없는
- 아래에
- 단위
- 미국
- 영국
- 대학
- ...을 제외하면
- 까지
- 사용
- 익숙한
- 사용
- v1
- 진공
- 다르다
- 대
- 를 통해
- 방문
- 방문
- 심상
- 필수
- 생체
- 음량
- 자원 봉사
- 자원 봉사자
- W
- 따뜻한
- 였다
- 물
- we
- 착용
- 주
- 무게
- 잘
- 했다
- 언제
- 이므로
- 어느
- 윌슨
- 과
- 빼는
- 이내
- 없이
- 작업
- 겠지
- 쓴
- 엑스선
- 젊은
- 제퍼 넷
- 제타