Dies ist Teil eins einer Fallstudie darüber, wie eine Untersuchung einer Verpackungsbeschwerde durchgeführt werden kann, wenn ein Kunde eine Verpackung offen vorfindet.
Überblick über die Untersuchung von Verpackungsbeschwerden
Bei diesem Fallbeispiel handelt es sich um einen flexiblen, abziehbaren Beutel aus Tyvek und einer durchsichtigen Kunststofffolie. Dies ist eine der am häufigsten verwendeten Verpackungsarten für sterile Medizinprodukte. Parallel zur Untersuchung der Beschwerde werden umgehend Eindämmungsmaßnahmen und Korrekturen umgesetzt, um zu verhindern, dass die Beschwerde zu einem größeren Problem wird. Der Untersuchungsprozess verwendet ein „Fischgrätendiagramm“, um die Grundursache der Verpackungsstörung zu identifizieren. Dies ist nur eines von mehreren Tools zur Ursachenanalyse, die Sie für Reklamationsuntersuchungen verwenden können. Es eignet sich jedoch besonders gut für Beispiele, bei denen bei der Kontrolle des Produktionsprozesses ein Fehler aufgetreten ist, wir uns jedoch nicht sicher sind, welche Prozesskontrolle fehlgeschlagen ist.
Beschreibung der Verpackungsstörung
Der erste Schritt des Beschwerdebearbeitungsprozesses (siehe SYS-018, Kundenfeedback und Beschwerdebearbeitung) besteht darin, eine Beschreibung des angeblichen Qualitätsproblems aufzuzeichnen. Ein Händler meldete den gemeldeten Vorfall. Der Händler teilte dem Kundendienst mit, dass bei zwei Beuteln in einem Karton mit 24 sterilen Geräten eine Versiegelung festgestellt wurde, die offenbar abblätterte. Leider war der Händler nicht in der Lage, ein Muster der delaminierten Beutel oder die Chargennummer der Einheiten bereitzustellen. Verpackungsprobleme und Etikettierungsprobleme sind typischerweise zwei der häufigsten Beschwerdekategorien für Medizinprodukte. Häufig sind die Etikettierungsprobleme auf Bedienerfehler oder eine Verwechslung der Etikettierung zurückzuführen, während die Verpackungsfehler darauf zurückzuführen sein können, dass Kunden versehentlich die falsche Produktgröße bestellt oder geöffnet haben. Daher kann es sein, dass sie sich über die Verpackung beschweren, wenn nichts falsch ist. Es ist wichtig, bei der Untersuchung jeder Verpackungsreklamation sorgfältig vorzugehen, denn wenn es ein berechtigtes Problem mit der Verpackungsqualität gibt, kann im Rahmen Ihres Korrekturmaßnahmenplans ein Produktrückruf erforderlich sein.
Einleitung der Untersuchung einer Verpackungsreklamation
In Ihrem Beschwerdeprotokoll müssen Sie eine Person mit der Untersuchung der Beschwerde beauftragen. Der einzig akzeptable Grund dafür, keine Untersuchung einzuleiten, besteht darin, dass ein ähnlicher Vorfall bereits für ein anderes Gerät derselben Charge oder einer verwandten Charge untersucht wurde (d. h. die Verpackungsrohmaterialcharge ist dieselbe und das Problem hängt mit dem Material zusammen). Wenn die Beschwerde bereits untersucht wurde, sollte der Beschwerdedatensatz einen Querverweis auf den vorherigen Beschwerdedatensatz enthalten.
Die mit der Untersuchung der Beschwerde beauftragte Person muss in der Untersuchung von Beschwerden geschult sein und über technische Qualifikationen für die Untersuchung der mit der Beschwerde verbundenen Prozesse verfügen (z. B. Validierung des Verpackungsprozesses). Der Ermittler muss aufzeichnen, welche Aufzeichnungen im Rahmen der Untersuchung überprüft wurden, und die Untersuchung sollte umgehend abgeschlossen werden, falls eine behördliche Berichterstattung erforderlich ist oder Abhilfemaßnahmen erforderlich sind. Es muss auch nachgewiesen werden, dass Beschwerden konsistent und zeitnah bearbeitet werden (z. B. kann die durchschnittliche Dauer bis zum Abschluss einer Beschwerde ein Qualitätsziel sein).
Regulatorische Meldung von Verpackungsfehlern
Wir wissen, dass jeder die behördliche Berichterstattung vermeiden möchte, weil wir befürchten, dass andere Kunden das Vertrauen in unser Produkt verlieren und schlechte Werbung den Umsatz beeinträchtigen könnte. Allerdings sind die Konsequenzen, wenn man es versäumt, Berichte über Medizinprodukte bei der FDA einzureichen, viel schlimmer. Auch wenn es bei einem sterilen Medizinprodukt nicht zu Verletzungen oder Todesfällen kam, sollte das Qualitätsproblem dennoch als MDR gemäß 21 CFR 803 gemeldet werden (siehe SYS-029, Meldung von Medizinprodukten), da ein wiederholter Vorfall eine Infektion verursachen könnte, die zu Sepsis und Tod führen könnte. Wenn Sie der Meinung sind, dass dies ein äußerst konservativer Ansatz ist, werden Sie überrascht sein zu erfahren, dass der FDA im vierten Quartal 251 4 MDRs wegen Verpackungsproblemen gemeldet wurden. Von diesen Berichten handelte es sich nur bei einem um eine tatsächliche Verletzung, und bei den anderen 2023 handelte es sich um eine Fehlfunktion des Geräts, jedoch nicht um Todesfälle oder Verletzungen. Die folgende Ereignisbeschreibung und der Bericht des Herstellers sind ein Beispiel:
Event-Beschreibung
„Der Vertriebsmitarbeiter in Japan berichtete, dass während eines nicht näher bezeichneten chirurgischen Eingriffs am (b)(6) 2023 die sterile Verpackung des verstellbaren Standardgeräts rgdloop nicht versiegelt und verunreinigt war. Ein anderes ähnliches Gerät wurde verwendet, um den Eingriff abzuschließen. Das gab es.“ Es wurde eine unbekannte Verzögerung des Eingriffs gemeldet. Es wurden keine nachteiligen Folgen für den Patienten gemeldet. Es wurden keine zusätzlichen Informationen bereitgestellt.“
Erzählung des Herstellers
„Dieser Bericht wird gemäß den Bestimmungen von 21 cfr, Teil 803 eingereicht. Dieser Bericht basiert möglicherweise auf Informationen, die vor dem erforderlichen Berichtsdatum nicht untersucht oder überprüft werden konnten. Dieser Bericht spiegelt keine Schlussfolgerung von Mitek wider oder seine Mitarbeiter, dass der Bericht ein Eingeständnis darstellt, dass das Gerät, mitek oder seine Mitarbeiter das in diesem Bericht beschriebene potenzielle Ereignis verursacht oder dazu beigetragen haben. Wenn Informationen erhalten werden, die bei der ersten medizinischen Überwachung nicht verfügbar waren, wird eine Nachuntersuchung durchgeführt entsprechend eingereicht. Das Gerät wurde für die Behandlung und nicht für die Diagnose verwendet. Wenn Informationen erhalten werden, die für die erste medizinische Überwachung nicht verfügbar waren, wird gegebenenfalls eine nachfolgende medizinische Überwachung eingereicht. Zusätzliche H10-Erzählung: e3: Der Reporter ist ein J&J-Vertriebsmitarbeiter. H4: Das Herstellungsdatum des Geräts ist unbekannt.Udi: (b)(4).“
Untersuchung von Verpackungsbeschwerden bei Produkt IST NICHT Rückkehrerd
Worauf die obige Erzählung nicht näher eingeht, sind die konkreten Untersuchungsdetails für die „Überprüfung der Chargenhistorie“. Eines der nützlichsten Tools für die Untersuchung einer Verpackungsbeschwerde ist das „Fishbone-Diagramm“. Andere Namen sind „Ishikawa-Diagramm“ und „Ursache-Wirkungs-Diagramm“. Das Diagramm besteht aus sechs Teilen (d. h. „6Ms“):
- Materialien,
- Verfahren
- Maschine,
- „Mutter Natur“ oder Umwelt,
- „Manpower“ oder Menschen, und
- Messung.
Welche Unterlagen können ohne Rücksendung des Produkts untersucht werden?
Auch wenn der Kunde die Verpackung mit der angeblichen Fehlfunktion nicht zurücksendet, könnten die folgenden Aufzeichnungen auf mögliche Ursachen überprüft und bewertet werden:
- Überprüfen Sie das Reklamationsprotokoll auf andere Reklamationen mit derselben Chargennummer und/oder aus einem ähnlichen Zeitraum, einer ähnlichen Charge von Rohstoffen oder einer ähnlichen Verpackungsmaschine
- Überprüfen Sie den Geräteverlaufsdatensatz für die Charge, um sicherzustellen, dass die Anzahl der im Rahmen der normalen In-Prozess- und Endkontrolle zurückgewiesenen Einheiten die vorab festgelegten Schwellenwerte zur Überwachung des Versiegelungsprozesses nicht überschreitet
- Wenn Restbestände der Charge verfügbar sind, können diese erneut getestet werden, um sicherzustellen, dass die Testergebnisse nach der Echtzeitalterung weiterhin akzeptabel sind
- Die Wartungs- und Kalibrierungsaufzeichnungen der Geräte zur Herstellung und Prüfung können überprüft werden, um sicherzustellen, dass keine Reparaturen erforderlich waren und keine Geräte als nicht kalibriert identifiziert wurden
Wenn alle oben genannten Punkte keine mögliche Ursache für einen Verpackungsfehler identifizieren, liegt möglicherweise ein Problem im Zusammenhang mit Menschen oder der Umwelt vor. Zu den Personen zählen die Personen, die die Produktverpackung verschließen, und die Benutzer. Die Umgebung umfasst die Temperatur und Luftfeuchtigkeit für die Lagerung von Verpackungsrohstoffen, verpackten Produkten, Sterilisationsbedingungen, Lagerbedingungen nach der Sterilisation und Versandbedingungen – einschließlich aller vorübergehenden Extreme, die während des Transports auftreten können.
In unserer Fallstudie wurde das Produkt nicht zurückgegeben und wir hatten keine Chargennummern. Daher müssen wir möglicherweise die Vertriebsunterlagen an diesen Händler und/oder den Kunden überprüfen, um die möglichen Chargen auf eine oder mehrere Chargen einzugrenzen. Dann müssten wir für jedes potenzielle Los die gleiche Art der Überprüfung der Chargenverlaufsaufzeichnungen durchführen. Der beste Ansatz besteht darin, ein Foto der Verpackungsetikette einschließlich des UDI-Strichcodes anzufordern, da diese Informationen die Identifizierung der Charge erleichtern. Selbst wenn das Produkt entsorgt wurde, wird die UDI häufig während der Operation in die elektronische Krankenakte (EMR) des Patienten eingescannt.
Durchführung von Produktuntersuchungen IS ist zurückgekommen
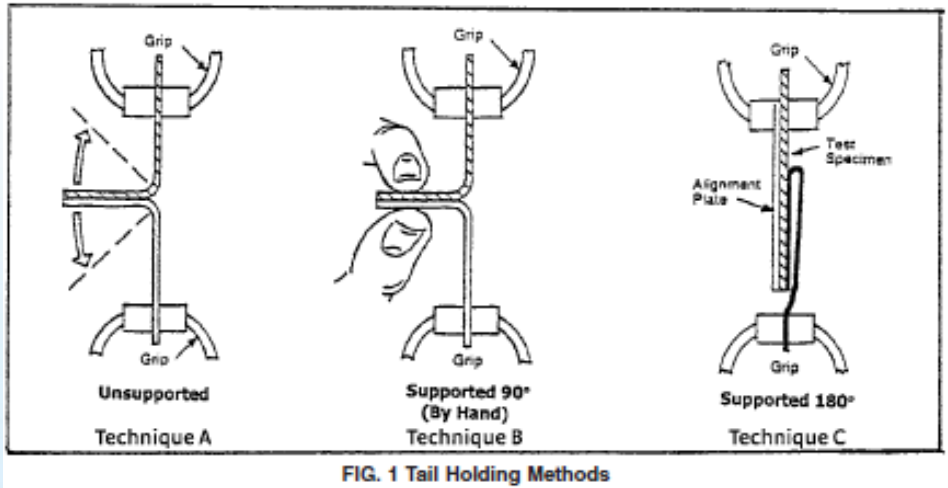
Manchmal haben Sie das Glück, zurückgegebene Produkte zu erhalten. Das Produkt sollte sofort von Ihren anderen Produkten getrennt werden, um Verwechslungen und/oder Kontaminationen zu vermeiden. Normalerweise werden die zurückgegebenen Produkte als gekennzeichnet nicht konforme Produkte und unter Quarantäne gestellt. Nachdem die Sicherheit des unter Quarantäne gestellten Produkts bewertet wurde, kann der beauftragte Prüfer die Verpackung in einem abgetrennten Bereich inspizieren. Verpackungsuntersuchungen beginnen mit der anschließenden Sichtprüfung ASTM F1886. Wenn mehrere Verpackungsmuster verfügbar sind oder die Verpackung groß genug ist, kann der Prüfer eine destruktive Prüfung durchführen (d. h. ASTM F88) einen 1-Zoll-Streifen aus dem Verpackungssiegel ausschneiden, um zu überprüfen, ob die zurückgegebene Verpackung den Originalspezifikationen entspricht. Wenn Sie Verpackungsreste mit der gleichen Charge flexibler Verpackungen aufbewahrt haben, können Sie auch die Aufbewahrungsbehälter einer Sichtprüfung und einer zerstörenden Prüfung unterziehen.
Nächste Schritte der Untersuchung der Verpackungsreklamation
Sobald die Grundursache für eine Verpackungsreklamation identifiziert ist, müssen Sie Korrekturmaßnahmen ergreifen, um ein erneutes Auftreten zu verhindern. Außerdem verlangen FDA Klausel 21 CFR 820.100 und ISO 13485, Klausel 8.5.3, dass Sie vorbeugende Maßnahmen ergreifen, um Situationen zu erkennen, die in Zukunft zu einem potenziellen Verpackungsfehler führen könnten, und vorbeugende Maßnahmen ergreifen, damit ähnliche Verpackungsfehler nicht auftreten können . Wenn Sie mehr über die Durchführung einer Ursachenanalyse erfahren möchten, lesen Sie bitte unseren Blog zu diesem Thema: Effektive Ursachenanalyse – Lernen Sie 4 Tools.
Dieser Artikel ist die erste Hälfte der Fallstudie zur Untersuchung von Verpackungsbeschwerden. Der zweite Hälfte In der zweiteiligen Fallstudie werden die notwendigen Eindämmungsmaßnahmen, Korrekturen, Korrekturmaßnahmen und vorbeugenden Maßnahmen erläutert, um die Grundursache des Verpackungsfehlers zu beheben.
Zusätzliche Ressourcen zur Verpackungsvalidierung
Es gibt viele Artikel zum Thema Verpackungsprüfung und Verpackungsdesign für sterile Medizinprodukte. Wenn Sie mehr erfahren möchten, registrieren Sie sich bitte für unseren Kostenloses Webinar zur Verpackungsvalidierung von Jan Gates.
- SEO-gestützte Content- und PR-Distribution. Holen Sie sich noch heute Verstärkung.
- PlatoData.Network Vertikale generative KI. Motiviere dich selbst. Hier zugreifen.
- PlatoAiStream. Web3-Intelligenz. Wissen verstärkt. Hier zugreifen.
- PlatoESG. Kohlenstoff, CleanTech, Energie, Umwelt, Solar, Abfallwirtschaft. Hier zugreifen.
- PlatoHealth. Informationen zu Biotechnologie und klinischen Studien. Hier zugreifen.
- Quelle: https://medicaldeviceacademy.com/packaging-complaint-investigation/
- :hast
- :Ist
- :nicht
- :Wo
- 08
- 1
- 100
- 11
- 2015
- 2023
- 24
- 250
- 58
- 8
- 820
- a
- Fähig
- LiveBuzz
- oben
- akzeptabel
- Action
- Aktionen
- präsentieren
- Zusätzliche
- Zusätzliche Angaben
- Adresse
- einstellbar
- Neben
- Angst
- Nach der
- Hautalterung
- Alle
- angeblich
- bereits
- ebenfalls
- am
- an
- Analyse
- und
- Ein anderer
- jedem
- erschienen
- Ansatz
- angemessen
- SIND
- Bereich
- Artikel
- Artikel
- AS
- zugewiesen
- At
- verfügbar
- durchschnittlich
- vermeiden
- b
- Badewanne
- Bar
- basierend
- BE
- weil
- Werden
- war
- beginnen
- Sein
- BESTE
- Blog
- Box
- aber
- by
- CAN
- Häuser
- Fallstudie
- Kategorien
- Verursachen
- verursacht
- Ursachen
- klar
- Schließung
- Code
- gemeinsam
- Beschwerde
- Beschwerden
- abschließen
- Abgeschlossene Verkäufe
- Abschluss
- Bedingungen
- Leitung
- Vertrauen
- Folgen
- konservativ
- konsistent
- besteht
- Eindämmung
- Inhalt
- beigetragen
- Smartgeräte App
- Steuerung
- Korrekturen
- könnte
- Kunde
- Kundenservice
- Kunden
- Schneiden
- Datum
- Tage
- Tod
- verzögern
- zeigen
- beschrieben
- Beschreibung
- Design
- Details
- entdecken
- Gerät
- Geräte
- Diagnose
- DID
- Verteilung
- Zwischenhändler
- die
- nach unten
- zwei
- im
- e
- e3
- jeder
- bewirken
- Erarbeiten
- elektronisch
- eingebettet
- Mitarbeiter
- genug
- Arbeitsumfeld
- Ausrüstung
- Fehler
- essential
- Bewerten
- Sogar
- Event
- jedermann
- Beispiel
- Beispiele
- überschreiten
- Erklärt
- äußerst
- Extreme
- erleichtern
- FAIL
- Gescheitert
- andernfalls
- Scheitern
- Ausfälle
- FDA
- Feedback
- Reichen Sie das
- eingereicht
- Filme
- Finale
- Vorname
- flexibel
- Folgende
- Aussichten für
- glücklich
- gefunden
- für
- Zukunft
- Gates
- weg
- Hälfte
- Handling
- Haben
- GUTE
- Geschichte
- Ultraschall
- Hilfe
- aber
- HTML
- http
- HTTPS
- i
- Login
- identifiziert
- identifizieren
- if
- sofort
- Impact der HXNUMXO Observatorien
- implementieren
- umgesetzt
- in
- Zwischenfall
- das
- Einschließlich
- Infektion
- Information
- Anfangs-
- Einleiten
- Verletzung
- interessiert
- in
- untersuchen
- Untersuchung
- Untersuchungen
- beteiligt
- beinhaltet
- ISO
- Problem
- Probleme
- IT
- SEINE
- Januar
- Japan
- nur
- nur einer
- gehalten
- Wissen
- Beschriftung
- grosse
- LERNEN
- lernen
- legitim
- Gefällt mir
- Log
- verlieren
- Los
- viel
- gemacht
- Wartung
- um
- Weise
- viele
- Ihres Materials
- Materialien
- max-width
- Kann..
- MDR
- Maßnahmen
- sowie medizinische
- medizinisches Gerät
- Medizinprodukte
- Trifft
- könnte
- Mitek
- Überwachung
- mehr
- vor allem warme
- viel
- mehrere
- sollen
- Namen
- NARRATIVE
- schmal
- notwendig,
- Need
- erforderlich
- nicht
- normal
- Normalerweise
- nichts
- Anzahl
- Zahlen
- Ziel
- erhalten
- auftreten
- of
- vorgenommen,
- on
- EINEM
- einzige
- XNUMXh geöffnet
- geöffnet
- Operator
- or
- Original
- Andere
- UNSERE
- Paket
- verpackt
- Verpackung
- Parallel
- Teil
- besonders
- Teile
- Vertrauen bei Patienten
- Personen
- ausführen
- Durchführung
- Zeit
- person
- für Ihre privaten Foto
- Plan
- Kunststoff
- Plato
- Datenintelligenz von Plato
- PlatoData
- Spieler
- Bitte
- möglich
- Potenzial
- verhindern
- früher
- Vor
- Aufgabenstellung:
- Verfahren
- Prozessdefinierung
- verarbeitet
- anpassen
- Produkt
- Produktion
- Produkte
- die
- vorausgesetzt
- Werbung
- Gemäß
- qualifiziert
- Qualität
- Roh
- Lesen Sie mehr
- Echtzeit
- Grund
- erhalten
- Rekord
- Aufzeichnungen
- Wiederholung
- reflektieren
- Registrieren
- Regulierungsbehörden
- Abgelehnt..
- bezogene
- bleiben
- Reparaturen
- wiederholen
- berichten
- Berichtet
- Reporter
- Reporting
- Meldungen
- Vertreter
- Anforderung
- erfordern
- falls angefordert
- Folge
- Die Ergebnisse
- behält
- Rückkehr
- Überprüfen
- bewertet
- Wurzel
- Sicherheit
- Vertrieb
- gleich
- sehen
- segregierten
- Sepsis
- mehrere
- Versand
- sollte
- ähnlich
- Umstände
- SIX
- Größe
- So
- etwas
- spezifisch
- Spezifikationen
- Schritt
- Shritte
- Immer noch
- Lagerung
- Streifen Konfektionierung
- Studie
- eingereicht
- sicher
- Chirurgie
- chirurgisch
- überrascht
- technisch
- vorübergehend
- Test
- Testen
- zur Verbesserung der Gesundheitsgerechtigkeit
- Das
- Die Zukunft
- dann
- Dort.
- deswegen
- Diese
- vom Nutzer definierten
- Denken
- fehlen uns die Worte.
- rechtzeitig
- zu
- sagte
- Werkzeuge
- Thema
- trainiert
- Transit
- Behandlungen
- XNUMX
- tippe
- Typen
- typisch
- nicht fähig
- für
- Unglücklicherweise
- Bereiche
- unbekannt
- -
- benutzt
- nützlich
- Nutzer
- die
- Bestätigung
- überprüfen
- Video
- visuell
- visuell
- wollen
- will
- wurde
- we
- Webinar
- GUT
- waren
- Was
- wann
- welche
- während
- WHO
- weit verbreitet
- werden wir
- mit
- ohne
- Werk
- schlimmer
- würde
- WPEngine
- Falsch
- U
- Ihr
- Youtube
- Zephyrnet